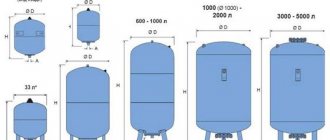
Jedním z mnoha fyzikálně-chemických procesů, které našly široké uplatnění v průmyslu i v každodenním životě, je elektrolýza - výběr na povrchu elektrod připojených ke zdroji proudu umístěného v roztoku nebo tavenině, jejich složek (čistý kov - hliník, měď, plyn atd.). Hlavní instalací, ve které probíhá tento proces, je elektrolyzér.

Elektrolyzér
Co je to elektrolyzér
Elektrolyzér je speciální zařízení sloužící k oddělení jeho složek od roztoku nebo taveniny.
Hlavní vlastnosti elektrolyzéru jsou:
- Provozní napětí pro jednu elektrodu se pohybuje od 1,8 do 2,0 V;
- Síla proudu - pro normální průběh procesu elektrolýzy je do elektrod dodáván proud s hodnotou této charakteristiky od 5 do 10 A;
- Počet elektrod - minimální počet elektrod je 2, maximum je omezeno velikostí samotné instalace a jejím účelem;
- Rozměry elektrod - jako elektrody se nepoužívají uhlíkové tyče, ale kovové desky, jejichž velikost je dána účelem instalace, charakteristikou proudu a napětí proudu dodávaného do desek;
- Vzdálenost mezi opačně nabitými povrchy elektrod - minimální vzdálenost mezi elektrodovými deskami musí být nejméně 1,5 mm;
- Materiál elektrody - v moderních elektrolyzérech se jako materiál pro anodu a katodu používá nerezový plech s niklem.
Další důležitou vlastností elektrolýzního zařízení je také použití katalyzátorů.
Taková zařízení se používají pro následující účely:
- Získání plynného kyslíku sestávajícího ze směsi vodíku a kyslíku (Brownův plyn);
- Izolace čistého hliníku, hořčíku, zinku z jejich solných tavenin;
- Čištění vody ze solí a nečistot v ní rozpuštěných;
- Aplikace tenké vrstvy niklu, zinku, která zabraňuje korozi na povrchu kovových částí;
- Dezinfekce potravinářských výrobků;
- Čištění odpadních vod z rozpuštěných solí těžkých kovů a jiných škodlivých látek.
Důležité! Platinová elektroda z obyčejného železa se v elektrolýzních zařízeních používá méně často než z nerezové oceli, protože rychleji oxiduje a stává se nepoužitelným.
Vlastní elektrolyzér
Každý si může vyrobit elektrolyzér vlastními rukama. Pro montážní proces nejběžnější konstrukce budou zapotřebí následující materiály:
- plech z nerezové oceli (nejlepší možnosti jsou zahraniční AISI 316L nebo náš 03X16H15M3);
- šrouby М6х150;
- podložky a matice;
- průhledná trubka - můžete použít vodováhu, která se používá pro stavební účely;
- několik rybích tvarovek s vnějším průměrem 8 mm;
- plastová nádoba o objemu 1,5 litru;
- malý filtr filtrující vodu z vodovodu, například filtr pro pračky;
- zpětný vodní ventil.
Proces montáže
Sbírejte elektrolyzér vlastníma rukama podle následujících pokynů:
- Nejprve musíte označit a následné řezání plechu z nerezové oceli na stejné čtverce. Řezání lze provádět úhlovou bruskou (úhlová bruska). Jeden z rohů těchto čtverců musí být pro správné zajištění desek podříznut;
- Dále musíte udělat otvor pro šroub na straně desky naproti řezu rohové pily;
- Připojení desek by mělo být provedeno postupně: jedna deska na "+", další na "-" a tak dále;
- Mezi různě nabitými deskami by měl být izolátor, který funguje jako trubka z vodováhy.Měl by být rozřezán na kroužky, které by měly být rozřezány podélně, aby se získaly pruhy o tloušťce 1 mm. Tato vzdálenost mezi deskami je dostatečná pro dobrý vývoj plynu během elektrolýzy;
- Desky jsou k sobě připevněny pomocí podložek následujícím způsobem: na šroub sedí podložka, poté deska, poté tři podložky, po desce atd. Destičky, příznivě nabité, jsou umístěny do zrcadlového obrazu negativně nabitých listů. To umožňuje zabránit tomu, aby se řezané hrany dotýkaly elektrod;


Desky zařízení na elektrolýzu se spojily
- Při montáži desek byste je měli současně izolovat a utáhnout matice;
- Každá deska musí být také vyzváněna, aby se zajistilo, že nedojde ke zkratu;
- Dále musí být celá sestava umístěna v plastové krabičce;
- Poté stojí za to zdůraznit místa, kde se šrouby dotýkají stěn kontejneru, kde vyvrtejte dva otvory. Pokud šrouby nezapadnou do kontejneru, je třeba je řezat pilou;
- Poté jsou šrouby utaženy maticemi a podložkami pro těsnost konstrukce;


Desky umístěné v plastové nádobě
- Po provedených krocích budete muset ve víku nádoby vytvořit otvory a zasunout do nich tvarovky. Nepropustnost v tomto případě lze zajistit utěsněním spár tmely na bázi silikonu;
- Pojistný ventil a filtr v konstrukci jsou umístěny na výstupu plynu a slouží jako prostředek k řízení nadměrného hromadění plynu, které může vést ke špatným výsledkům;
- Jednotka pro elektrolýzu je smontována.
Poslední fází je test, který se provádí podobným způsobem:
- naplnění nádoby vodou až po značku šroubů pro upevňovací prvky;
- připojení napájení k zařízení;
- připojení k armatuře trubky, jejíž opačný konec je spuštěn do vody.
Pokud je na zařízení aplikován slabý proud, pak bude uvolňování plynu trubicí téměř nepostřehnutelné, ale bude možné jej sledovat zevnitř elektrolyzéru. Zvýšením střídavého proudu a přidáním alkalického katalyzátoru do vody lze výrazně zvýšit výtěžek plynu.
Vyrobený elektrolyzér je zpravidla důležitou součástí mnoha zařízení, například vodíkovým hořákem.


vzhled vodíkového hořáku, jehož základ je považován za vlastní elektrolyzér
Znáte-li typy, klíčové vlastnosti, zařízení a pracovní princip iontových zařízení, můžete provést správnou montáž domácí konstrukce, která je vynikajícím pomocníkem v různých každodenních situacích: od svařování a úspory spotřeby paliva motorových vozidel po fungování topných systémů.
Zařízení a princip činnosti
Katoda a anoda
Nejjednodušší zařízení na elektrolýzu se skládá z několika „článků“, z nichž každý zahrnuje:
- 2 deskové elektrody - katoda (negativní) a anoda (pozitivní);
- Gumové těsnění po obvodu dvou sousedních odlišných elektrod.
Vnější články jsou vybaveny speciálními trubkami, kterými jsou odváděny uvolněné plyny.
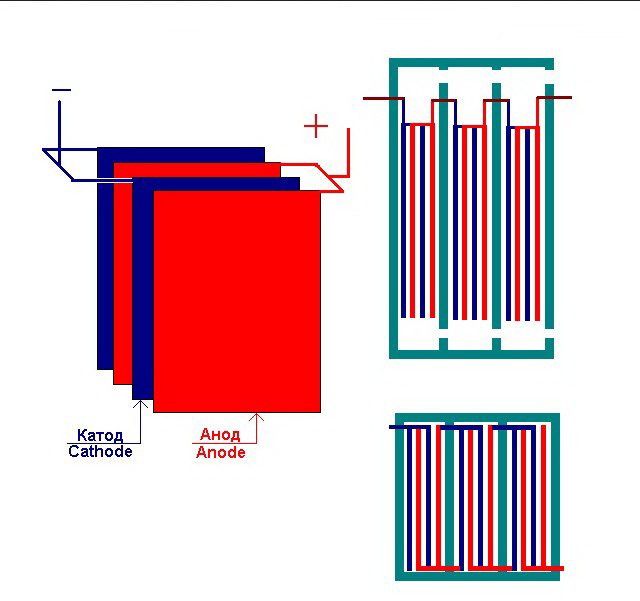

Několik vzájemně propojených „článků“ elektrolýzního závodu
Elektrolyzér může obsahovat od 1 do 30–40 nebo více takových „článků“, desky stejného jména jsou zapojeny do série.
Důležité! Při použití napájecích zdrojů se střídavým proudem se dodatečně používají usměrňovače, z nichž nejjednodušší je diodový můstek.
Taková instalace funguje následovně:
- Do prostoru mezi elektrodami se nalije destilovaná voda s v ní rozpuštěnou zásadou nebo obyčejná jedlá soda;
- Z napájecího zdroje na elektrody všech článků instalace se dodává napětí 1,8–2,0 V;
- V důsledku procesu elektrolýzy jsou anionty (kladně nabité ionty) látky rozpuštěné ve vodě přitahovány k záporně nabité katodě, v důsledku čehož se na ní vytvoří tenký sodíkový film;
- Na kladně nabité anodě dochází ke zničení molekul vody, přičemž každý z nich tvoří 2 atomy vodíku a 1 atom kyslíku;
- Uvolněný detonační plyn větvícími trubkami vstupuje do jím určené nádoby.
Intenzita procesu elektrolýzy závisí na síle napětí a proudu - při nízkých hodnotách těchto charakteristik nebude proces pokračovat. Pokud napájecí zdroj dodává proud s příliš vysokými hodnotami charakteristiky proudu a napětí, roztok nalitý do elektrolyzéru bude velmi horký a bude se vařit.
Ladění a testování zařízení
Poté je nutné určit, kde se šrouby dotýkají stěn krabice, a na těchto místech vyvrtat dva otvory. Pokud se bez zjevného důvodu ukáže, že šrouby do kontejneru nezapadají, pak by měly zastřihněte a utáhněte na těsnost pomocí matic... Nyní musíte vyvrtat kryt a zasunout tam závitové konektory z obou stran. Aby byla zajištěna nepropustnost, měl by být spoj utěsněn tmelem na bázi silikonu.
Po sestavení vlastního elektrolyzéru vlastníma rukama byste to měli vyzkoušet. Chcete-li to provést, připojte zařízení ke zdroji napájení, naplňte ji vodou do šroubů, nasaďte víčko připojením hadice k armatuře a spuštěním opačného konce trubky do vody. Pokud je proud slabý, bude proud viditelný zevnitř elektrolyzéru.
Postupně zvyšujte proud ve vašem domácím spotřebiči. Destilovaná voda nevede dobře elektřinu, protože neobsahuje žádné soli ani nečistoty. Pro přípravu elektrolytu je nutné přidat do vody alkálie. K tomu musíte vzít hydroxid sodný (obsažený v prostředcích na čištění trubek, jako je "Mole"). Je zapotřebí pojistný ventil, aby se zabránilo hromadění slušného množství plynu.
- Je lepší použít jako katalyzátor destilovanou vodu a sódu.
- Měli byste smíchat trochu jedlé sody se čtyřiceti díly vody. Stěny po stranách jsou nejlépe z akrylového skla.
- Elektrody jsou nejlépe vyrobeny z nerezové oceli. Má smysl používat zlato na talíře.
- Jako podklad použijte průsvitné PVC. Mohou mít velikost 200 x 160 milimetrů.
- K vaření potravin můžete použít vlastní elektrolyzér, který jste si sami vyrobili, a to pro úplné spalování benzínu v automobilech a ve většině případů.
Suché elektrolyzéry se používají hlavně pro stroje. Generátor zvyšuje výkon spalovacího motoru. Vodík se vznítí mnohem rychleji než kapalné palivo, čímž se zvýší síla pístu. Kromě Mole si můžete vzít Mister Muscle, louh sodný, sódu na pečení.
Generátor nefunguje na pitnou vodu. Je lepší připojit elektřinu takto: první a poslední deska - minus a na desce uprostřed - plus. Čím větší je plocha desek a čím silnější je proud, tím více plynu se uvolní.
Druhy elektrolyzérů
DIY bodové svařování pro baterie
V závislosti na konstrukci a principu provozu existuje 5 typů elektrolýzních zařízení.
Suchý
Takové elektrolyzéry sestávají z deskových elektrod oddělených utěsněnými gumovými těsněními. „Buňky“ instalace jsou často dodatečně umístěny v uzavřeném krytu.
Vodík a kyslík generované v důsledku elektrolýzy jsou odstraňovány speciálními odbočkami umístěnými na konci těla nebo krajními deskami zařízení.
Tekoucí
Elektrolýza tohoto typu má následující zařízení:
- Elektrolýzní lázeň (těleso) se dvěma tryskami, z nichž jedna je přiváděna do ní elektrolytem, druhou je odpalován plyn vznikající v důsledku elektrolýzy;
- Deskové elektrody oddělené rozpěrkami;
- Nádrž s elektrolytem umístěná nad pouzdrem s elektrodami a připojená hadicemi k odbočkám potrubí elektrolýzní lázně zařízení a mající odbočku s plynovým ventilem v horní části.
Během provozu takového zařízení uvolňovaný plyn přes odbočné potrubí a hadici vstupuje do nádrže s elektrolytem a vytváří v něm určitý tlak a opouští instalaci přes ventil na odbočném potrubí.
Membrána
Elektrolýzové články takových instalací se skládají ze dvou elektrod oddělených tenkou membránou, která umožňuje průchod produktů elektrolýzy a odděluje elektrody od sebe navzájem.
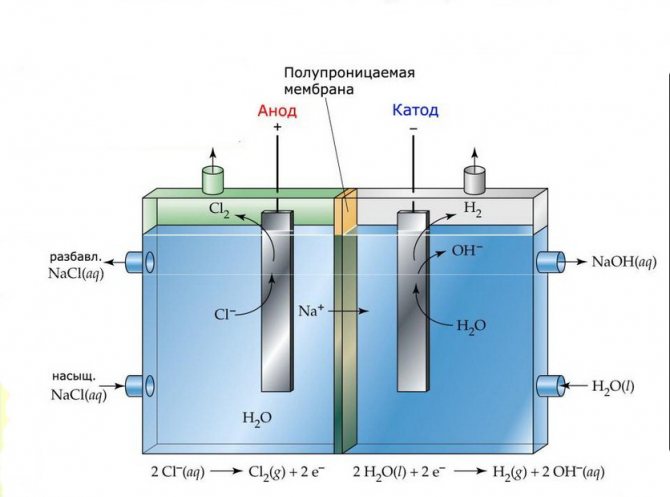

Membránová elektrolýza
Membrána
Elektrolýzní zařízení tohoto typu se skládají z baňky ve tvaru písmene „U“, do které jsou vloženy dvě elektrody a 2–3 nepropustných membrán. Podobné elektrolyzéry se používají pro samostatnou výrobu čistého vodíku a kyslíku.
Alkalické
Na rozdíl od jiných modelů elektrolyzérů se v nich alkalický roztok používá jako elektrolyt - louh sodný (hydroxid sodný), který je nejen dalším zdrojem vodíku a kyslíku, ale také katalyzátorem pro elektrolýzu.


Alkalický obvod elektrolyzéru
Taková zařízení, na rozdíl od analogů jiných typů, umožňují použití levnějších elektrod z obyčejného železa.
Proveďte elektrolyzér vlastními rukama
Jistě jste obeznámeni s procesem elektrolýzy z osnov základní školy. To je, když jsou 2 polární elektrody umístěny do vody pod proudem, aby se získaly kovy nebo nekovy v čisté formě. K rozložení molekul vody na kyslík a vodík je zapotřebí elektrolyzér. Elektrolyzér jako součást vědeckých mechanismů rozděluje molekuly na ionty.
Existují dva typy tohoto zařízení:
- Suchý elektrolyzér (jedná se o zcela uzavřený článek);
- Mokrý elektrolyzér (jedná se o dvě kovové desky umístěné v nádobě s vodou).
Toto zařízení je z hlediska zařízení jednoduché, což umožňuje používat i doma... Elektrolyzéry rozdělují náboje elektrolýzy atomů molekul na nabité atomy.
V našem případě rozděluje vodu na pozitivní vodík a negativní kyslík. K tomu je zapotřebí velké množství energie a aby se z požadovaného množství energie odešlo méně, použije se katalyzátor.
Elektrolyzér na výrobu vodíku
Výpočet uzemnění
Chcete-li sestavit nejjednodušší elektrolyzér vlastními rukama, můžete použít výkres zobrazený na obrázku.


Nákres nejjednoduššího domácího elektrolyzéru
Poznámka! Elektrolyzér je poměrně nebezpečná instalace, která během provozu může hromadit ve velkém množství kyslíkatý plynný plyn, který může způsobit vážnou explozi. Jednotka by neměla být umístěna v blízkosti zdrojů otevřeného ohně a topných zařízení.
DIY elektrolyzér pro auto
Pro zlepšení spalování paliva v motoru automobilu se často montuje elektrolyzér, který se skládá z pouzdra ze staré baterie s nerezovými deskami umístěnými uvnitř, ze dvou trysek, z nichž jedna je připojena k nádrži naplněné elektrolytem, druhá je připojeno k hadici dodávající vzduch k motoru (přesněji zvlněné od přívodu vzduchu k vzduchovému filtru).
Takový domácí tekoucí elektrolyzér je napájen z baterie automobilu pomocí relé a 10 A pojistky.
Vytváříme zařízení vlastními rukama
Zařízení pro tento proces lze provést ručně.
K tomu budete potřebovat:
- Nerezový plech;
- Šrouby M6 x 150;
- Podložky;
- Ořechy;
- Průhledná trubice;
- Spojovací prvky se závitem na obou stranách;
- Jeden a půl litru plastové nádoby;
- Vodní filtr;
- Zpětný ventil na vodu.
Vynikající volbou pro nerezovou ocel je AISI 316L od zahraničního výrobce nebo 03X16H15M3 od výrobce z naší země. Není nutné kupovat nerezovou ocel, můžete si vzít starou. Stačí vám 50 až 50 centimetrů.
„Proč brát samotnou nerezovou ocel?“ - ptáte se. Protože nejběžnější kov bude korodovat. Nerezová ocel lépe snáší alkálie. By měl obrys listu tak, aby byl rozdělen na 16 podobných čtverců... Můžete jej řezat úhlovou bruskou. V každém čtverci vyřízněte jeden z rohů.
Na druhé straně a opačném rohu, z odříznutého rohu, vyvrtejte otvor pro šroub, který pomůže držet desky pohromadě. Elektrolyzér nepřestává fungovat takto:Na desku proudí elektřina desky - a voda se rozkládá na kyslík a vodík. Díky tomu potřebujeme dobrou a negativní desku.
Desky musí být připojeny střídavě: plus-minus-plus-minuss podobnou metodou bude silný proud. K izolaci desek od jedné se používá trubice. Z úrovně je vyříznut prsten. Řezáním získáme pás o tloušťce milimetru. Tato vzdálenost je správnější pro výrobu plynu.
Desky jsou vzájemně propojeny s podložkami: na šroub položíme podložku, poté desku a tři podložky, pak znovu desku atd. Plus a minus musí být zasazeno osm talířů. Pokud je vše provedeno správně, pak se řezy desek nedotknou elektrod.
Poté musíte matice utáhnout a destičky izolovat. Poté vložíme konstrukci do plastové nádoby.
Přehled výrobců elektrolyzéru
Hlavními výrobci elektrolyzérů jsou jak domácí podniky (RUSAL, NPF RutTech, JSC Uralkhimmash), tak jejich zahraniční konkurenti - Teledyne Energy Systems, Inc (USA), Hydrogenics Corp. (Belgie).
Elektrolyzér je tedy poměrně jednoduchá a na funkce bohatá instalace používaná k výrobě plynného kyslíku, který se v budoucnu plánuje použít jako palivo pro spalovací motory a topné kotle.
Udělejte si domácí elektrolýzu
Když jsem byl malý, vždy jsem chtěl něco udělat sám, vlastníma rukama. Ale rodiče (a další blízcí lidé) to ve většině případů nedovolili. A neviděl jsem tehdy (a dosud nevidím) nic špatného, když se malé děti chtějí učit ??
Tento článek jsem samozřejmě nenapsal, abych si vzpomněl na zážitky z dětství v touze zahájit sebevzdělávání. Jen náhodou, když jsem surfoval na internetu, narazil jsem na otázku tohoto druhu. Nějaký malý chlapec z bombardéru se ptal, jak provádět elektrolýzu doma. Je pravda, že jsem mu neodpověděl, protože tento chlapec chtěl elektrolyzovat bolestivě podezřelou směs ?? Rozhodl jsem se, že už nebudu z hříchu říkat dále, dovolte mi nahlédnout do knih sám. Ale ne tak dávno jsem znovu bloudil po fórech a viděl jsem podobnou otázku od učitele na chemické škole. Podle popisu je jeho škola tak špatná, že si nemůže (nechce) koupit elektrolyzér za 300 rublů. Učitel (jaký problém!) Nenašel východisko z výsledné situace. Tak jsem mu pomohl. Pro ty, kteří jsou zvědaví na tento druh domácích produktů, zveřejňuji tento článek na webu.
Ve skutečnosti je výrobní proces a použití naší vlastní palety velmi primitivní. Nejprve vám ale řeknu o bezpečnosti a o výrobě - až na druhé. Jde o to, že mluvíme o demonstračním elektrolyzéru, a ne o průmyslové instalaci. Díky tomu bude z důvodu bezpečnosti dobré jej napájet nikoli ze sítě, ale z AA baterií nebo z baterie. Přirozeně, čím vyšší napětí, tím rychleji bude proces elektrolýzy probíhat. Pro vizuální pozorování plynových bublin je to však docela dost 6 V, ale 220 je již nadměrné. s takovým napětím bude například voda vařit nejrychleji, a to není příliš bezpečné ... No, myslím, že jsi přišel na napětí?
Nyní si promluvme o tom, kde a za jakých podmínek budeme experimentovat. Úplně první věc by měla být buď volná plocha, nebo dobře větraná místnost. I když jsem dělal všechno v bytě se zavřenými okny a nic podobného? Zadruhé, experiment se nejlépe provádí na dobrém stole. Slovo „dobrý“ znamená, že stůl musí být stabilní, lépe těžký, tuhý a připevněný k povrchu podlahy. V tomto případě musí být pokrývka stolu odolná vůči agresivním látkám. Mimochodem, dlaždice z dlaždice je pro to ideální (i když ne každý, bohužel). Taková tabulka se bude hodit nejen pro tuto zkušenost. Všechno jsem však dělal na obyčejné stoličce ?? Za třetí, během experimentu nemusíte přesouvat zdroj energie (v mém případě baterie). Díky tomu je pro spolehlivost nejlepší je okamžitě položit na stůl a opravit, aby se nehnuly. Věřte mi, je to pohodlnější, než je pravidelně držet rukama. Jednoduše jsem si svázal vlastní baterie elektrickou páskou k prvnímu tvrdému předmětu, který jsem viděl. Za čtvrté, jídla, ve kterých budeme experimentovat, ať jsou malá. Jednoduché sklo nebo sklenice. Mimochodem, toto je nejoptimálnější způsob, jak používat brýle doma, na rozdíl od nalití alkoholu do nich s dalším použitím ...
No, pojďme přejít konkrétně k zařízení. Je to uvedeno na obrázku, ale prozatím stručně vysvětlím, co a co.
Musíme si vzít jednoduchou tužku, odstranit z ní strom obyčejným nožem a vytáhnout z tužky celé vodítko. Můžete si však vzít vodítko z mechanické tužky. Existují však dvě potíže najednou. První je obvyklý. Olovo z mechanické tužky je příliš tenké, pro nás to prostě není vhodné pro vizuální experiment. Druhou obtížností je nepochopitelné složení současných balíků. Cítím, že nejsou vyrobeny z grafitu, ale z něčeho jiného. Obecně moje zkušenost s takovým „olovem“ nebyla vůbec úspěšná, dokonce ani při napětí 24 V. Díky tomu jsem potřeboval vybrat dobrou dřevitou jednoduchou tužku. Výsledná grafitová tyč bude pro nás sloužit jako elektroda. Jak si dokážete představit, potřebujeme dvě elektrody. Díky tomu si vybereme druhou tužku, nebo jednoduše zlomíme stávající tyč na dvě části. Vlastně jsem to udělal.
U každého drátu, který vám přijde po ruce, obalíme první olověnou elektrodu (jedním koncem drátu) a tento vodič připojíme k minusu zdroje energie (druhým koncem). Pak vezmeme druhé vedení a uděláme to samé s ním. K tomu, na základě toho, potřebujeme druhý vodič. Ale v tomto případě připojíme tento vodič k plusu napájecího zdroje. Pokud máte problémy s připevněním křehké grafitové tyče k drátu, můžete použít po ruce nástroje, jako je páska nebo lepicí páska. Pokud se nepodařilo obalit hrot grafitu samotným drátem a páska nebo izolační páska neposkytovaly těsný kontakt, zkuste vodítko lepit vodivým lepidlem. Pokud toto nemáte, pak alespoň svázejte vodič o drát pomocí nitky. Není třeba se bát, nit z takového napětí nevyhoří ??
Pro ty, kteří nevědí nic o bateriích a jednoduchých pravidlech pro jejich připojení, trochu vysvětlím. Baterie typu finger produkuje napětí 1,5 V. Na obrázku mám dvě podobné baterie. Navíc jsou propojené postupně - jeden po druhém, ne paralelně. Při podobném (sériovém) připojení bude konečné napětí sečteno z napětí každé baterie, to je pro mě 1,5 + 1,5 = 3,0 V. To je méně než dříve uvedených 6 voltů. Ale byl jsem příliš líný na to, abych si koupil ještě pár baterií. Princip ty a tak musí být jasný ??
Začněme experiment. Například se omezíme na elektrolýzu vody.Zaprvé je velmi přístupný (doufám, že čtenář tohoto článku nežije na Sahaře), zadruhé je neškodný. Kromě toho ukážu, jak se stejným zařízením (elektrolyzérem) se stejnou látkou (vodou) provést dva rozličný Zkušenosti. Myslím, že máte dostatek představivosti, abyste vymysleli spoustu podobných experimentů s jinými látkami ?? Voda z vodovodu je pro nás obecně vhodná. Ale doporučuji přidat trochu víc a posolit. Trochu - to znamená malou špetku, ne celou dezertní lžičku. Toto je důležité! Sůl dobře promíchejte, aby se rozpustila. Voda, která je dielektrikum v čistém stavu, bude tedy dokonale vést elektřinu. na začátku experimentu otřete stůl od potenciální vlhkosti a poté na něj položte zdroj energie a sklenici vody.
Obě elektrody, přítomné pod napětím, spustíme do vody. Současně zajistěte, aby byl do vody ponořen pouze grafit a samotný drát by se vody neměl dotýkat. Začátek experimentu může být odložen. Čas závisí na mnoha ukazatelích: na složení vody, kvalitě drátů, kvalitě grafitu a samozřejmě napětí zdroje energie. Začátek mé reakce se na pár sekund zpozdil. Kyslík se začíná vyvíjet na elektrodě, která byla připojena k bateriím plus. Na elektrodě připojené k minusu se uvolní vodík. Je třeba poznamenat, že vodíkových bublin je více. Kolem části grafitu, která je ponořena ve vodě, se drží velmi malé bublinky. Poté začnou některé bubliny plavat.
Elektroda na začátku experimentu. Zatím nejsou žádné plynové bubliny. Na elektrodě připojené k zápornému pólu baterií se vytvořily vodíkové bubliny
Jaké další experimenty mohou existovat? Pokud jste si už s vodíkem a kyslíkem hráli dost, pokračujeme dalším experimentem. Je to zajímavější, zejména pro domácí vědce. Zajímavé je, že je možné to nejen vidět, ale také cítit. V minulých zkušenostech jsme dostávali kyslík a vodík, což podle mého názoru není příliš velkolepé. A v dalším experimentu dostaneme dvě látky (mimochodem užitečné v každodenním životě). na začátku experimentu zastavte předchozí experiment a vysuňte elektrody. Nyní vezměte kuchyňskou sůl (kterou obvykle používáte v kuchyni) a rozpusťte ji ve vodní hmotě. V tomto případě ne malé množství. Slušné množství soli je ve skutečnosti jediná věc, díky které se druhá zkušenost liší od první. Po rozpuštění soli můžete experiment okamžitě opakovat. Nyní probíhá jiná reakce. Na dobré elektrodě se nyní neuvolňuje kyslík, ale chlor. Negativně se také uvolňuje vodík. Pokud jde o sklo, ve kterém se nachází solný roztok, zůstává v něm po delší elektrolýze hydroxid sodný. Toto je známá louh sodný, alkalický.
Chlór, budeš to cítit. Ale pro nejlepší účinek doporučuji použít napětí alespoň 12 V. V opačném případě možná nebudete cítit vůni. Přítomnost zásady (po velmi dlouhé elektrolýze) ve skle lze zkontrolovat několika způsoby. Nejjednodušší a nejnásilnější je dát ruku do sklenice. Etnické znamení říká, že pokud začne pálení, ve skle je alkálie. Chytřejší a výraznější způsob je lakmusový test. Pokud je vaše škola tak špatná, že není schopna ani lakmusového papíru, příslušné ukazatele vám pomohou. Jeden z nich, jak se říká, může sloužit jako kapka řepné šťávy ?? Je ale docela možné do roztoku nakapat trochu tuku. Pokud vím, mělo by dojít k zmýdelnění.
Pro velmi zvědavé popíšu, co se vlastně stalo během experimentů. V prvním experimentu pod vlivem elektrického proudu proběhla podobná reakce: 2 H2O >>> 2 H2 + O2 Oba plyny přirozeně plují z vody na povrch. Mimochodem, plovoucí plyny mohou být zachyceny. Zvládnete to sami?
V dalším experimentu byla reakce úplně jiná.Bylo také iniciováno elektrickým proudem, ale nyní jako činidla působila nejen voda, ale také sůl: 4H2O + 4NaCl >>> 4NaOH + 2H2 + 2Cl2 Pamatujte, že reakce musí probíhat v přebytku vody. Chcete-li zjistit, jaké množství soli je považováno za největší, můžete jej spočítat z výše uvedené reakce. Můžete také přemýšlet o tom, jak vylepšit zařízení nebo jaké další experimenty lze provést. Je skutečně možné, že chlornan sodný lze získat elektrolýzou. Za laboratorních podmínek se ve většině případů získává průchodem plynného chloru roztokem hydroxidu sodného.