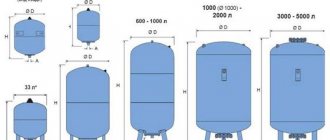
Az egyik a fizikai-kémiai folyamatok közül, amelyek széles körben alkalmazhatók mind az iparban, mind a mindennapi életben, az elektrolízis - az áramforráshoz kapcsolt, oldatba vagy olvadékba helyezett elektródák felületének szelekciója, alkatrészeik (tiszta fém - alumínium) , réz, gáz stb.). A fő telepítés, amelyen belül ez a folyamat zajlik, egy elektrolizátor.

Elektrolizátor
Mi az elektrolízis
Az elektrolizátor egy speciális berendezés, amelyet alkatrészeinek elválasztásához oldattól vagy olvadéktól kell használni.
Az elektrolízis fő jellemzői:
- Az egyik elektróda üzemi feszültsége 1,8 és 2,0 V között mozog;
- Áramerősség - az elektrolízis folyamatának normál lefolyása érdekében áramot juttatnak az elektródákhoz, ennek a jellemzőnek az értéke 5-10 A;
- Elektródák száma - az elektródák minimális száma 2, a maximumot maga a telepítés mérete és célja korlátozza;
- Az elektródák méretei - nem szénrudakat használnak elektródaként, hanem fémlemezeket, amelyek méretét a telepítés célja határozza meg, a lemezekre juttatott áram áramfeszültség-jellemzői;
- Az ellentétesen töltött elektróda felületek közötti távolság - az elektródalemezek közötti minimális távolságnak legalább 1,5 mm-nek kell lennie;
- Elektróda anyaga - a modern elektrolizátorokban az anód és a katód anyagaként rozsdamentes acéllemezt használnak nikkelből.
Az elektrolízis üzem másik fontos jellemzője a katalizátorok használata.
Az ilyen berendezéseket a következő célokra használják:
- Oxigénhidrogéngáz előállítása, amely hidrogén és oxigén keverékéből áll (Brown-gáz);
- A tiszta alumínium, magnézium, cink elkülönítése sóikból;
- Víz tisztítása sókból és a benne oldott szennyeződésekből;
- Vékony nikkelréteg, cink, amely megakadályozza a korróziót a fémrészek felületén;
- Élelmiszerek fertőtlenítése;
- Szennyvíz tisztítása nehézfémek és egyéb káros anyagok oldott sóiból.
Fontos! A közönséges vasból készült platinaelektródát ritkábban használják az elektrolízis létesítményekben, mint a rozsdamentes acélt, mivel gyorsabban oxidálódik és használhatatlanná válik.
Saját gyártású elektrolizátor
Bárki saját kezűleg készíthet elektrolizátort. A leggyakoribb tervezésű összeszerelési folyamathoz a következő anyagokra lesz szükség:
- rozsdamentes acéllemez (a legjobb lehetőség a külföldi AISI 316L vagy a miénk 03X16H15M3);
- csavarok М6х150;
- alátétek és anyák;
- átlátszó cső - használhat vízmértéket, amelyet építési célokra használnak;
- több halszálka-szerelvény, amelynek külső átmérője 8 mm;
- műanyag tartály, amelynek térfogata 1,5 liter;
- egy kis szűrő a csapvíz szűrésére, például egy mosógépekhez való szűrő;
- visszacsapó vízszelep.
Összeszerelési folyamat
Gyűjtse össze saját kezével az elektrolizátort az alábbi utasítások szerint:
- Először meg kell jelölnie és a rozsdamentes acéllemez későbbi fűrészelését azonos négyzetekre. A fűrészelés sarokcsiszolóval végezhető (sarokcsiszoló). Az ilyen négyzetek egyik sarkát szögben kell levágni a lemezek megfelelő rögzítéséhez;
- Ezután lyukat kell készítenie a csavar számára a lemez sarokvágással ellentétes oldalán;
- A lemezek összekapcsolását egymás után kell elvégezni: az egyik lemezt a "+" -on, a következőt a "-" -on és így tovább;
- A különböző töltésű lemezek között kell lennie egy szigetelőnek, amely csőként működik a vízmértéktől.Karikákra kell vágni, amelyeket hosszában vágni kell, hogy 1 mm vastag csíkokat kapjunk. Ez a lemezek közötti távolság elegendő a jó gázfejlődéshez az elektrolízis során;
- A lemezeket alátétek segítségével rögzítik az alábbiak szerint: alátét ül a csavaron, majd egy lemez, majd egy lemez után három alátét és így tovább. A kedvezően feltöltött lemezeket negatív töltésű lapok tükörképébe helyezzük. Ez lehetővé teszi, hogy a fűrészelt élek ne érjenek az elektródákhoz;


Elektrolízis üzemben összeállított lemezek
- A lemezek összeszerelésekor egyszerre kell elkülöníteni és meghúzni az anyákat;
- Ezenkívül minden lemezt meg kell gyűrűzni annak biztosítása érdekében, hogy nincs rövidzárlat;
- Továbbá az egész szerelvényt egy műanyag dobozba kell helyezni;
- Ezt követően érdemes kiemelni azokat a helyeket, ahol a csavarok érintik a tartály falát, ahol két lyukat fúr. Ha a csavarok nem illenek a tartályba, akkor fémfűrésszel kell őket levágni;
- Ezután a csavarokat anyákkal és alátétekkel meghúzza a szerkezet szorossága érdekében;


Műanyag tartályba helyezett lemezek
- A megtett lépések után lyukakat kell készítenie a tartály fedelében, és bele kell illeszteni a szerelvényeket. Az áthatolhatatlanság ebben az esetben az ízületek szilikon alapú tömítőanyagokkal történő lezárásával biztosítható;
- A szerkezetben egy biztonsági szelep és szűrő a gáz kimenetén helyezkedik el, és a gáz túlzott felhalmozódásának ellenőrzésére szolgál, ami rossz eredményekhez vezethet;
- Az elektrolízis egység össze van szerelve.
Az utolsó szakasz egy teszt, amelyet hasonló módon hajtanak végre:
- a tartály feltöltése vízzel a rögzítőelemek csavarjainak jeléig;
- áramellátás csatlakoztatása a készülékhez;
- csatlakozás a cső illesztéséhez, amelynek átellenes végét a vízbe engedjük.
Ha gyenge áramot vezetnek a berendezésre, akkor a gáz kibocsátása a csövön keresztül szinte észrevehetetlen lesz, de az elektrolizáló belsejéből figyelemmel kísérhető. A váltakozó áram növelésével, lúgos katalizátor hozzáadásával a vízhez jelentősen növelhető a gáznemű anyag hozama.
Az elkészített elektrolizátor általában sok eszköz fontos része, például egy hidrogén-égő.


hidrogénégő megjelenése, amelynek alapját saját gyártású elektrolizátornak tekintik
Az ionos berendezések típusainak, főbb jellemzőinek, eszközének és működési elvének ismeretében elvégezheti a házilag gyártott szerkezet helyes összeszerelését, amely kiváló segítség a mindennapi helyzetekben: a hegesztéstől és a gépjárművek üzemanyag-fogyasztásának megtakarításától kezdve a fűtési rendszerek működése.
Eszköz és a működés elve
Katód és anód
A legegyszerűbb elektrolízisüzem több "cellából" áll, amelyek mindegyike a következőket tartalmazza:
- 2 lemezes elektróda - katód (negatív) és anód (pozitív);
- Gumi tömítés két szomszédos, egymástól eltérő elektróda kerületén.
A külső cellák speciális csövekkel vannak felszerelve, amelyeken keresztül a képződött gázok távoznak.
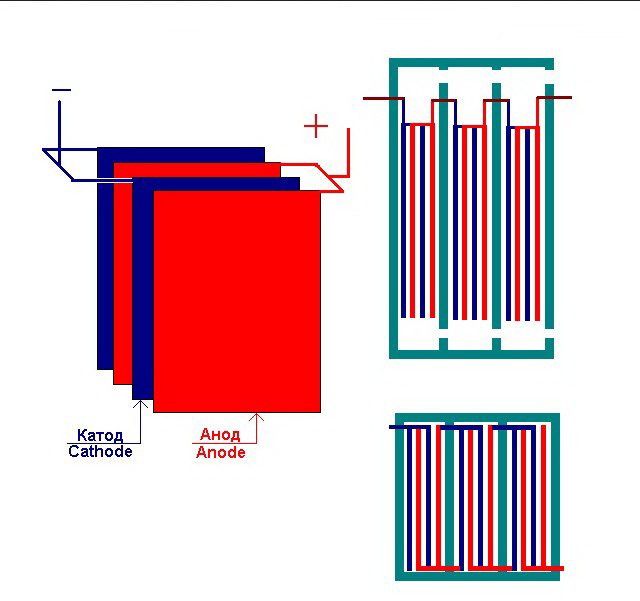

Az elektrolízis üzem több egymáshoz kapcsolódó "cellája"
Az elektrolizátor 1-30-40 vagy több ilyen "cellát" tartalmazhat, az azonos nevű lemezek sorba vannak kapcsolva.
Fontos! Váltóáramú tápegységek használata esetén egyenirányítókat is használnak, amelyek közül a legegyszerűbb a diódahíd.
Egy ilyen telepítés a következőképpen működik:
- Desztillált vizet alkáli oldattal vagy közönséges szódabikarbónát öntünk az elektródák közötti térbe;
- 1,8-2,0 V feszültséget táplálnak az áramellátásból a berendezés összes cellájának elektródáiba;
- Az elektrolízis eredményeként egy vízben oldott anyag anionjai (pozitív töltésű ionjai) vonzódnak a negatív töltésű katódhoz, amelynek eredményeként vékony nátrium-film képződik rajta;
- Egy pozitív töltésű anódon a vízmolekulák pusztulása következik be, miközben mindegyikből 2 hidrogénatom és 1 oxigénatom képződik;
- Az elágazó csöveken keresztül felszabaduló robbanó gáz jut a számára szánt tartályba.
Az elektrolízis folyamatának intenzitása a feszültségtől és az áramerősségtől függ - ezen jellemzők alacsony értékeinél a folyamat nem folytatódik. Ha az áramforrás olyan áramot szolgáltat, amelynek túl nagy az áramfeszültség-jellemző értéke, akkor az elektrolizátorba öntött oldat nagyon forró lesz, és forrni kezd.
Az eszköz hibakeresése és tesztelése
Ezután meg kell határozni, hogy a csavarok hol érintsék a doboz falát, és ezeken a helyeken két lyukat fúrni. Ha nyilvánvaló ok nélkül kiderül, hogy a csavarok nem illenek a tartályba, akkor meg kell vágja le és húzza meg szorosan anyákkal... Most ki kell fúrnia a fedelet, és mindkét oldalról be kell helyeznie a menetes csatlakozókat. Az át nem eresztő képesség biztosítása érdekében az illesztést szilikon alapú tömítőanyaggal kell lezárni.
Miután saját kezűleg összeállította saját elektrolizátorát, tesztelje. Ehhez csatlakoztassa az eszközt egy áramforráshoz, töltse fel vízzel a csavarokig, tegye a fedelet úgy, hogy egy csövet csatlakoztat a csatlakozóhoz, és a cső másik végét leereszti a vízbe. Ha az áram gyenge, akkor az áram az elektrolizátor belsejéből látható lesz.
Fokozatosan növelje a házi készülék áramát. A desztillált víz nem vezeti jól az áramot, mivel nem tartalmaz sókat és szennyeződéseket. Az elektrolit előállításához lúgot kell adni a vízhez. Ehhez nátrium-hidroxidot kell bevinnie (amely a csövek tisztítására szolgáló eszközökben található, például a "Vakond"). Biztonsági szelepre van szükség, hogy megakadályozzuk a megfelelő mennyiségű gáz felhalmozódását.
- Katalizátorként jobb desztillált vizet és szódát használni.
- Keverje össze a szódabikarbóna egy részét negyven rész vízzel. Az oldalakon lévő falak legjobban akrilüvegből készülnek.
- Az elektródák a legjobbak rozsdamentes acélból. Van értelme aranyat használni a lemezekhez.
- Használjon áttetsző PVC-t a hátlapon. 200 x 160 milliméter méretűek lehetnek.
- Használhatja saját, saját maga gyártott elektrolizálóját ételkészítéshez, benzin teljes elégetéséhez az autókban és a legtöbb esetben.
A száraz elektrolizátorokat elsősorban gépekhez használják. A generátor növeli az égésű motor teljesítményét. A hidrogén sokkal gyorsabban gyullad ki, mint a folyékony üzemanyag, növelve a dugattyú erejét. A Mole mellett beveheti a Mister Muscle-t, a maró nátriumot, a szódabikarbónát.
A generátor nem működik ivóvízzel. Jobb, ha ilyen módon csatlakoztatja az áramot: az első és az utolsó lemez - mínusz, és a közepén lévő lemezen - plusz. Minél nagyobb a lemezek területe és minél erősebb az áram, annál több gáz szabadul fel.
Az elektrolizátorok típusai
DIY ponthegesztés elemekhez
A kiviteltől és a működési elvtől függően 5 típusú elektrolízis-üzem létezik.
Száraz
Ezek az elektrolizátorok lemezelektródákból állnak, amelyeket lezárt gumitömítések választanak el egymástól. Gyakran a létesítmény "celláit" ráadásul egy lezárt házba helyezik.
Az elektrolízis eredményeként keletkező hidrogént és oxigént a test végén vagy a berendezés szélső lapjain elhelyezett speciális elágazó csöveken keresztül távolítják el.
Folyó
Az ilyen típusú elektrolízis berendezések a következő eszközzel rendelkeznek:
- Két fúvókával ellátott elektrolízis fürdő (test), amelyek közül az egyiken keresztül elektrolit kerül bevezetésre, a másodikon keresztül az elektrolízis eredményeként képződött detonáló gáz ürül;
- Távtartókkal elválasztott lemezelektródák;
- Elektrolittartály, amely a ház fölött helyezkedik el, elektródákkal és tömlőkkel csatlakozik a berendezés elektrolízisfürdőjének elágazócsöveihez, és amelynek felső részén elágazócső található gázszeleppel.
Egy ilyen eszköz működése során az elágazó csövön keresztül kialakult gáz és a tömlő az elektrolittal együtt bejut a tartályba, és bizonyos nyomást létrehozva benne, az elágazó cső szelepén keresztül távozik a berendezésből.
Membrán
Az ilyen berendezések elektrolízis cellái két elektródából állnak, amelyeket vékony membrán választ el, amely lehetővé teszi az elektrolízis termékek áthaladását és elválasztja az elektródákat egymástól.
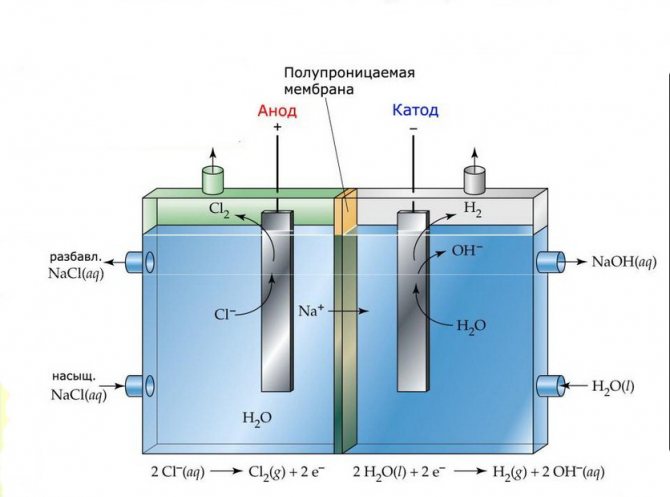

Membrán elektrolízis üzem
Diafragma
Az ilyen típusú elektrolízis berendezések egy "U" alakú lombikból állnak, amelyben két elektróda van behelyezve, és 2-3 át nem eresztő membrán. Hasonló elektrolizátorokat használnak a tiszta hidrogén és oxigén külön gyártásához.
Lúgos
Az elektrolizátorok más modelljeivel ellentétben ezekben egy alkáli oldatot használnak elektrolitként - maró nátriumot (nátrium-hidroxid), amely nemcsak kiegészítő hidrogén- és oxigénforrás, hanem az elektrolízis katalizátora is.


Alkáli elektrolízis áramkör
Az ilyen berendezések, ellentétben a más típusú analógokkal, lehetővé teszik az olcsóbb, hagyományos vasból készült elektródák használatát.
Saját kezűleg végezze el az elektrolízist
Bizonyára ismeri az elektrolízis folyamatát az általános iskolai tananyagból. Ekkor 2 poláris elektródát áram alá helyeznek vízbe annak érdekében, hogy tiszta vagy nemfémeket kapjanak. Elektrolizátorra van szükség a vízmolekulák oxigénné és hidrogénné bontásához. Az elektrolizátor a tudományos mechanizmusok részeként a molekulákat ionokra osztja.
Ennek az eszköznek két típusa van:
- Száraz elektrolizátor (ez egy teljesen zárt cella);
- Nedves elektrolizátor (ez két fémlemez, amelyet vízzel ellátott edénybe helyeznek).
Ez az eszköz a készülék szempontjából egyszerű, ami lehetővé teszi akár otthon is használható... Az elektrolizátorok felosztják a molekulák atomjainak elektrolízis töltéseit töltött atomokra.
Esetünkben a vizet pozitív hidrogénre és negatív oxigénre osztja. Ehhez nagy mennyiségű energia szükséges, és a szükséges energiamennyiség kevesebb előállításához katalizátort használnak.
Elektrolizátor hidrogéntermeléshez
Földelési számítás
Annak érdekében, hogy a legegyszerűbb elektrolizátort saját kezűleg szerelje össze, használhatja az ábrán látható rajzot.


A legegyszerűbb házi elektrolizátor rajza
Jegyzet! Az elektrolizátor meglehetősen veszélyes berendezés, amely működés közben a nagy mennyiségben felhalmozódó oxihidrogéngáz súlyos robbanást okozhat. Az egységet nem szabad nyílt tűzforrások, fűtőberendezések közelében elhelyezni.
Barkács elektrolizátor autóhoz
Az üzemanyag égésének javítása érdekében egy autómotorban gyakran elektrolizátort állítanak össze, amely egy régi akkumulátor testéből áll, benne rozsdamentes acéllemezekkel, két fúvókával, amelyek közül az egyik egy elektrolittal töltött tartályhoz csatlakozik, a második csatlakozik a motor levegőellátó tömlőjéhez (pontosabban a levegő beszívásától a légszűrőig hullámosítva).
Egy ilyen házi készítésű áramló elektrolizát az autó akkumulátorából táplálnak egy relé és egy 10 A-es biztosíték segítségével.
Saját kezűleg készítünk egy eszközt
Az eszköz ehhez a folyamathoz kézzel is elvégezhető.
Ehhez szüksége lesz:
- Rozsdamentes acéllemez;
- Csavarok M6 x 150;
- Alátétek;
- Diófélék;
- Átlátszó cső;
- Csatlakozó elemek mindkét oldalon menettel;
- Másfél literes műanyag edény;
- Vízszűrő;
- Visszacsapó szelep víz.
Kiváló lehetőség a rozsdamentes acél számára az AISI 316L egy külföldi gyártótól vagy a 03X16H15M3 egy országbeli gyártótól. Nincs szükség rozsdamentes acél vásárlására, a régit veheti. 50-50 centiméter elég neked.
- Miért vegye magát a rozsdamentes acélt? - kérdezed. Mivel a leggyakoribb fém korrodálódik. A rozsdamentes acél jobban tolerálja a lúgokat. Kellene vázolja fel a lapot úgy, hogy 16 hasonló négyzetre osztja... Vághatja sarokcsiszolóval. Minden négyzetben vágja le az egyik sarkot.
A másik oldalon és a szemközti sarokban fűrészeljen egy lyukat egy csavarhoz, amely elősegíti a lemezek összetartását. Az elektrolizátor nem áll le így:t lemez áram áramlik a lemezre - és a víz oxigénné és hidrogénné bomlik. Ennek köszönhetően szükségünk van egy jó és negatív lemezre.
A lemezeket felváltva kell csatlakoztatni: plusz-mínusz-plusz-mínusz, hasonló módszerrel erős áram lesz. A lemezek egyenként történő szigeteléséhez csövet használnak. A szintről gyűrűt vágnak le. Vágásával milliméter vastag csíkot kapunk. Ez a távolság a gáz előállításához megfelelőbb.
A lemezek alátétekkel vannak összekötve: alátétet teszünk a csavarra, majd egy lemezt és három alátétet, majd ismét egy lemezt stb. A pluszra és a mínuszra nyolc lemezt kell ültetni. Ha mindent helyesen végeznek, akkor a lemezek vágásai nem érintik az elektródákat.
Ezután meg kell húzni az anyákat és elkülöníteni a lemezeket. Ezután egy műanyag edénybe helyezzük a szerkezetet.
Az elektrolitcellák gyártói áttekintése
Az elektrolizátorok fő gyártói mind a hazai vállalkozások (RUSAL, NPF RutTech, JSC Uralkhimmash), mind külföldi versenytársaik - Teledyne Energy Systems, Inc. (USA), Hydrogenics Corp. (Belgium).
Így az elektrolizátor meglehetősen egyszerű és funkciókban gazdag létesítmény, amelyet oxihidrogéngáz előállítására használnak, és amelyet a jövőben a belső égésű motorok és a fűtőkazánok üzemanyagaként kívánnak felhasználni.
Csináld magad otthoni elektrolízist
Amikor kicsi voltam, mindig magam akartam csinálni valamit, saját kezűleg. De a szülők (és más közeli emberek) a legtöbb esetben ezt nem engedték meg. És akkor nem láttam (és eddig nem látok) semmi rosszat, amikor a kisgyerekek tanulni akarnak ??
Természetesen nem azért írtam ezt a cikket, hogy felidézzem a gyermekkori tapasztalatokat az önképzés megkezdésének vágyában. Csak véletlenül, amikor az interneten böngésztem, találkoztam egy ilyen kérdéssel. Néhány kis bombázó fiú kérdéseket tett fel arról, hogyan lehet otthon elvégezni az elektrolízist. Igaz, nem válaszoltam neki, mert ez a fiú akarta elektrolizálni a fájdalmasan gyanús keveréket ?? Úgy döntöttem, hogy a bűn miatt nem mondok tovább, hadd nézzen én magam a könyvekben. De nem is olyan régen, ismét a fórumokon kóborolva, hasonló kérdést láttam egy vegyésziskola tanárától. A leírás alapján ítélve iskolája olyan szegény, hogy nem tud (nem akar) 300 rubelért elektrolizátort vásárolni. Így segítettem neki. Azok számára, akik kíváncsiak erre a fajta házi készítésű termékre, felteszem ezt a cikket az oldalra.
Tulajdonképpen a gyártási folyamat és az önragadók használata nagyon primitív. De először a biztonságról, a másodikról pedig a gyártásról mesélek. És a lényeg az, hogy bemutató elektrolizáról beszélünk, és nem ipari üzemről. Ennek köszönhetően a biztonság kedvéért jó lesz nem a hálózatról táplálni, hanem AA elemekből vagy akkumulátorból. Természetesen minél nagyobb a feszültség, annál gyorsabban megy végbe az elektrolízis. A gázbuborékok vizuális megfigyeléséhez azonban igen elég 6 V, de a 220 már túlzott. ilyen feszültség mellett például a víz forr a leggyorsabban, és ez nem túl biztonságos ... Nos, azt hiszem, kitalálta a feszültséget?
Most beszéljünk arról, hogy hol és milyen körülmények között fogunk kísérletezni. A legelső dolog vagy szabad hely, vagy jól szellőző helyiség. Bár mindent zárt ablakú lakásban csináltam, és semmi ilyesmi? Másodszor, a kísérletet legjobb egy jó asztalon elvégezni. A "jó" szó azt jelenti, hogy az asztalnak stabilnak, jobbnak kell lennie, merevnek és a padló felületéhez rögzítettnek kell lennie. Ebben az esetben az asztallapnak ellenállónak kell lennie agresszív anyagokkal szemben. Egyébként erre egy csempe egy cserépről tökéletes (bár sajnos nem minden). Egy ilyen asztal nemcsak ehhez az élményhez fog jól jönni. Viszont mindent egy közönséges széken tettem ?? Harmadszor, a kísérlet során nem kell mozgatnia az áramforrást (esetemben az elemeket). Emiatt a megbízhatóság érdekében a legjobb, ha azonnal leteszi őket az asztalra és rögzíti, hogy ne mozduljanak. Hidd el, ez sokkal kényelmesebb, mint rendszeresen a kezeddel tartani őket. A saját akkumulátorokat egyszerűen elektromos szalaggal kötöttem az első kemény tárgyhoz, amelyet láttam. Negyedszer, azok az ételek, amelyekben kísérletezni fogunk, legyenek kicsik. Egyszerű pohár illik, vagy egy üveg. Egyébként ez a szemüveg otthoni használatának legoptimálisabb módja, szemben azzal, hogy további felhasználással alkoholt öntünk beléjük ...
Nos, most térjünk át konkrétan az eszközre. Az ábrán szerepel, de egyelőre röviden elmagyarázom, hogy mit és mit.
Vegyünk egy egyszerű ceruzát, és egy közönséges késsel vegyük le róla a fát, és egy egész ólmot kell kihoznunk a ceruzából. Vezethet azonban egy mechanikus ceruzából. De egyszerre két nehézség van. Az első a szokásos. A mechanikus ceruza ólma túl vékony, csak vizuális kísérlethez nem felel meg nekünk. A második nehézség a jelenlegi palák valamilyen érthetetlen összetétele. Olyan érzés, mintha nem grafitból készülnének, hanem valami másból. Általánosságban elmondható, hogy az ilyen "vezetéssel" kapcsolatos tapasztalataim egyáltalán nem voltak sikeresek, még 24 V-os feszültség mellett sem. Ennek köszönhetően ki kellett válogatnom egy jó fás, egyszerű ceruzát. A kapott grafitrúd elektródként szolgál számunkra. Ahogy el lehet képzelni, két elektródára van szükségünk. Ennek köszönhetően elmegyünk a második ceruzát választani, vagy egyszerűen kettétörjük a meglévő rudat. Valójában ezt tettem.
Bármely kéznél lévő vezetékkel beburkoljuk az első ólomelektródát (a vezeték egyik végével), és ezt a vezetéket összekapcsoljuk az áramforrás mínuszával (a másik végével). Ezután átvesszük a második vezetést, és ugyanezt tesszük vele. Ehhez ennek alapján szükségünk van egy második vezetékre. De ebben az esetben ezt a vezetéket az áramellátás pluszához kötjük. Ha problémái vannak a törékeny grafitrúdnak a huzalra való rögzítésével, használhatja a kéznél lévő eszközöket, például szalagot vagy ragasztószalagot. Ha nem jött össze, hogy a grafit hegyét magával a huzallal tekerje be, és a szalag vagy a szigetelőszalag nem adott szoros kapcsolatot, akkor próbálja meg az ólmot vezető ragasztóval ragasztani. Ha ez nincs meg, akkor legalább kösse össze a vezetéket a huzallal egy fonallal. Nem kell félni, a fonal nem fog kiégni egy ilyen feszültségtől ??
Azok számára, akik nem tudnak semmit az akkumulátorokról és azok csatlakoztatásának egyszerű szabályairól, elmagyarázok egy kicsit. Az ujj típusú akkumulátor 1,5 V feszültséget produkál. A képen két hasonló elemem van. Sőt, összekapcsolódnak fokozatosan - egymás után, nem párhuzamosan. Ilyen (soros) csatlakozás esetén az egyes akkumulátorok feszültségéből összegzik a végső feszültséget, vagyis számomra 1,5 + 1,5 = 3,0 V. Ez kevesebb, mint a korábban deklarált 6 volt. De lusta voltam még néhány elemet venni. Alapelv te és így egyértelműnek kell lennie ??
Kezdjük a kísérletet. Például korlátozzuk magunkat a víz elektrolízisére.Először is nagyon hozzáférhető (remélem, hogy a cikk olvasója nem a Szaharában él), másrészt ártalmatlan. Sőt, megmutatom, hogy ugyanazzal az eszközzel (elektrolizátorral) ugyanazzal az anyaggal (vízzel) hogyan lehet kettőt végrehajtani különféle tapasztalat. Azt hiszem, van elég fantáziád ahhoz, hogy egy csomó hasonló kísérletet előállíts más anyagokkal ?? Általában a csapvíz alkalmas számunkra. De azt javaslom, hogy adjon hozzá még egy keveset és sózza meg. Kicsit - ez egy kis csipet, nem pedig egy egész desszertkanál. Ez fontos! Alaposan keverje meg a sót, hogy feloldódjon. Tehát a víz tiszta állapotban dielektrikumként tökéletesen vezeti az áramot. a kísérlet elején törölje le az asztalt a lehetséges nedvességtől, majd tegye rá az áramforrást és egy pohár vizet.
Mindkét feszültség alatt álló elektródát leeresztjük a vízbe. Ugyanakkor ügyeljen arra, hogy csak grafit legyen a vízben, és maga a vezeték ne érjen a vízhez. A kísérlet kezdete késhet. Az idő sok tényezőtől függ: a víz összetételétől, a vezetékek minőségétől, a grafit minőségétől és természetesen az áramforrás feszültségétől. A reakcióm kezdete pár másodpercig elmaradt. Az oxigén kezd fejlődni azon az elektródon, amelyet az elemek pluszához csatlakoztattak. A mínuszhoz kapcsolt elektródon hidrogén szabadul fel. Meg kell jegyezni, hogy több a hidrogénbuborék. Nagyon kis buborékok tapadnak a grafitnak a vízbe merült része körül. Aztán a buborékok egy része úszni kezd.
Elektróda a kísérlet elején. Még nincsenek buborékbuborékok. Az elemek negatív pólusához kapcsolt elektródán hidrogénbuborékok képződtek
Milyen további kísérletek lehetnek? Ha már eleget játszottál hidrogénnel és oxigénnel, folytatunk egy újabb kísérletet. Érdekesebb, főleg az otthoni kutatók számára. Érdekessége, hogy nemcsak látni, hanem szagolni is lehet. A korábbi tapasztalatok szerint oxigént és hidrogént kaptunk, amelyek véleményem szerint nem túl látványosak. Egy másik kísérletben pedig két anyagot kapunk (egyébként hasznos a mindennapi életben). a kísérlet elején állítsa le az előző kísérletet és szárítsa meg az elektródákat. Most vegyen asztali sót (amelyet a legtöbb esetben a konyhában használ), és oldja fel a víztömegben. Ebben az esetben nem kevés. Valójában a tisztességes mennyiségű só az egyetlen, ami a második élményt különbözteti meg az elsőtől. A só feloldása után azonnal megismételheti a kísérletet. Most más a reakció. Egy jó elektródán most nem oxigén szabadul fel, hanem klór. Negatívumként a hidrogén is felszabadul. Ami azt az üveget illeti, amelyben a sóoldat található, hosszan tartó elektrolízis után nátrium-hidroxid marad benne. Ez az ismert maró nátrium, lúg.
Klór, érezni fogja a szagát. De a legjobb hatás érdekében ajánlom legalább 12 V feszültség felvételét. Ellenkező esetben előfordulhat, hogy nem érzi az aromát. A lúg jelenléte (nagyon hosszú elektrolízis után) az üvegben többféle módon ellenőrizhető. A legegyszerűbb és legerőszakosabb az, ha a pohárba teszed a kezed. Egy etnikai ómen azt mondja, hogy ha égő érzés kezdődik, lúg van a pohárban. Az okosabb és egyértelműbb módszer a lakmusz teszt. Ha iskolája olyan gyenge, hogy még lakmuszot sem képes megszerezni, akkor hasznos mutatók segítenek Önnek. Ezek egyike - mint mondják - csepp répaléként szolgálhat ?? De nagyon is lehetséges, hogy csak egy kis zsírt csepegtet az oldatba. Ha jól tudom, a szappanosításnak meg kell történnie.
A nagyon kíváncsiak számára leírom, hogy mi is történt valójában a kísérletek során. Az első kísérletben elektromos áram hatására hasonló reakció zajlott le: 2 H2O >>> 2 H2 + O2 Mindkét gáz természetesen a víz felől a felszínre úszik. Egyébként lebegő gázok csapdába eshetnek. Képes leszel megtenni magad?
Egy másik kísérletben a reakció teljesen más volt.Elektromos áram is elindította, de most már nemcsak a víz, hanem a só is reagensként működött: 4H2O + 4NaCl >>> 4NaOH + 2H2 + 2Cl2 Ne feledje, hogy a reakciónak vízfeleslegben kell végbemennie. Hogy megtudja, mekkora sómennyiséget tekintenek a legnagyobbnak, megszámolhatja a fenti reakcióból. Gondolhat arra is, hogyan lehetne továbbfejleszteni az eszközt, vagy milyen további kísérleteket lehet elvégezni. Valójában lehetséges, hogy a nátrium-hipoklorit elektrolízissel nyerhető. Laboratóriumi körülmények között a legtöbb esetben gáznemű klór nátrium-hidroxid-oldaton keresztül történő leadásával nyerik.