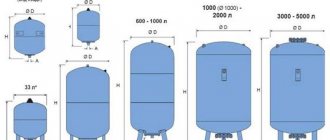
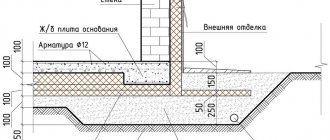
Ang isa sa maraming mga proseso ng physicochemical na natagpuan ang malawak na aplikasyon, kapwa sa industriya at sa pang-araw-araw na buhay, ay electrolysis - ang pagpili sa mga ibabaw ng mga electrode na konektado sa isang kasalukuyang mapagkukunan na inilagay sa isang solusyon o natunaw, ang kanilang mga bahagi (purong metal - aluminyo, tanso, gas, atbp.). Ang pangunahing pag-install sa loob kung saan nagaganap ang prosesong ito ay isang electrolyzer.

Electrolyzer
Ano ang isang electrolyser
Ang electrolyzer ay isang espesyal na pag-install na ginagamit upang paghiwalayin ang mga nasasakupan nito mula sa isang solusyon o matunaw.
Ang mga pangunahing katangian ng electrolyser ay:
- Ang boltahe ng operating para sa isang elektrod ay umaabot mula 1.8 hanggang 2.0 V;
- Kasalukuyang lakas - para sa normal na kurso ng proseso ng electrolysis, isang kasalukuyang ibinibigay sa mga electrode na may halaga ng katangiang ito mula 5 hanggang 10 A;
- Bilang ng mga electrode - ang minimum na bilang ng mga electrode ay 2, ang maximum ay limitado ng laki ng pag-install mismo at ang layunin nito;
- Mga sukat ng mga electrode - hindi carbon rods ang ginagamit bilang mga electrode, ngunit ang mga plate ng metal, ang laki nito ay natutukoy ng layunin ng pag-install, ang kasalukuyang boltahe na katangian ng kasalukuyang ibinibigay sa mga plato;
- Distansya sa pagitan ng salungat na sisingilin sa mga ibabaw ng elektrod - ang minimum na distansya sa pagitan ng mga plate ng elektrod ay dapat na hindi bababa sa 1.5 mm;
- Materyal ng elektrod - sa mga modernong electrolyzer, ang stainless steel sheet na may nickel ay ginagamit bilang materyal para sa anode at cathode.
Gayundin ang isa pang mahalagang katangian ng isang halaman ng electrolysis ay ang paggamit ng mga catalista.
Ang mga nasabing pag-install ay ginagamit para sa mga sumusunod na layunin:
- Pagkuha ng isang oxyhydrogen gas, na binubuo ng isang halo ng hydrogen at oxygen (Brown's gas);
- Paghiwalay ng purong aluminyo, magnesiyo, sink mula sa kanilang natunaw na asin;
- Ang paglilinis ng tubig mula sa mga asing-gamot at mga impurities na natunaw dito;
- Paglalapat ng isang manipis na layer ng nikel, sink na pumipigil sa kaagnasan sa ibabaw ng mga bahagi ng metal;
- Pagdidisimpekta ng mga produktong pagkain;
- Ang paglilinis ng basurang tubig mula sa mga natunaw na asing-gamot ng mabibigat na riles at iba pang nakakapinsalang sangkap.
Mahalaga! Ang platinum-electrode na gawa sa ordinaryong iron ay ginagamit nang mas madalas sa mga halaman ng electrolysis kaysa sa mula sa hindi kinakalawang na asero, dahil mas mabilis itong mag-oxidize at hindi magamit.
Gumawa ng sariling electrolyzer
Kahit sino ay maaaring gumawa ng isang electrolyzer gamit ang kanilang sariling mga kamay. Para sa proseso ng pagpupulong ng pinaka-karaniwang disenyo, kakailanganin ang mga sumusunod na materyales:
- hindi kinakalawang na asero sheet (ang pinakamahusay na mga pagpipilian ay dayuhan AISI 316L o amin 03X16H15M3);
- bolts М6х150;
- mga washer at mani;
- transparent tube - maaari kang gumamit ng antas ng espiritu, na ginagamit para sa mga hangarin sa pagtatayo;
- maraming mga herringbone fittings na may isang panlabas na diameter ng 8 mm;
- lalagyan ng plastik na may dami na 1.5 liters;
- isang maliit na pansala ng pag-filter ng tubig sa gripo, halimbawa, isang filter para sa mga washing machine;
- di-bumalik na balbula ng tubig.
Proseso ng Assembly
Kolektahin ang electrolyzer gamit ang iyong sariling mga kamay alinsunod sa mga sumusunod na tagubilin:
- Una sa lahat, kailangan mong markahan at ang kasunod na paglalagari ng sheet na hindi kinakalawang na asero sa magkaparehong mga parisukat. Ang paglalagari ay maaaring gawin sa isang gilingan ng anggulo (anggiling gilingan). Ang isa sa mga sulok sa gayong mga parisukat ay dapat na gupitin sa isang anggulo para sa tamang pag-aayos ng mga plato;
- Susunod, kailangan mong gumawa ng isang butas para sa bolt sa gilid ng plato sa tapat mula sa sulok ng lagari na gupitin;
- Ang koneksyon ng mga plato ay dapat gawin sa pagliko: isang plato sa "+", ang susunod sa "-" at iba pa;
- Sa pagitan ng magkakaibang singil na mga plato dapat mayroong isang insulator, na gumaganap bilang isang tubo mula sa antas ng espiritu.Dapat itong i-cut sa mga singsing, na dapat i-cut pahaba upang makakuha ng mga piraso ng 1 mm kapal. Ang distansya sa pagitan ng mga plato ay sapat para sa mahusay na evolution ng gas sa panahon ng electrolysis;
- Ang mga plato ay nakakabit nang magkasama gamit ang mga washer tulad ng sumusunod: ang isang washer ay nakaupo sa bolt, pagkatapos ay isang plato, pagkatapos ay tatlong mga washer, pagkatapos ng isang plato, at iba pa. Ang mga plato, pinapaboran na sisingilin, ay inilalagay sa isang mirror na imahe ng mga negatibong sisingilin na sheet. Ginagawang posible upang mapigilan ang mga gilid na gabas na hawakan ang mga electrode;


Ang mga plate ng planta ng electrolysis ay nagtipon-tipon
- Kapag pinagsama ang mga plato, dapat mong sabay na ihiwalay ang mga ito at higpitan ang mga mani;
- Gayundin, ang bawat plato ay dapat na ring upang matiyak na walang maikling circuit;
- Dagdag dito, ang buong pagpupulong ay dapat ilagay sa isang plastik na kahon;
- Pagkatapos nito, sulit na i-highlight ang mga lugar kung saan hinahawakan ng mga bolt ang mga dingding ng lalagyan, kung saan ka drill ng dalawang butas. Kung ang mga bolt ay hindi umaangkop sa lalagyan, pagkatapos ay kailangan nilang i-cut sa isang hacksaw;
- Pagkatapos ang mga bolt ay hinihigpit ng mga mani at washer para sa higpit ng istraktura;


Mga plato na inilagay sa isang lalagyan ng plastik
- Matapos ang mga hakbang na ginawa, kakailanganin mong gumawa ng mga butas sa takip ng lalagyan at ipasok ang mga fittings sa kanila. Ang impermeability sa kasong ito ay maaaring matiyak sa pamamagitan ng pag-sealing ng mga kasukasuan na may mga silanteng nakabatay sa silikon;
- Ang isang balbula ng kaligtasan at filter sa istraktura ay matatagpuan sa outlet ng gas at nagsisilbing isang paraan ng pagkontrol sa labis na akumulasyon ng gas, na maaaring humantong sa hindi magandang resulta;
- Ang yunit ng electrolysis ay binuo.
Ang huling yugto ay isang pagsubok, na ginaganap sa katulad na paraan:
- pagpuno ng lalagyan ng tubig hanggang sa marka ng mga bolts para sa mga fastener;
- pagkonekta ng lakas sa aparato;
- koneksyon sa pag-angkop ng tubo, ang kabaligtaran na dulo nito ay ibinaba sa tubig.
Kung ang isang mahina na kasalukuyang ay inilalapat sa pag-install, pagkatapos ang paglabas ng gas sa pamamagitan ng tubo ay halos hindi mahahalata, ngunit posible na panoorin ito mula sa loob ng electrolyzer. Sa pamamagitan ng pagdaragdag ng kasalukuyang alternating, pagdaragdag ng isang alkaline catalyst sa tubig, posible na makabuluhang taasan ang ani ng puno ng gas na sangkap.
Ang ginawang electrolyzer, bilang panuntunan, ay isang mahalagang bahagi ng maraming mga aparato, halimbawa, isang hydrogen burner.


ang hitsura ng isang hydrogen burner, ang batayan nito ay itinuturing na isang self-made electrolyzer
Alam ang mga uri, pangunahing katangian, aparato at prinsipyo ng pagtatrabaho ng mga ionic na pag-install, maaari mong maisagawa ang tamang pagpupulong ng isang istrakturang ginawa ng bahay, na kung saan ay isang mahusay na katulong sa iba't ibang mga pang-araw-araw na sitwasyon: mula sa hinang at pag-save ng pagkonsumo ng gasolina ng mga sasakyan sa motor ang paggana ng mga sistema ng pag-init.
Device at prinsipyo ng pagpapatakbo
Cathode at anode
Ang pinakasimpleng halaman ng electrolysis ay binubuo ng maraming mga "cell", na ang bawat isa ay may kasamang:
- 2 plate electrodes - cathode (negatibo) at anode (positibo);
- Ang isang gasket na goma sa paligid ng perimeter ng dalawang katabing hindi magkatulad na mga electrode.
Ang panlabas na mga cell ay nilagyan ng mga espesyal na tubo kung saan ang mga nagbabagong gas ay pinalabas.
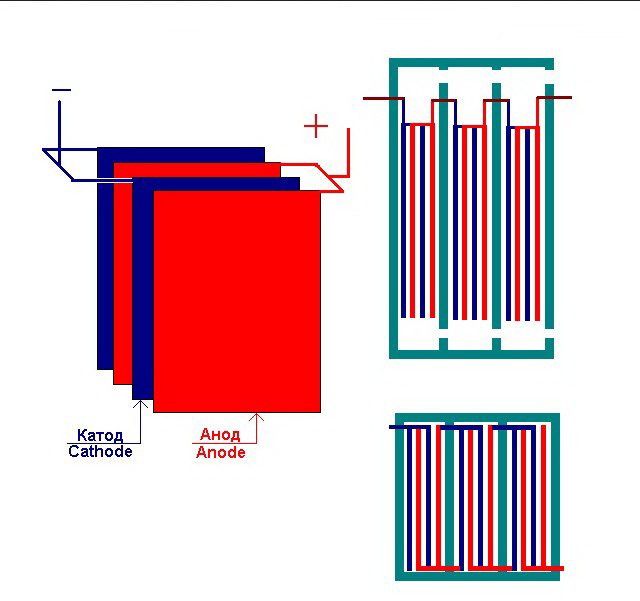

Maraming magkakaugnay na "cells" ng electrolysis plant
Ang electrolyzer ay maaaring maglaman mula 1 hanggang 30-40 o higit pa tulad ng "mga cell", ang mga plato ng parehong pangalan ay konektado sa serye.
Mahalaga! Kapag gumagamit ng mga supply ng kuryente na may alternating kasalukuyang, ang mga rectifier ay karagdagan na ginagamit, ang pinakasimpleto ay isang diode bridge.
Ang ganitong pag-install ay gumagana tulad ng sumusunod:
- Ang distiladong tubig na may alkali na natunaw dito o ordinaryong baking soda ay ibinuhos sa puwang sa pagitan ng mga electrode;
- Ang boltahe na 1.8-2.0 V ay ibinibigay mula sa power supply sa mga electrodes ng lahat ng mga cell ng pag-install;
- Bilang isang resulta ng proseso ng electrolysis, ang mga anion (positibong nasingil na mga ions) ng isang sangkap na natunaw sa tubig ay naaakit sa negatibong sisingilin na katod, bilang isang resulta kung saan nabuo ang isang manipis na sosa na pelikula dito;
- Sa isang positibong sisingilin na anod, nangyayari ang pagkasira ng mga molekula ng tubig, na may bawat nabuo na 2 atom ng hydrogen at 1 oxygen atom;
- Ang pinakawalan na nagpaputok na gas sa pamamagitan ng mga tubo ng sangay ay pumapasok sa lalagyan na inilaan para dito.
Ang tindi ng proseso ng electrolysis ay nakasalalay sa boltahe at kasalukuyang lakas - sa mababang halaga ng mga katangiang ito, hindi magpapatuloy ang proseso. Kung ang pinagmulan ng kuryente ay nagbibigay ng isang kasalukuyang may masyadong mataas na halaga ng kasalukuyang boltahe na katangian, ang solusyon na ibinuhos sa electrolyzer ay magiging napakainit at pakuluan.
Pag-debug at pagsubok ng aparato
Pagkatapos ito ay kinakailangan upang matukoy kung saan ang mga bolts ay hawakan ang mga dingding ng kahon at, sa mga lugar na iyon, mag-drill ng dalawang butas. Kung sa walang maliwanag na dahilan ito ay lumalabas na ang mga bolt ay hindi umaangkop sa lalagyan, kung gayon dapat gupitin at higpitan para sa higpit ng mga mani... Ngayon ay kailangan mong i-drill ang takip at ipasok ang mga sinulid na konektor doon mula sa magkabilang panig. Upang matiyak ang kawalang-tatag, ang magkasanib ay dapat na selyohan ng isang silicone-based sealant.
Matapos tipunin ang iyong sariling electrolyzer gamit ang iyong sariling mga kamay, dapat mo itong subukan. Upang magawa ito, ikonekta ang aparato sa isang mapagkukunan ng kuryente, punan ito ng tubig sa mga bolt, ilagay sa talukap ng mata sa pamamagitan ng pagkonekta ng isang tubo sa angkop at pagbaba ng kabaligtaran na dulo ng tubo sa tubig. Kung mahina ang kasalukuyang, ang kasalukuyang ay makikita mula sa loob ng electrolyzer.
Unti-unting taasan ang kasalukuyang sa iyong homemade appliance. Ang distiladong tubig ay hindi mahusay na nagsasagawa ng kuryente sapagkat wala itong mga asing-gamot o impurities. Upang maihanda ang electrolyte, kinakailangan upang magdagdag ng alkali sa tubig. Upang magawa ito, kailangan mong kumuha ng sodium hydroxide (nakapaloob sa mga paraan para sa paglilinis ng mga tubo tulad ng "Mole"). Kailangan ng isang balbula sa kaligtasan upang maiwasan ang pag-iipon ng disenteng halaga ng gas.
- Mas mahusay na gamitin ang dalisay na tubig at soda bilang isang katalista.
- Dapat mong ihalo ang ilan sa baking soda na may apatnapung bahagi ng tubig. Ang mga pader sa gilid ay pinakamahusay na gawa sa acrylic na baso.
- Ang mga electrode ay pinakamahusay na gawa sa hindi kinakalawang na asero. Makatuwirang gumamit ng ginto para sa mga plato.
- Gumamit ng translucent PVC para sa pag-back. Maaari silang 200 sa pamamagitan ng 160 millimeter na laki.
- Maaari mong gamitin ang iyong sariling electrolyzer, na ginawa ng iyong sarili, upang magluto ng pagkain, para sa kumpletong pagkasunog ng gasolina sa mga kotse at sa karamihan ng mga kaso.
Pangunahing ginagamit ang mga dry electrolyzer para sa mga makina. Pinapataas ng generator ang lakas ng engine ng pagkasunog. Ang hydrogen ay nag-apoy nang mas mabilis kaysa sa likidong gasolina, na nagdaragdag ng lakas ng piston. Bilang karagdagan sa Mole, maaari kang kumuha ng Mister Muscle, caustic soda, baking soda.
Ang generator ay hindi gumagana sa inuming tubig. Mas mahusay na ikonekta ang kuryente tulad nito: ang una at ang huling plato - minus, at sa plato sa gitna - plus. Kung mas malaki ang lugar ng mga plato at mas malakas ang kasalukuyang, mas maraming gas ang pinakawalan.
Mga uri ng electrolyzer
DIY spot welding para sa mga baterya
Nakasalalay sa disenyo at prinsipyo ng pagpapatakbo, mayroong 5 uri ng mga halaman ng electrolysis.
Matuyo
Ang mga nasabing electrolyzer ay binubuo ng mga plate electrodes na pinaghihiwalay ng mga selyadong gasket na goma. Kadalasan, ang "mga cell" ng pag-install ay karagdagan na inilalagay sa isang selyadong enclosure.
Ang hydrogen at oxygen na nabuo bilang isang resulta ng electrolysis ay inalis sa pamamagitan ng mga espesyal na tubo ng sangay na matatagpuan sa dulo ng katawan o ang matinding mga plato ng pag-install.
Dumadaloy
Ang mga pag-install ng electrolysis ng ganitong uri ay may mga sumusunod na aparato:
- Ang isang electrolysis bath (katawan) na may dalawang mga nozzles, sa pamamagitan ng isa sa mga ito ang electrolyte ay pinakain dito, sa pamamagitan ng pangalawa ang detonating gas na nabuo bilang isang resulta ng electrolysis ay natanggal;
- Ang mga electrodes ng plate ay pinaghihiwalay ng mga spacer;
- Ang isang tangke na may electrolyte na matatagpuan sa itaas ng pabahay na may mga electrode at konektado sa pamamagitan ng mga hose sa mga tubo ng sangay ng electrolysis bath ng pag-install at pagkakaroon ng isang tubo ng sangay na may isang balbula ng gas sa itaas na bahagi.
Sa panahon ng pagpapatakbo ng naturang aparato, ang umunlad na gas sa pamamagitan ng tubo ng sangay at ang hose ay pumapasok sa tangke gamit ang electrolyte at, lumilikha ng isang tiyak na presyon dito, iniiwan ang pag-install sa pamamagitan ng balbula sa tubo ng sangay.
Lamad
Ang mga cell ng electrolysis ng naturang mga pag-install ay binubuo ng dalawang electrode na pinaghihiwalay ng isang manipis na lamad na nagpapahintulot sa mga produktong electrolysis na dumaan at ihiwalay ang mga electrode sa bawat isa.
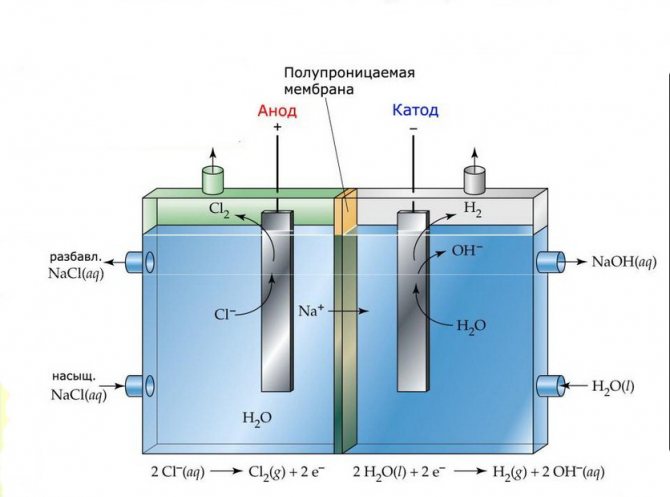

Halaman ng lamad ng electrolysis
Diaphragm
Ang mga pag-install ng electrolysis ng ganitong uri ay binubuo ng isang "U" na hugis na prasko na may dalawang electrode na nakapasok dito at 2-3 hindi mahahalata na mga diaphragms. Ang mga katulad na electrolyzer ay ginagamit para sa magkahiwalay na produksyon ng purong hydrogen at oxygen.
Alkalina
Hindi tulad ng iba pang mga modelo ng electrolyzers, sa mga ito, ang isang solusyon sa alkali ay ginagamit bilang isang electrolyte - caustic soda (sodium hydroxide), na kung saan ay hindi lamang isang karagdagang mapagkukunan ng hydrogen at oxygen, kundi pati na rin isang sanhi ng electrolysis.


Alkaline electrolyser circuit
Ang mga nasabing pag-install, taliwas sa mga analogue ng iba pang mga uri, pinapayagan ang paggamit ng mas murang mga electrode na gawa sa ordinaryong bakal.
Gawin ang electrolyser gamit ang iyong sariling mga kamay
Tiyak, pamilyar ka sa proseso ng electrolysis mula sa kurikulum sa elementarya. Ito ay kapag ang 2 polar electrodes ay inilalagay sa tubig sa ilalim ng kasalukuyang upang makakuha ng mga metal o di-metal sa kanilang dalisay na anyo. Kailangan ng electrolyzer upang mabulok ang mga molekula ng tubig sa oxygen at hydrogen. Ang electrolyzer, bilang bahagi ng mga mekanismong pang-agham, ay hinahati ang mga molekula sa mga ions.
Mayroong dalawang uri ng aparatong ito:
- Dry electrolyzer (ito ay isang ganap na sarado na cell);
- Basang electrolyzer (ito ang dalawang metal plate na nakalagay sa isang lalagyan ng tubig).
Ang aparato na ito ay simple sa mga tuntunin ng aparato, na ginagawang posible gamitin kahit sa bahay... Hinahati ng mga electrolyzer ang mga singil ng electrolysis ng mga atomo ng mga molekula sa mga singil na atomo.
Sa aming kaso, hinahati nito ang tubig sa positibong hydrogen at negatibong oxygen. Upang magawa ito, isang malaking halaga ng enerhiya ang kinakailangan, at upang mas mababa ang kinakailangang dami ng enerhiya, ginamit ang isang katalista.
Electrolyzer para sa paggawa ng hydrogen
Pagkalkula ng ground
Upang mapagsama ang pinakasimpleng electrolyzer gamit ang iyong sariling mga kamay, maaari mong gamitin ang guhit na ipinakita sa pigura.


Pagguhit ng pinakasimpleng gawang bahay na electrolyzer
Tandaan! Ang isang electrolyzer ay isang mapanganib na pag-install, kung saan, sa panahon ng operasyon, oxyhydrogen gas, na naipon ng maraming dami, ay maaaring maging sanhi ng isang seryosong pagsabog. Ang yunit ay hindi dapat mailagay malapit sa mga mapagkukunan ng bukas na apoy, mga aparatong pampainit.
DIY electrolyser para sa isang kotse
Upang mapabuti ang pagkasunog ng gasolina sa isang makina ng kotse, ang isang electrolyzer ay madalas na tipunin, na binubuo ng isang katawan mula sa isang lumang baterya na may mga plate na hindi kinakalawang na asero na inilagay sa loob, dalawang mga nozel, na ang isa ay konektado sa isang tangke na puno ng electrolyte, ang pangalawa ay konektado sa isang air na nagbibigay ng hose sa makina (mas tiyak, na may isang corrugated mula sa pag-inom ng hangin sa filter ng hangin).
Ang nasabing isang lutong bahay na dumadaloy na electrolyzer ay pinalakas mula sa baterya ng kotse gamit ang isang relay at isang 10 A fuse.
Lumilikha kami ng isang aparato gamit ang aming sariling mga kamay
Ang aparato para sa prosesong ito ay maaaring gawin sa pamamagitan ng kamay.
Para dito kakailanganin mo:
- Hindi kinakalawang na asero sheet;
- Bolts M6 x 150;
- Mga washer;
- Mga mani;
- Transparent tube;
- Pagkonekta ng mga elemento na may thread sa magkabilang panig;
- Isa't kalahating litro na lalagyan ng plastik;
- Pansala ng tubig;
- Suriin ang balbula para sa tubig.
Ang isang mahusay na pagpipilian para sa hindi kinakalawang na asero ay ang AISI 316L ng isang banyagang tagagawa o 03X16H15M3 ng isang tagagawa mula sa ating bansa. Mayroong ganap na hindi na kailangang bumili ng hindi kinakalawang na asero, maaari mong kunin ang luma. 50 hanggang 50 sentimo ay sapat na para sa iyo.
"Bakit kumuha mismo ng hindi kinakalawang na asero?" - tinatanong mo. Dahil ang pinaka-karaniwang metal ay magwawalis. Mas tinitiis ng hindi kinakalawang na asero ang mga alkalis. Dapat balangkas ang sheet sa isang paraan upang hatiin ito sa 16 na magkatulad na mga parisukat... Maaari mo itong i-cut gamit ang isang gilingan ng anggulo. Sa bawat parisukat, gupitin ang isa sa mga sulok.
Sa kabilang panig at kabaligtaran na sulok, mula sa nawn-off na sulok, mag-drill ng isang butas para sa isang bolt na makakatulong na magkasama ang mga plato. Ang electrolyzer ay hindi titigil sa pagtatrabaho tulad nito:t plate kuryente dumadaloy sa plato - at ang tubig ay nabubulok sa oxygen at hydrogen. Salamat sa ito, kailangan namin ng isang mahusay at negatibong plate.
Ang mga plato ay dapat na magkonekta nang halili: plus-minus-plus-minus, na may katulad na pamamaraan, magkakaroon ng isang malakas na kasalukuyang. Upang insulate ang mga plate isa mula sa isa, isang tubo ang ginagamit. Ang isang singsing ay pinutol mula sa antas. Sa pamamagitan ng pagputol nito, nakakakuha tayo ng isang strip millimeter na makapal. Ang distansya na ito ay mas tama para sa paggawa ng gas.
Ang mga plato ay magkakaugnay sa mga washer: inilalagay namin ang isang washer sa bolt, pagkatapos ay isang plato at tatlong mga washer, pagkatapos ay isang plato muli, at iba pa. Sa plus at minus, walong plato ang dapat itanim. Kung ang lahat ay tapos na nang tama, kung gayon ang mga pagbawas ng mga plato ay hindi hawakan ang mga electrode.
Pagkatapos ay kailangan mong higpitan ang mga mani at ihiwalay ang mga plato. Pagkatapos ay inilalagay namin ang istraktura sa isang lalagyan ng plastik.
Pangkalahatang-ideya ng mga tagagawa ng electrolyzer
Ang pangunahing mga gumagawa ng electrolysers ay kapwa mga domestic enterprise (RUSAL, NPF RutTech, JSC Uralkhimmash), pati na rin ang kanilang mga kakumpitensyang dayuhan - Teledyne Energy Systems, Inc (USA), Hydrogenics Corp. (Belgium).
Kaya, ang electrolyzer ay isang medyo simple at mayaman sa pag-install na ginamit upang makabuo ng oxyhydrogen gas, na sa hinaharap ay pinlano na magamit bilang gasolina para sa panloob na mga engine ng pagkasunog at mga boiler ng pag-init.
Do-it-yourself electrolysis sa bahay
Noong maliit ako, palagi kong nais na gumawa ng isang bagay sa aking sarili, gamit ang aking sariling mga kamay. Ngunit ang mga magulang (at iba pang malapit na tao) sa karamihan ng mga kaso ay hindi pinapayagan ito. At hindi ko nakita noon (at hanggang ngayon hindi ko nakikita) anumang masama kapag nais malaman ng maliliit na bata ??
Siyempre, hindi ko isinulat ang artikulong ito upang maalala ang mga karanasan sa pagkabata sa pagnanais na magsimula ng sariling edukasyon. Sa hindi sinasadya lamang, nang mag-surf ako sa Internet, napag-alaman ko ang isang uri ng ganitong uri. Ang ilang maliit na bomber boy ay nagtanong tungkol sa kung paano gumawa ng electrolysis sa bahay. Totoo, hindi ko siya sinagot, dahil ang batang ito ay nais na electrolyze ang masakit na kahina-hinalang pinaghihinalaan ?? Napagpasyahan kong hindi ko na sasabihin nang higit pa sa kasalanan, hayaan mo akong tumingin sa mga libro mismo. Ngunit hindi pa matagal, ang muling pagala sa mga forum, nakita ko ang isang katulad na tanong mula sa isang guro sa isang paaralan sa chemistry. Sa paghusga sa paglalarawan, ang kanyang paaralan ay mahirap kaya't hindi ito (hindi nais) bumili ng electrolyzer para sa 300 rubles. Ang guro (anong problema!) Hindi makahanap ng isang paraan palabas sa nagresultang sitwasyon. Kaya tinulungan ko siya. Para sa mga nag-uusisa tungkol sa ganitong uri ng mga produktong lutong bahay, nai-post ko ang artikulong ito sa site.
Sa totoo lang, ang proseso ng produksyon at ang paggamit ng aming self-pallet ay napakauna. Ngunit sasabihin ko sa iyo ang tungkol sa kaligtasan muna, at tungkol sa pagmamanupaktura - sa pangalawa. At ang punto ay pinag-uusapan natin ang tungkol sa isang demonstration electrolyzer, at hindi tungkol sa isang pang-industriya na halaman. Salamat dito, para sa kaligtasan, mainam na mapalakas ito hindi mula sa network, ngunit mula sa mga baterya ng AA o mula sa isang baterya. Naturally, mas mataas ang boltahe, mas mabilis ang proseso ng electrolysis. Gayunpaman, para sa visual na pagmamasid ng mga bula ng gas, medyo ito sapat na 6 V, ngunit ang 220 ay sobra na. na may tulad na boltahe, ang tubig, halimbawa, ay magpapakulo ng pinakamabilis, at hindi ito gaanong ligtas ... Buweno, sa palagay ko nalaman mo ang pag-igting?
Ngayon pag-usapan natin kung saan at sa ilalim ng kung anong mga kundisyon ang mag-e-eksperimento kami. Ang pinakaunang bagay, dapat itong alinman sa libreng puwang o isang maayos na maaliwalas na silid. Kahit na ginawa ko ang lahat sa isang apartment na may saradong bintana at walang katulad? Pangalawa, ang eksperimento ay pinakamahusay na ginagawa sa isang magandang mesa. Ang salitang "mabuti" ay nangangahulugang ang mesa ay dapat na matatag, at mas mabigat, matigas at nakakabit sa ibabaw ng sahig. Sa kasong ito, ang takip ng talahanayan ay dapat na lumalaban sa agresibong mga sangkap. Sa pamamagitan ng paraan, ang tile mula sa isang tile ay perpekto para sa mga ito (kahit na hindi bawat, sa kasamaang palad). Ang isang talahanayan na tulad nito ay darating sa madaling gamiting hindi lamang para sa karanasang ito. Gayunpaman, ginawa ko ang lahat sa isang ordinaryong dumi ng tao ?? Pangatlo, sa panahon ng eksperimento, hindi mo kailangang ilipat ang pinagmulan ng kuryente (sa aking kaso, mga baterya). Dahil dito, para sa pagiging maaasahan, pinakamahusay na agad na itabi ang mga ito sa mesa at ayusin ang mga ito upang hindi sila makilos. Maniwala ka sa akin, mas maginhawa ito kaysa sa regular na paghawak sa kanila ng iyong mga kamay. Pasimple kong itinali ang aking sariling mga baterya gamit ang electrical tape sa unang matigas na bagay na nakita ko. Pang-apat, ang mga pinggan kung saan kami mag-e-eksperimento, hayaan silang maging maliit. Isang simpleng baso na sukat o isang shot glass. Sa pamamagitan ng paraan, ito ang pinakamainam na paraan upang magamit ang mga baso sa bahay, taliwas sa pagbuhos ng alkohol sa kanila na may karagdagang paggamit ...
Sa ngayon, partikular na lumiko tayo sa aparato. Ito ay ibinigay sa pigura, ngunit sa ngayon ay maikling ipapaliwanag ko kung ano at ano ang.
Kailangan naming kumuha ng isang simpleng lapis at alisin ang puno mula dito gamit ang isang ordinaryong kutsilyo at makakuha ng isang buong tingga sa lapis. Gayunpaman, maaari kang humantong mula sa isang mekanikal na lapis. Ngunit mayroong dalawang paghihirap nang sabay-sabay. Ang una ay ang dati. Ang tingga mula sa isang mekanikal na lapis ay masyadong manipis, para sa amin ito ay simpleng hindi angkop para sa isang visual na eksperimento. Ang pangalawang kahirapan ay ilang hindi maunawaan na komposisyon ng kasalukuyang mga slate. Nararamdaman na hindi sila gawa mula sa grapayt, ngunit mula sa iba pa. Sa pangkalahatan, ang aking karanasan sa naturang "tingga" ay hindi matagumpay, kahit na sa boltahe na 24 V. Salamat dito, kailangan kong pumili ng isang mahusay na makahoy na simpleng lapis. Ang nagreresultang rodite ng grapayt ay magsisilbing isang elektrod para sa amin. Tulad ng naiisip mo, kailangan namin ng dalawang electrode. Salamat dito, pupunta kami upang kunin ang pangalawang lapis, o simpleng basagin ang umiiral na tungkod sa dalawa. Talagang nagawa ko ito.
Sa anumang kawad na magagamit, binabalot namin ang unang lead-electrode (na may isang dulo ng kawad), at ikinonekta namin ang kawad na ito sa minus ng pinagmulan ng kuryente (sa kabilang dulo). Pagkatapos ay hahantong kami sa pangalawang tingga at gawin ang pareho dito. Para sa mga ito, batay dito, kailangan namin ng isang pangalawang kawad. Ngunit sa kasong ito, ikinonekta namin ang kawad na ito sa plus ng suplay ng kuryente. Kung mayroon kang mga problema sa paglakip ng marupok na baras ng grapayt sa kawad, maaari mong gamitin ang mga tool sa kamay, tulad ng tape o duct tape. Kung hindi ito gumana upang ibalot ang dulo ng grapayt gamit ang wire mismo, at ang tape o insulate tape ay hindi nagbigay ng isang mahigpit na contact, pagkatapos ay subukang idikit ang tingga gamit ang conductive glue. Kung wala ka nito, pagkatapos ay hindi bababa sa itali ang tingga sa kawad na may isang thread. Hindi kailangang matakot, ang thread ay hindi masusunog mula sa naturang pag-igting ??
Para sa mga hindi nakakaalam ng anuman tungkol sa mga baterya at mga simpleng patakaran para sa pagkonekta sa kanila, magpapaliwanag ako nang kaunti. Ang bateryang uri ng daliri ay gumagawa ng boltahe na 1.5 V. Sa larawan mayroon akong dalawang magkatulad na baterya. Bukod dito, sila ay konektado unti-unti - sunod-sunod, hindi sa parallel. Sa isang katulad na (serial) na koneksyon, ang panghuling boltahe ay mai-buod mula sa boltahe ng bawat baterya, iyon ay, para sa akin ito ay 1.5 + 1.5 = 3.0 V. Ito ay mas mababa kaysa sa dating nakasaad na 6 volts. Ngunit tinamad ako upang bumili ng ilan pang mga baterya. Prinsipyo ka at dapat malinaw?
Simulan na natin ang eksperimento. Halimbawa, paghigpitan natin ang ating sarili sa electrolysis ng tubig.Una, ito ay napaka-naa-access (Inaasahan kong ang mambabasa ng artikulong ito ay hindi nakatira sa Sahara), at pangalawa, hindi ito nakakasama. Bukod dito, ipapakita ko kung paano gumanap ng dalawa iba-iba karanasan Sa palagay ko mayroon kang sapat na imahinasyon upang makabuo ng isang bungkos ng mga katulad na eksperimento sa iba pang mga sangkap ?? Sa pangkalahatan, ang tubig sa gripo ay angkop para sa amin. Ngunit inirerekumenda kong magdagdag ka ng kaunti pa rito at asinin ito. Konti lang - nangangahulugan ito ng isang maliit na kurot, hindi isang buong kutsara ng panghimagas. Ito ay mahalaga! Pukawin ng mabuti ang asin upang matunaw. Kaya't ang tubig, pagiging isang dielectric sa isang purong estado, ay perpektong magsasagawa ng kuryente. sa simula ng eksperimento, punasan ang mesa mula sa potensyal na kahalumigmigan, at pagkatapos ay ilagay ang pinagmulan ng kuryente at isang baso ng tubig dito.
Ibinaba namin ang parehong mga electrode, naroroon sa ilalim ng boltahe, sa tubig. Sa parehong oras, siguraduhin na ang grapayt lamang ang nahuhulog sa tubig, at ang kawad mismo ay hindi dapat hawakan ang tubig. Maaaring maantala ang simula ng eksperimento. Ang oras ay nakasalalay sa maraming mga tagapagpahiwatig: sa komposisyon ng tubig, ang kalidad ng mga wire, ang kalidad ng grapayt at, siyempre, ang boltahe ng mapagkukunan ng kuryente. Ang simula ng aking reaksyon ay naantala ng ilang segundo. Nagsisimula ang oxygen sa pag-evolve sa electrode na konektado sa plus ng mga baterya. Ang hydrogen ay ilalabas sa elektrod na konektado sa minus. Dapat pansinin na mayroong higit pang mga bula ng hydrogen. Napakaliit na mga bula ang dumidikit sa paligid ng bahagi ng grapayt na nakalubog sa tubig. Pagkatapos ang ilan sa mga bula ay nagsisimulang lumutang.
Electrode sa simula ng eksperimento. Wala pang mga bula ng gas. Ang mga bula ng hydrogen na nabuo sa elektrod na konektado sa negatibong poste ng mga baterya
Ano ang iba pang mga eksperimento? Kung nakapaglaro ka nang sapat sa hydrogen at oxygen, nagpapatuloy kami sa isa pang eksperimento. Ito ay mas kawili-wili, lalo na para sa mga mananaliksik sa bahay. Ito ay kagiliw-giliw na posible na hindi lamang ito makita, ngunit maamoy din ito. Sa nakaraang karanasan, nakatanggap kami ng oxygen at hydrogen, kung saan, sa palagay ko, ay hindi gaanong kamangha-mangha. At sa isa pang eksperimento, nakakakuha kami ng dalawang sangkap (kapaki-pakinabang sa pang-araw-araw na buhay, sa pamamagitan ng paraan). sa simula ng eksperimento, itigil ang nakaraang eksperimento at patuyuin ang mga electrode. Ngayon kumuha ng table salt (na karaniwang ginagamit mo sa silid sa kusina) at matunaw ito sa bigat ng tubig. Sa kasong ito, hindi isang maliit na halaga. Sa totoo lang, ang isang disenteng halaga ng asin ay ang tanging bagay na nagpapakaiba sa pangalawang karanasan mula sa una. Matapos matunaw ang asin, maaari mong agad na ulitin ang eksperimento. Ngayon may ibang reaksyon na nagaganap. Sa isang mahusay na elektrod, hindi oxygen ang pinakawalan ngayon, ngunit murang luntian. At sa negatibo, ang hydrogen ay pinakawalan din. Tulad ng para sa baso kung saan matatagpuan ang solusyon sa asin, ang sodium hydroxide ay mananatili dito pagkatapos ng matagal na electrolysis. Ito ang pamilyar na caustic soda, alkali.
Chlorine, maaamoy mo ito. Ngunit para sa pinakamahusay na epekto, inirerekumenda ko ang pagkuha ng boltahe na hindi bababa sa 12 V. Kung hindi man, maaaring hindi mo maramdaman ang aroma. Ang pagkakaroon ng alkali (pagkatapos ng isang napakahabang electrolysis) sa baso ay maaaring masuri sa maraming paraan. Ang pinakasimpleng at pinaka-marahas ay ilagay ang iyong kamay sa baso. Sinasabi ng isang etniko na tanda na kung nagsimula ang isang nasusunog na pandamdam, mayroong alkali sa baso. Ang isang mas matalinong at mas natatanging paraan ay ang pagsubok sa litmus. Kung ang iyong paaralan ay napakahirap na hindi ito nakakakuha ng isang litmus, tutulungan ka ng mga madaling gamiting tagapagpahiwatig. Ang isa sa mga ito, tulad ng sinasabi nila, ay maaaring magsilbing isang patak ng beet juice ?? Ngunit posible na ihulog lamang ang isang maliit na taba sa solusyon. Sa pagkakaalam ko, dapat maganap ang saponification.
Para sa napaka-usyoso, ilalarawan ko kung ano talaga ang nangyari sa panahon ng mga eksperimento. Sa unang eksperimento, sa ilalim ng impluwensya ng isang kasalukuyang kuryente, naganap ang isang katulad na reaksyon: 2 H2O >>> 2 H2 + O2 Ang parehong gas natural na lumutang mula sa tubig hanggang sa ibabaw. Sa pamamagitan ng paraan, ang mga lumulutang na gas ay maaaring nakulong. Maaari mo ba itong gawin?
Sa isa pang eksperimento, ang reaksyon ay ganap na magkakaiba.Pinasimulan din ito ng isang kasalukuyang kuryente, ngunit ngayon hindi lamang ang tubig, ngunit ang asin din ang kumilos bilang mga reagent: 4H2O + 4NaCl >>> 4NaOH + 2H2 + 2Cl2 Tandaan na ang reaksyon ay dapat maganap sa labis na tubig. Upang malaman kung anong halaga ng asin ang itinuturing na pinakamalaking, maaari mo itong bilangin mula sa reaksyong nasa itaas. Maaari mo ring pag-isipan kung paano pagbutihin ang aparato o kung anong iba pang mga eksperimento ang maaaring gawin. Sa katunayan, posible na ang sodium hypochlorite ay maaaring makuha ng electrolysis. Sa mga kondisyon sa laboratoryo, sa karamihan ng mga kaso, nakukuha ito sa pamamagitan ng pagdaan ng gas na murang luntian sa pamamagitan ng isang solusyon ng sodium hydroxide.