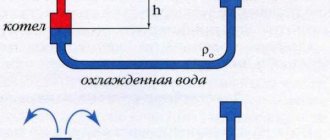
Metoder til produktion af brint under industrielle forhold
Ekstraktion ved metanomdannelse
... Vand i damptilstand, forvarmet til 1000 grader Celsius, blandes med methan under tryk og i nærværelse af en katalysator. Denne metode er interessant og gennemprøvet. Det skal også bemærkes, at den konstant forbedres: søgningen efter nye katalysatorer, billigere og mere effektive, er i gang.
Overvej den ældste metode til produktion af brint - kulforgasning
... Forudsat at der ikke er luftadgang og en temperatur på 1300 grader Celsius opvarmes kul og vanddamp. Således fortrænges hydrogen fra vand, og der opnås carbondioxid (hydrogen vil være øverst, carbondioxid, også opnået som et resultat af reaktionen, er i bunden). Dette vil være adskillelsen af gasblandingen, alt er meget simpelt.
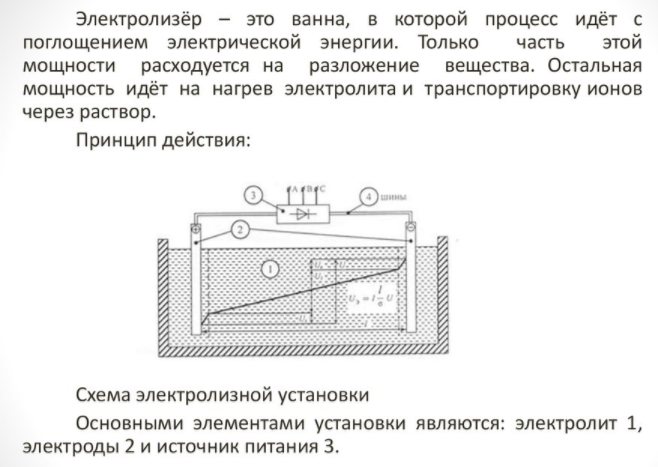
Opnåelse af brint ved elektrolyse af vand
betragtes som den enkleste mulighed. Til implementeringen er det nødvendigt at hælde en sodavand i beholderen og også placere to elektriske elementer der. Den ene vil blive ladet positivt (anode) og den anden negativt (katode). Når der tilføres strøm, går brint til katoden og ilt til anoden.
Opnåelse af brint ved metoden delvis oxidation
... Til dette anvendes en legering af aluminium og gallium. Det anbringes i vand, hvilket fører til dannelsen af brint og aluminiumoxid under reaktionen. Gallium er nødvendigt for at reaktionen kan finde sted fuldt ud (dette element forhindrer aluminium i at oxideres for tidligt).
Nyligt erhvervet relevans metode til anvendelse af bioteknologi
: under betingelse af mangel på ilt og svovl begynder klamydomonas at frigive intensivt brint. En meget interessant effekt, som nu undersøges aktivt.

Glem ikke en anden gammel, gennemprøvet metode til brintproduktion, som består i at bruge forskellige alkaliske elementer
og vand. I princippet er denne teknik mulig i laboratorieindstillinger med de nødvendige sikkerhedsforanstaltninger på plads. Således dannes der under reaktionen (det fortsætter med opvarmning og med katalysatorer) et metaloxid og hydrogen. Det er kun at samle det.
Få brint forbi interaktion mellem vand og kulilte
kun muligt i et industrielt miljø. Der dannes kuldioxid og brint, princippet om deres adskillelse er beskrevet ovenfor.

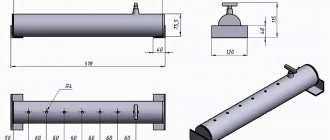
Brintgeneratorens rækkevidde
H2 er en moderne energibærer, der bruges aktivt i mange industriområder. Her er blot nogle få:
- produktion af hydrogenchlorid (HC) l;
- produktion af brændstof til raketkastere;
- produktion af ammoniak;
- bearbejdning og skæring af metal på det;
- udvikling af gødning til sommerhuse;
- syntese af salpetersyre;
- skabelse af methylalkohol;
- fødevareindustri;
- produktion af saltsyre;
- oprettelse af varme gulvsystemer.
Derudover er HHO blevet meget nyttigt i hverdagen, om end med forbehold. Først og fremmest bruges det til autonome varmesystemer. Derudover tilsættes Browns gas til benzin i et forsøg på at narre motoren og spare på brændstof.
Begge sager har deres egne særegenheder. Så når du organiserer opvarmning af hjemmet, skal du tage højde for, at forbrændingstemperaturen for HHO er en størrelsesorden højere end metanens. I denne henseende er det nødvendigt at købe en speciel, dyr kedel med en varmebestandig dyse. Ellers vil ejeren og hans hjem være i betydelig fare.
OPFINDELSEN HAR FØLGENDE FORDELE
Varmen opnået ved oxidation af gasser kan bruges direkte på stedet, og hydrogen og ilt opnås ved bortskaffelse af spildamp og procesvand.
Lavt vandforbrug ved generering af elektricitet og varme.
Enkelheden i vejen.
Betydelige energibesparelser som det bruges kun på opvarmning af starteren til det etablerede termiske regime.
Høj produktivitet i processen, fordi dissociation af vandmolekyler varer tiendedele af et sekund.
Eksplosion og brandsikkerhed af metoden, fordi i implementeringen er der ikke behov for beholdere til opsamling af brint og ilt.
Under driften af installationen renses vand gentagne gange og omdannes til destilleret vand. Dette eliminerer sedimenter og kalk, hvilket øger installationens levetid.
Installationen er lavet af almindeligt stål; undtagen kedler lavet af varmebestandigt stål med foring og afskærmning af deres vægge. Det vil sige, der kræves ingen specielle dyre materialer.
Opfindelsen kan finde anvendelse i
industri ved at erstatte kulbrinte og nukleart brændsel i kraftværker med billigt, udbredt og miljøvenligt vand, samtidig med at kraften fra disse anlæg opretholdes.
Brint derhjemme: er der en fordel
Vi bemærker med det samme: det er urentabelt at bruge en brintgenerator til at opvarme et hus. Du bruger mere elektricitet på at producere ren H2, end du får energi efter at have brændt den. Så for 1 kW varme bruges 2 kW elektricitet, det vil sige, der er ingen fordel. Det er lettere at installere nogen af de elektriske kedler derhjemme.
For at udskifte 1 liter benzin til en bil skal du bruge 4766 liter rent brint eller 7150 liter oxyhydrogengas, hvoraf 1/3 er ilt. Indtil videre har selv de bedste hjerner i verden ikke udviklet en enhed, der er i stand til at levere sådan ydeevne.


PÅSTAND
Metode til fremstilling af brint og ilt fra vanddamp
, herunder at føre denne damp gennem et elektrisk felt, kendetegnet ved, at de bruger overophedet vanddamp med en temperatur
500 - 550 ° C
, passeret gennem et højspændings-jævnstrøm elektrisk felt for at adskille damp og adskille det i hydrogen- og iltatomer.
Jeg har længe ønsket at gøre en lignende ting. Men yderligere eksperimenter med et batteri og et par elektroder nåede ikke. Jeg ville lave et fuldt udstyret apparat til produktion af brint i mængder til at puste en ballon op. Før jeg lavede et fuldt udstyret apparat til elektrolyse af vand derhjemme, besluttede jeg at kontrollere alt på modellen.
Den generelle ordning for elektrolysatoren ser sådan ud.
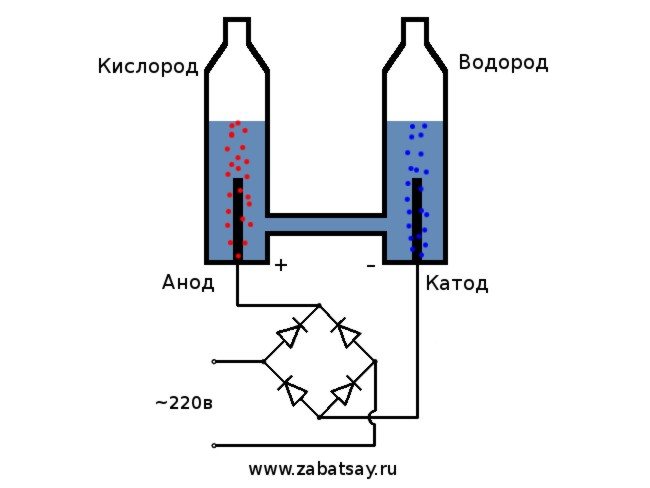

Denne model er ikke egnet til fuld daglig brug. Men det lykkedes os at teste ideen.
Så jeg besluttede at bruge grafit til elektroderne. En fremragende kilde til grafit til elektroder er trolleybusopsamleren. Der er masser af dem, der ligger ved slutstoppene. Det skal huskes, at en af elektroderne vil kollapse.


Vi så og afslutte med en fil. Intensiteten af elektrolyse afhænger af strømstyrken og området for elektroderne.


Ledninger er fastgjort til elektroderne. Ledningerne skal være omhyggeligt isolerede.


For elektrolysermodellen er plastflasker meget velegnede. Huller er lavet i dækslet til rør og ledninger.


Alt er grundigt overtrukket med fugemasse.


Afskårne flaskehalse er velegnede til at forbinde to beholdere.


De skal sammenføjes, og sømmen skal smeltes.


Nødderne er lavet af flaskehætter.


Huller er lavet i to flasker i bunden. Alt er forbundet og omhyggeligt fyldt med fugemasse.


Vi bruger et 220V husstandsnetværk som spændingskilde. Jeg vil advare dig om, at dette er et ret farligt legetøj. Så hvis du ikke har tilstrækkelige færdigheder, eller hvis der er tvivl, er det bedre ikke at gentage det.I husstandsnetværket har vi en vekselstrøm, til elektrolyse skal den rettes ud. En diodebro er perfekt til dette. Den på billedet var ikke stærk nok og brændte hurtigt ud. Den bedste løsning var den kinesiske MB156-diodebro i en aluminiumskasse.


Diodebroen bliver meget varm. Aktiv køling er påkrævet. En køler til en computerprocessor er perfekt. En koblingsboks af passende størrelse kan bruges til kabinettet. Solgt i elektriske varer.


Flere lag pap skal placeres under diodebroen.


De nødvendige huller er lavet i dækslet til samledåsen.


Sådan ser den samlede enhed ud. Elektrolysatoren får strøm fra lysnettet, blæseren drives af en universel strømkilde. En bagepulveropløsning anvendes som en elektrolyt. Her skal det huskes, at jo højere koncentrationen af opløsningen er, jo højere reaktionshastighed. Men på samme tid er opvarmningen også højere. Desuden vil reaktionen af natriumnedbrydning ved katoden bidrage til opvarmningen. Denne reaktion er eksoterm. Som et resultat dannes der hydrogen og natriumhydroxid.


Enheden på billedet ovenfor var meget varm. Det skulle slukkes med jævne mellemrum og vent, indtil det køler af. Opvarmningsproblemet blev delvist løst ved afkøling af elektrolytten. Til dette brugte jeg en springvandspumpe på bordet. Et langt rør løber fra en flaske til en anden gennem en pumpe og en spand koldt vand.


Relevansen af dette emne i dag er ret høj på grund af det faktum, at anvendelsen af brint er ekstremt omfattende, og i sin rene form findes det praktisk talt ingen steder i naturen. Derfor er der udviklet adskillige teknikker, der muliggør ekstraktion af denne gas fra andre forbindelser gennem kemiske og fysiske reaktioner. Dette diskuteres i artiklen ovenfor.
At få brint og kontrollere det for renhed
Hydrogen kan opnås ved omsætning af zink og saltsyre.
Zn + 2HCl = ZnCl2 + H2 ↑
Zink fortrænger brint fra syrer, ligesom alle metaller, der står i spændingsserien til venstre for brint.
For at opsamle brint i et reagensglas skal du vende det på hovedet, fordi brint er lettere end luft og har en tendens opad. Denne metode til opsamling af brint kaldes "luftforskydningsmetoden".
Fig. 1. Indsamling af brint og opsamling ved luftforskydning
Testrøret akkumulerer brint, men det indeholder også luft og derfor ilt. Brint og ilt er eksplosive blandinger. Vi antænder det opsamlede brint med en splinter. Reagensglasset er lille, og eksplosionen af brint og ilt er bare et skarpt brag. Jo mindre ilt i blandingen, jo mere støjsvag bomuld.
Hvis brintet, der er opsamlet i reagensglasset, er rent, vil vi høre en kedelig pop. Sådan brint kan antændes.
Husholdningers brintproduktion
Valg af elektrolysator
For at opnå et element i huset har du brug for et specielt apparat - en elektrolyser. Der er mange muligheder for sådant udstyr på markedet; enhederne tilbydes af både kendte teknologifirmaer og små producenter. Mærkeenheder er dyrere, men byggekvaliteten er højere.
Husholdningsapparatet er lille og let at bruge. Dets vigtigste detaljer er:

Elektrolysator - hvad er det?
- reformator;
- rengøringssystem;
- brændstofceller;
- kompressor udstyr;
- en beholder til opbevaring af brint.
Simpel ledningsvand tages som råmateriale, og elektricitet kommer fra en almindelig stikkontakt. Soldrevne enheder sparer strøm.
Hjembrint bruges i varme- eller madlavningssystemer. Og også beriger de brændstof-luft-blandingen for at øge kraften i bilens motorer.
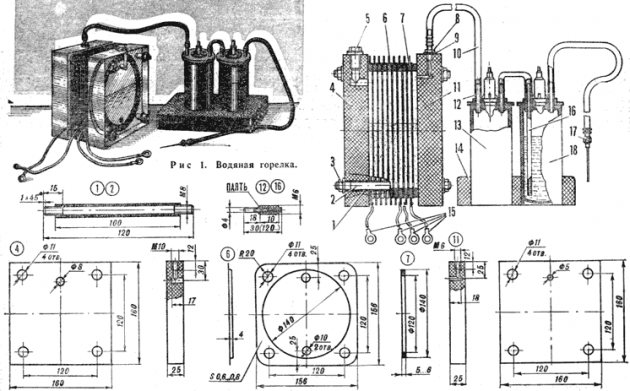
Lav et apparat med dine egne hænder
Det er endnu billigere at fremstille enheden selv derhjemme.En tør celle ligner en forseglet beholder, der består af to elektrodeplader i en beholder med en elektrolytisk opløsning. World Wide Web tilbyder en række monteringsordninger til enheder af forskellige modeller:
- med to filtre;
- med top eller bund arrangement af beholderen;
- med to eller tre ventiler;
- med galvaniseret plade;
- på elektroderne.

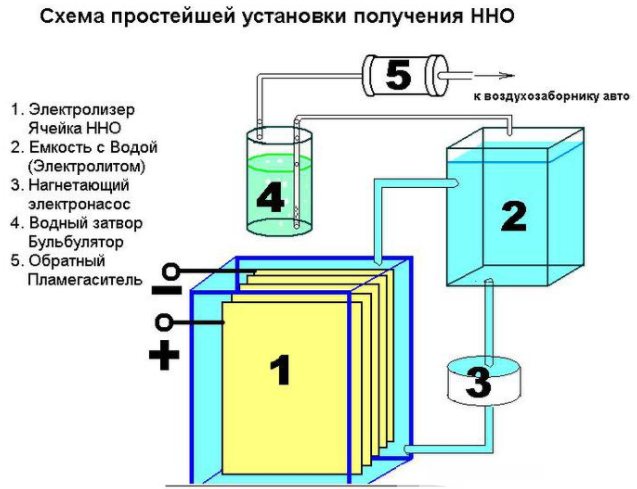
Elektrolyseanordning diagram
Det er ikke svært at skabe en simpel enhed til produktion af brint. Det vil kræve:
- plade rustfrit stål;
- gennemsigtigt rør;
- fittings;
- plastbeholder (1,5 l);
- vandfilter og kontraventil.

Enheden til en simpel enhed til produktion af brint
Derudover er der brug for forskellige hardware: møtrikker, skiver, bolte. Det første trin er at skære arket i 16 firkantede rum, skære et hjørne fra hver af dem. I det modsatte hjørne skal du bore et hul til boltning af pladerne. For at sikre konstant strøm skal pladerne forbindes i henhold til plus - minus - plus - minus skemaet. Disse dele er isoleret fra hinanden med et rør og ved forbindelsen med en bolt og skiver (tre stykker mellem pladerne). 8 plader er placeret på plus og minus.
Når pladerne er samlet korrekt, vil de ikke røre ved elektroderne. De samlede dele sænkes ned i en plastikbeholder. På det sted, hvor væggene berører, er der monteret to monteringshuller med bolte. Installer en sikkerhedsventil for at fjerne overskydende gas. Beslag monteres i beholderlåget, og sømmene forsegles med silikone.
Test af apparatet
For at teste enheden skal du udføre flere handlinger:

Brintproduktionsordning
- Fyld med væske.
- Dæk med et låg, tilslut den ene ende af røret til beslaget.
- Den anden nedsænkes i vand.
- Tilslut til en strømkilde.
Efter at have tilsluttet enheden til en stikkontakt efter nogle få sekunder, vil elektrolyseprocessen og nedbør være synlig.
Rent vand har ikke god elektrisk ledningsevne. For at forbedre denne indikator skal du oprette en elektrolytisk opløsning ved at tilføje et alkali-natriumhydroxid. Det findes i rørrensningsforbindelser som molen.
Metoder til produktion af brint
Brint er et farveløst og lugtfrit luftformigt element med en massefylde på 1/14 i forhold til luft. I en fri stat er det sjældent. Normalt kombineres brint med andre kemiske grundstoffer: ilt, kulstof.
Brintproduktion til industrielle behov og kraftudvikling udføres ved flere metoder. De mest populære er:
- elektrolyse af vand;
- koncentrationsmetode
- kondensvand ved lav temperatur
- adsorption.
Brint kan ikke kun isoleres fra gasformige eller vandforbindelser. Brint produceres ved at udsætte træ og kul for høje temperaturer samt ved at behandle bioaffald.
Atomisk brint til energiteknik opnås ved hjælp af metoden til termisk dissociation af et molekylært stof på en ledning lavet af platin, wolfram eller palladium. Det opvarmes i en brintatmosfære under et tryk på mindre end 1,33 Pa. Og også radioaktive grundstoffer bruges til at producere brint.
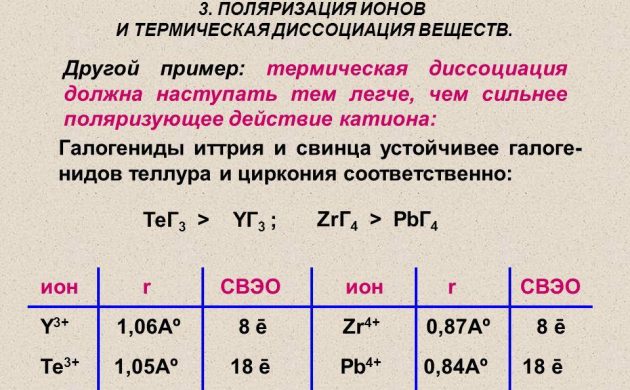

Termisk dissociation
Elektrolysemetode
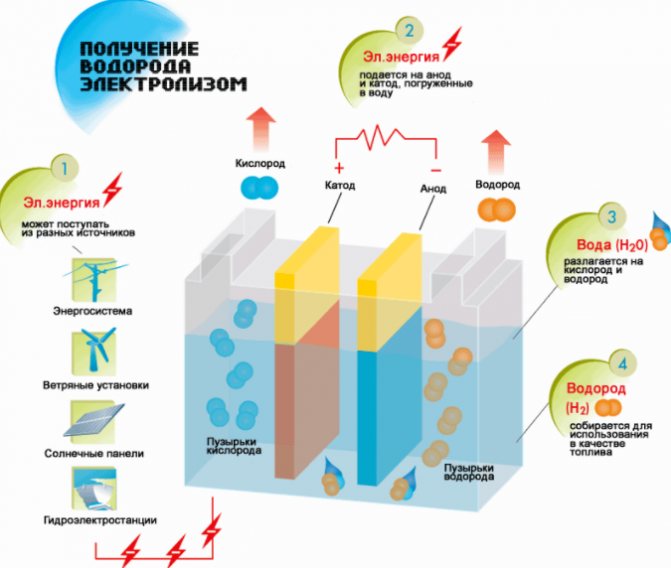
Den enkleste og mest populære metode til brintudvikling er vandelektrolyse. Det tillader produktion af praktisk talt rent brint. Andre fordele ved denne metode er:
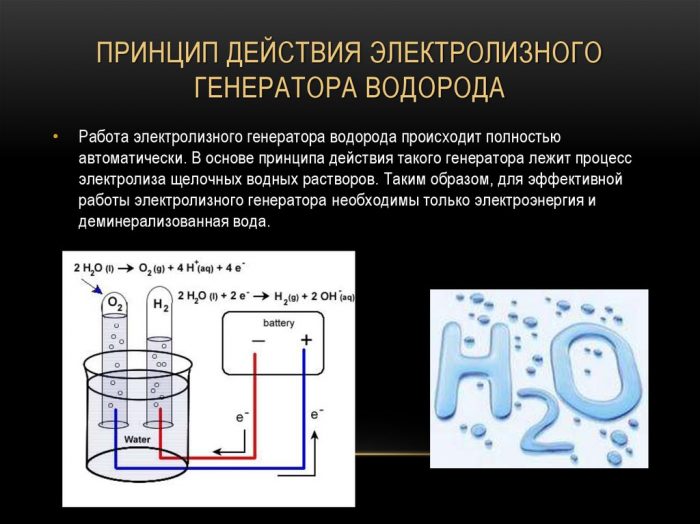

Princippet om drift af elektrolyse-brintgeneratoren
- tilgængelighed af råmaterialer
- modtagelse af et element under tryk;
- evnen til at automatisere processen på grund af manglen på bevægelige dele.
Proceduren til opdeling af en væske ved elektrolyse er omvendt af forbrændingen af brint. Dens essens er, at der under påvirkning af jævnstrøm frigøres ilt og brint på elektroderne dyppet i en vandig elektrolytopløsning.
En yderligere fordel anses for at være produktionen af biprodukter med industriel værdi.Således er der brug for en stor mængde ilt til at katalysere teknologiske processer i energisektoren, rydde op i jord og vandområder og bortskaffe husholdningsaffald. Tungt vand opnået under elektrolyse anvendes til energiteknik i atomreaktorer.
Brintproduktion efter koncentration
Denne metode er baseret på adskillelsen af et element fra gasblandinger, der indeholder det. Således ekstraheres den største del af det industrielt producerede stof ved hjælp af dampreformering af metan. Brint ekstraheret i denne proces anvendes i energi, olieraffinering, raketbygningsindustrier såvel som til produktion af kvælstofgødning. Processen med at opnå H2 udføres på forskellige måder:
- kort cyklus;
- kryogen;
- membran.
Sidstnævnte metode betragtes som den mest effektive og billigere.
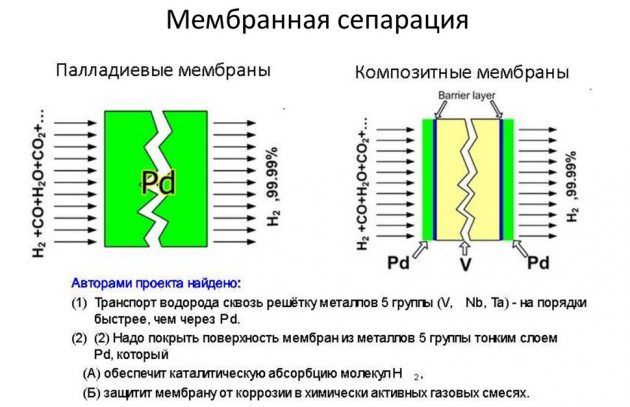

Kondens ved lav temperatur
Denne metode til opnåelse af H2 består i stærk afkøling af gasformige forbindelser under tryk. Som et resultat omdannes de til et to-faset system, som efterfølgende adskilles af en separator i en flydende komponent og en gas. Flydende medier bruges til afkøling:
- vand;
- flydende etan eller propan;
- flydende ammoniak.


Denne procedure er ikke så let som den lyder. Det vil ikke være muligt at adskille kulbrintegasser på en gang. Nogle af komponenterne efterlades med gas taget fra separationsrummet, hvilket ikke er økonomisk. Problemet kan løses ved dybkøling af råmaterialet inden adskillelse. Men dette kræver en masse energi.
I moderne lavtemperatur kondensatorsystemer er der desuden tilvejebragt demethanisering eller deetaniseringskolonner. Gasfasen fjernes fra det sidste separeringstrin, og væsken sendes til destillationskolonnen med en strøm af rå gas efter varmeveksling.
Adsorptionsmetode
Under adsorption bruges adsorbenter til at frigive hydrogen - faste stoffer, der absorberer de nødvendige komponenter i gasblandingen. Aktivt kul, silikatgel, zeolitter anvendes som adsorbenter. For at udføre denne proces anvendes specielle anordninger - cykliske adsorbere eller molekylsigter. Når den implementeres under tryk, kan denne metode genvinde 85% brint.
Hvis vi sammenligner adsorption med kondens ved lav temperatur, kan vi bemærke en lavere materialemæssige og driftsomkostning ved processen - i gennemsnit 30 procent. Brint produceres ved adsorption til energiteknik og ved brug af opløsningsmidler. Denne metode tillader ekstraktion af 90 procent H2 fra gasblandingen og opnå det endelige produkt med en brintkoncentration på op til 99,9%.