Endüstriyel koşullarda hidrojen üretme yöntemleri
Metan dönüşümü ile ekstraksiyon
... 1000 santigrat dereceye kadar önceden ısıtılmış buhar halindeki su, basınç altında ve bir katalizör varlığında metanla karıştırılır. Bu yöntem ilginç ve kanıtlanmıştır, ayrıca sürekli iyileştirildiği de belirtilmelidir: daha ucuz ve daha etkili yeni katalizör arayışı devam etmektedir.
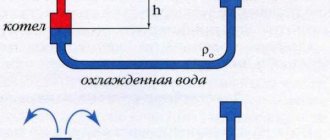
Hidrojen üretmek için en eski yöntemi düşünün - kömür gazlaştırma
... Hava erişiminin olmaması ve 1300 santigrat derece sıcaklıkta kömür ve su buharı ısıtılır. Böylece sudan hidrojen yer değiştirir ve karbondioksit elde edilir (hidrojen üstte, yine reaksiyon sonucu elde edilen karbondioksit altta). Bu gaz karışımının ayrılması olacak, her şey çok basit.
Hidrojen elde etmek suyun elektrolizi
en basit seçenek olarak kabul edilir. Uygulanması için, kabın içine bir soda çözeltisi dökmek ve ayrıca oraya iki elektrikli eleman yerleştirmek gerekir. Biri pozitif (anot) ve diğeri negatif (katot) olarak yüklenecektir. Akım uygulandığında, hidrojen katoda, oksijen ise anoda gidecektir.
Yöntemle hidrojen elde edilmesi kısmi oksidasyon
... Bunun için bir alüminyum ve galyum alaşımı kullanılır. Reaksiyon sırasında hidrojen ve alümina oluşumuna yol açan suya yerleştirilir. Reaksiyonun tam olarak gerçekleşmesi için galyum gereklidir (bu element alüminyumun erken oksitlenmesini önleyecektir).
Yakın zamanda edinilen alaka düzeyi biyoteknoloji kullanma yöntemi
: Oksijen ve kükürt eksikliği koşulu altında, klamidomonas yoğun bir şekilde hidrojeni serbest bırakmaya başlar. Şu anda aktif olarak araştırılmakta olan çok ilginç bir etki.

Farklı kullanmaktan oluşan eski, kanıtlanmış bir hidrojen üretim yöntemini unutmayın. alkali elementler
ve su. Prensip olarak, bu teknik, gerekli güvenlik önlemleri yerinde olan bir laboratuar ortamında uygulanabilir. Böylece, reaksiyon sırasında (ısıtma ve katalizörlerle ilerler), bir metal oksit ve hidrojen oluşur. Sadece onu toplamak için kalır.
Hidrojen alın su ve karbon monoksit etkileşimi
sadece endüstriyel bir ortamda mümkündür. Karbondioksit ve hidrojen oluşur, ayrılma prensibi yukarıda açıklanmıştır.

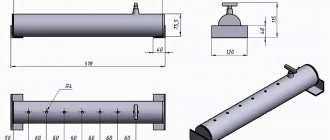
Hidrojen jeneratörünün kapsamı
H2, birçok endüstriyel alanda aktif olarak kullanılan modern bir enerji taşıyıcısıdır. İşte bunlardan sadece birkaçı:
- hidrojen klorür (HC) üretimi 1;
- roketatarlar için yakıt üretimi;
- amonyak üretimi;
- metal işleme ve üzerinde kesme;
- yazlık evler için gübre geliştirilmesi;
- nitrik asit sentezi;
- metil alkolün oluşturulması;
- Gıda endüstrisi;
- hidroklorik asit üretimi;
- sıcak zemin sistemlerinin oluşturulması.
Buna ek olarak, HHO, çekincelere rağmen günlük yaşamda çok faydalı hale geldi. Öncelikle otonom ısıtma sistemleri için kullanılır. Ek olarak, Brown'un gazı, motoru kandırmak ve yakıttan tasarruf etmek amacıyla benzine eklenir.
Her iki vakanın da kendine has özellikleri vardır. Bu nedenle, ev ısıtmasını organize ederken, HHO'nun yanma sıcaklığının metandan daha yüksek bir mertebede olduğunu hesaba katmak gerekir. Bu bağlamda, ısıya dayanıklı nozullu özel, pahalı bir kazan satın almak gerekir. Aksi takdirde, mal sahibi ve evi büyük tehlike altında olacaktır.
BULUŞUN AŞAĞIDAKİ AVANTAJLARA SAHİPTİR
Gazların oksidasyonundan elde edilen ısı doğrudan sahada kullanılabilir ve hidrojen ve oksijen, atık buhar ve proses suyunun bertarafından elde edilir.
Elektrik ve ısı üretirken düşük su tüketimi.
Yolun basitliği.
Olarak önemli enerji tasarrufu sadece marş motorunu yerleşik termal rejime kadar ısıtmak için harcanır.
Sürecin yüksek üretkenliği, çünkü su moleküllerinin ayrışması saniyenin onda biri kadar sürer.
Yöntemin patlama ve yangın güvenliği, çünkü uygulamasında hidrojen ve oksijeni toplamak için kaplara ihtiyaç yoktur.
Tesisatın çalışması sırasında, su tekrar tekrar arıtılır ve damıtılmış suya dönüştürülür. Bu, kurulumun hizmet ömrünü uzatan tortu ve tortuları ortadan kaldırır.
Kurulum normal çelikten yapılmıştır; duvarları astarlı ve perdeli ısıya dayanıklı çelikten yapılmış kazanlar hariç. Yani, özel bir pahalı malzemeye gerek yoktur.
Buluş, uygulama bulabilir
Santrallerdeki hidrokarbon ve nükleer yakıtı ucuz, yaygın ve çevre dostu su ile değiştirerek, bu santrallerin gücünü koruyarak sanayi.
Evde hidrojen: bir faydası var mı
Hemen not edelim: Ev ısıtması için bir hidrojen jeneratörü kullanmak kârsızdır. Saf H2 üretmek için, yaktıktan sonra alacağınızdan daha fazla elektrik harcayacaksınız. Yani 1 kW'lık ısı için 2 kW elektrik harcanır yani faydası olmaz. Elektrikli kazanlardan herhangi birini evde kurmak daha kolaydır.
Bir araba için 1 litre benzini değiştirmek için, 4766 litre saf hidrojene veya 1 / 3'ü oksijen olan 7150 litre oksihidrojen gazına ihtiyacınız olacak. Şimdiye kadar, dünyanın en iyi beyinleri bile bu tür bir performans sunabilecek bir birim geliştirmedi.


İDDİA
Su buharından hidrojen ve oksijen üretme yöntemi
, bu buharı bir elektrik alanından geçirmek dahil, karakterize edici özelliği, bir sıcaklıkta aşırı ısıtılmış su buharı kullanmalarıdır.
500 - 550 o C
, buharı ayrıştırmak ve onu hidrojen ve oksijen atomlarına ayırmak için yüksek voltajlı bir doğru akım elektrik alanından geçti.
Uzun zamandır benzer bir şey yapmak istedim. Ancak bir pil ve bir çift elektrotla ilgili başka deneyler ulaşamadı. Bir balonu şişirmek için miktarlarda hidrojen üretimi için tam teşekküllü bir cihaz yapmak istedim. Evde suyun elektrolizi için tam teşekküllü bir cihaz yapmadan önce, modeldeki her şeyi kontrol etmeye karar verdim.
Elektrolizörün genel şeması buna benzer.
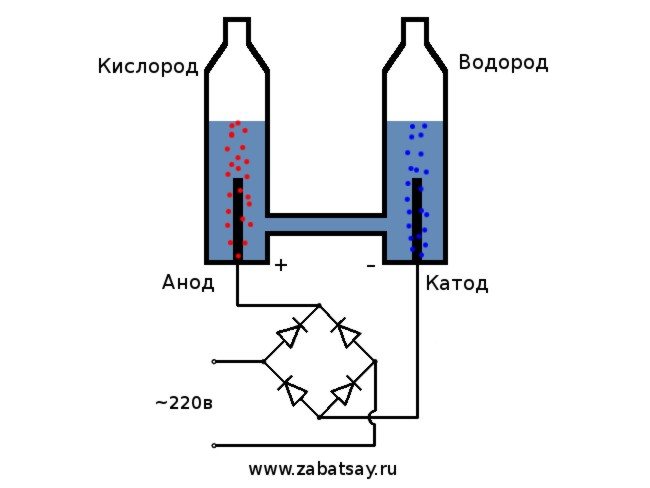

Bu model tam günlük kullanım için uygun değildir. Ama fikri test etmeyi başardık.
Bu yüzden elektrotlar için grafit kullanmaya karar verdim. Elektrotlar için mükemmel bir grafit kaynağı troleybüs toplayıcıdır. Son duraklarda bir sürü yalan var. Elektrotlardan birinin çökeceği unutulmamalıdır.


Bir dosya ile gördük ve değiştirdik. Elektrolizin yoğunluğu, akımın gücüne ve elektrotların alanına bağlıdır.


Teller elektrotlara bağlanır. Teller dikkatlice yalıtılmalıdır.


Plastik şişeler elektrolizör modelinin kasasına oldukça uygundur. Borular ve teller için kapakta delikler açılmıştır.


Her şey tamamen sızdırmazlık maddesi ile kaplanmıştır.


Kesik şişe boyunları iki kabı bağlamak için uygundur.


Birleştirilmeleri gerekir ve dikiş eritilmelidir.


Somunlar şişe kapaklarından yapılmıştır.


Delikler altta iki şişede yapılır. Her şey birbirine bağlı ve dikkatlice dolgu macunu ile doldurulur.


Voltaj kaynağı olarak 220V ev ağı kullanacağız. Sizi bunun oldukça tehlikeli bir oyuncak olduğu konusunda uyarmak istiyorum. Bu nedenle, yeterli beceriniz yoksa veya şüpheleriniz varsa, tekrar etmemek daha iyidir.Ev ağında alternatif bir akımımız var, elektroliz için düzeltilmesi gerekiyor. Bunun için bir diyot köprüsü mükemmeldir. Fotoğraftaki yeterince güçlü değildi ve çabucak yandı. En iyi seçenek, alüminyum kasadaki Çin MB156 diyot köprüsü idi.


Diyot köprüsü çok ısınır. Aktif soğutma gerekli olacaktır. Bir bilgisayar işlemcisi için bir soğutucu mükemmeldir. Muhafaza için uygun boyutta bir bağlantı kutusu kullanılabilir. Elektrikli ürünlerde satılır.


Diyot köprüsünün altına birkaç kat karton yerleştirilmelidir.


Bağlantı kutusu kapağına gerekli delikler açılır.


Monte edilen ünite böyle görünüyor. Elektrolizör ana şebekeden beslenir, fan evrensel bir güç kaynağı ile çalışır. Elektrolit olarak bir kabartma tozu çözeltisi kullanılır. Burada, çözeltinin konsantrasyonu ne kadar yüksek olursa, reaksiyon hızının o kadar yüksek olduğu unutulmamalıdır. Ancak aynı zamanda ısıtma da daha yüksektir. Ayrıca, katotta sodyum ayrışmasının reaksiyonu ısınmaya katkıda bulunacaktır. Bu reaksiyon ekzotermiktir. Sonuç olarak, hidrojen ve sodyum hidroksit oluşacaktır.


Yukarıdaki fotoğraftaki cihaz çok sıcaktı. Periyodik olarak kapatılması ve soğumasını beklemesi gerekiyordu. Isıtma sorunu, elektrolitin soğutulmasıyla kısmen çözüldü. Bunun için bir masa üstü fıskiye pompası kullandım. Uzun bir tüp, bir şişeden diğerine bir pompa ve bir kova soğuk su ile akar.


Hidrojen kullanma alanının son derece geniş olması ve saf haliyle pratikte doğada hiçbir yerde bulunmaması nedeniyle bugün bu konunun alaka düzeyi oldukça yüksektir. Bu nedenle, bu gazın diğer bileşiklerden kimyasal ve fiziksel reaksiyonlarla ekstraksiyonuna izin veren birkaç teknik geliştirilmiştir. Bu, yukarıdaki makalede tartışılmaktadır.
Hidrojen elde etmek ve saflığını kontrol etmek
Hidrojen, çinko ve hidroklorik asidin reaksiyona sokulmasıyla elde edilebilir.
Zn + 2HCl = ZnCl2 + H2 ↑
Çinko, hidrojenin solundaki voltaj dizisinde duran tüm metaller gibi hidrojeni asitlerden uzaklaştırır.
Bir test tüpünde hidrojeni toplamak için, onu ters çevirmeniz gerekir, çünkü hidrojen havadan daha hafiftir ve yukarı doğru meyillidir. Bu hidrojeni toplama yöntemine "havayla yer değiştirme yöntemi" denir.
İncir. 1. Hidrojenin elde edilmesi ve havayla yer değiştirerek toplanması
Test tüpü hidrojen biriktirir, ancak aynı zamanda hava ve dolayısıyla oksijen içerir. Hidrojen ve oksijen patlayıcı karışımlardır. Toplanan hidrojeni bir kıymıkla tutuşturuyoruz. Test tüpü küçüktür ve hidrojen ve oksijen patlaması sadece keskin bir patlamadır. Karışımda ne kadar az oksijen varsa, pamuk o kadar sessizdir.
Test tüpünde toplanan hidrojen safsa, donuk bir ses duyacağız. Böyle bir hidrojen tutuşabilir.
Ev hidrojen üretimi
Elektrolizör seçimi
Evin bir elemanını elde etmek için özel bir aparata ihtiyacınız var - bir elektrolizör. Piyasada bu tür ekipmanlar için birçok seçenek bulunmaktadır, cihazlar hem tanınmış teknoloji şirketleri hem de küçük üreticiler tarafından sunulmaktadır. Markalı birimler daha pahalıdır, ancak yapım kalitesi daha yüksektir.
Ev aleti küçüktür ve kullanımı kolaydır. Ana detayları:
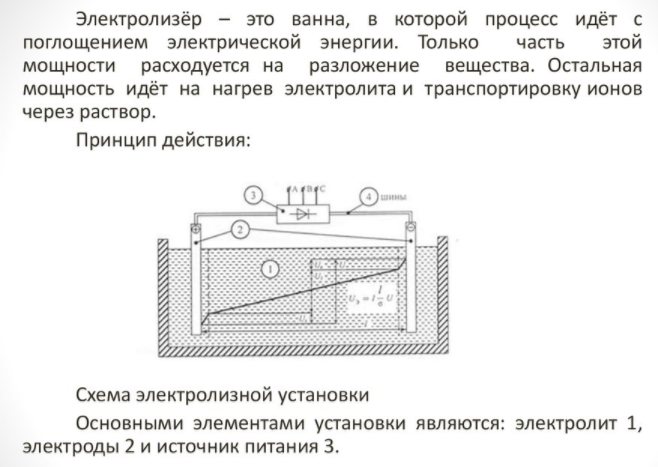

Elektrolizör - nedir
- reformcu;
- temizleme sistemi;
- yakıt hücreleri;
- kompresör ekipmanı;
- hidrojeni depolamak için bir kap.
Hammadde olarak basit musluk suyu alınır ve elektrik normal bir prizden gelir. Güneş enerjisiyle çalışan üniteler elektrikten tasarruf sağlar.
Evde hidrojen, ısıtma veya pişirme sistemlerinde kullanılır. Ayrıca otomobilin motorlarının gücünü artırmak için yakıt-hava karışımını zenginleştiriyorlar.
Kendi elinizle bir aparat yapmak
Cihazı evde kendiniz yapmak daha da ucuzdur.Kuru bir hücre, elektrolitik çözelti içeren bir kap içinde iki elektrot plakasından oluşan kapalı bir kap gibi görünür. World Wide Web, farklı modellerde cihazlar için çeşitli montaj şemaları sunar:
- iki filtreli;
- kabın üst veya alt düzenlemesi ile;
- iki veya üç valfli;
- galvanizli levha ile;
- elektrotlarda.
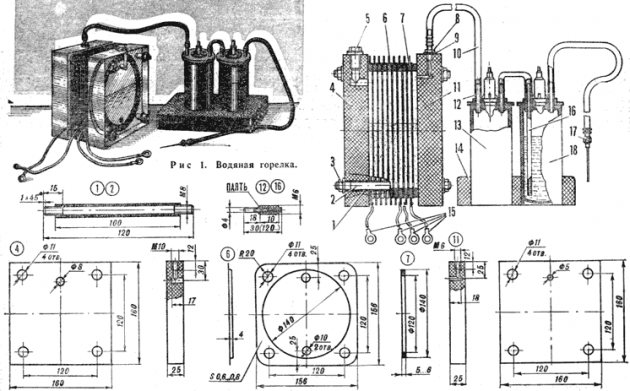

Elektroliz cihazı diyagramı
Hidrojen üretmek için basit bir cihaz yaratmak zor değildir. Şunları gerektirecektir:
- paslanmaz çelik sac;
- şeffaf tüp;
- bağlantı parçaları;
- plastik kap (1,5 l);
- su filtresi ve çek valf.
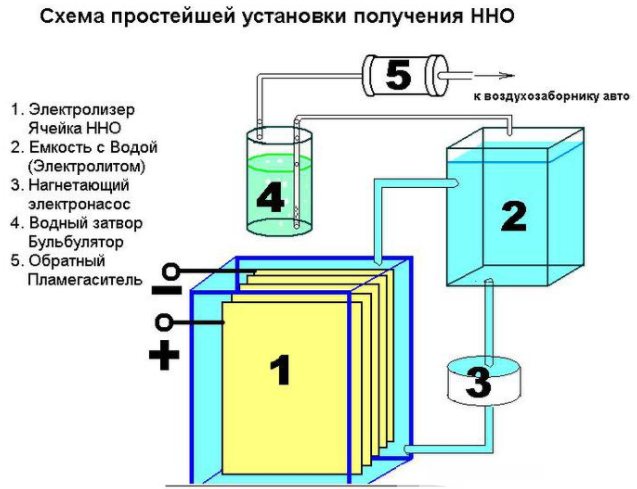

Hidrojen üretmek için basit bir cihazın cihazı
Ek olarak, çeşitli donanımlara ihtiyaç duyulacaktır: somunlar, rondelalar, cıvatalar. İlk adım, tabakayı 16 kare bölmeye kesmek, her birinden bir köşe kesmek. Bunun karşı köşesinde, plakaları cıvatalamak için bir delik açmak gerekir. Sabit akım sağlamak için, plakalar artı - eksi - artı - eksi şemasına göre bağlanmalıdır. Bu parçalar birbirinden bir boru ile ve bir cıvata ve rondela ile bağlantıda (plakalar arasında üç adet) izole edilir. Artı ve eksi üzerine 8 tabak yerleştirilir.
Düzgün bir şekilde monte edildiğinde, plakaların nervürleri elektrotlara temas etmeyecektir. Birleştirilen parçalar plastik bir kaba indirilir. Duvarların temas ettiği noktada civatalarla iki adet montaj deliği açılır. Fazla gazı çıkarmak için bir emniyet valfi takın. Bağlantı parçaları kap kapağına monte edilir ve dikişler silikon ile kapatılır.
Aparatın test edilmesi
Cihazı test etmek için birkaç eylem gerçekleştirin:
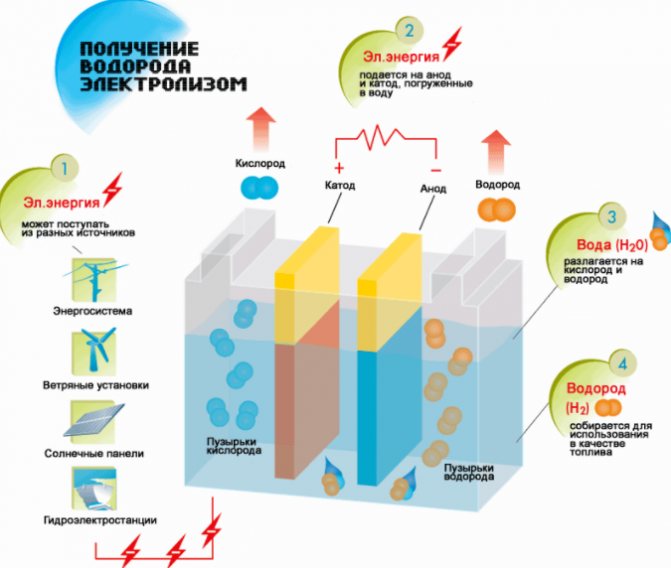

Hidrojen üretim şeması
- Sıvı ile doldurun.
- Bir kapakla örtün, borunun bir ucunu bağlantı parçasına bağlayın.
- İkincisi suya batırılır.
- Bir güç kaynağına bağlayın.
Cihazı prize taktıktan birkaç saniye sonra elektroliz işlemi ve çökelme farkedilir hale gelecektir.
Saf su iyi elektrik iletkenliğine sahip değildir. Bu göstergeyi iyileştirmek için, bir alkali - sodyum hidroksit ekleyerek bir elektrolitik çözelti oluşturmanız gerekir. Mole gibi boru temizleme bileşiklerinde bulunur.
Hidrojen üretme yöntemleri
Hidrojen, havaya göre yoğunluğu 1/14 olan renksiz ve kokusuz bir gaz elementidir. Özgür bir durumda nadirdir. Genellikle hidrojen, diğer kimyasal elementlerle birleştirilir: oksijen, karbon.
Endüstriyel ihtiyaçlar ve enerji mühendisliği için hidrojen üretimi birkaç yöntemle gerçekleştirilmektedir. En popüler olanlar:
- suyun elektrolizi;
- konsantrasyon yöntemi;
- düşük sıcaklıkta yoğunlaşma;
- adsorpsiyon.
Hidrojen sadece gaz veya su bileşiklerinden izole edilemez. Hidrojen, odun ve kömürün yüksek sıcaklıklara maruz bırakılmasının yanı sıra biyoatıkların işlenmesiyle üretilir.
Enerji mühendisliği için atomik hidrojen, bir moleküler maddenin platin, tungsten veya paladyumdan yapılmış bir tel üzerinde termal ayrışma yöntemi kullanılarak elde edilir. 1.33 Pa'dan daha düşük bir basınç altında hidrojen atmosferinde ısıtılır. Ayrıca hidrojen elde etmek için radyoaktif elementler kullanılır.

Termal ayrışma
Elektroliz yöntemi
Hidrojen evriminin en basit ve en popüler yöntemi su elektrolizidir. Pratik olarak saf hidrojen üretimine izin verir. Bu yöntemin diğer avantajları şunlardır:
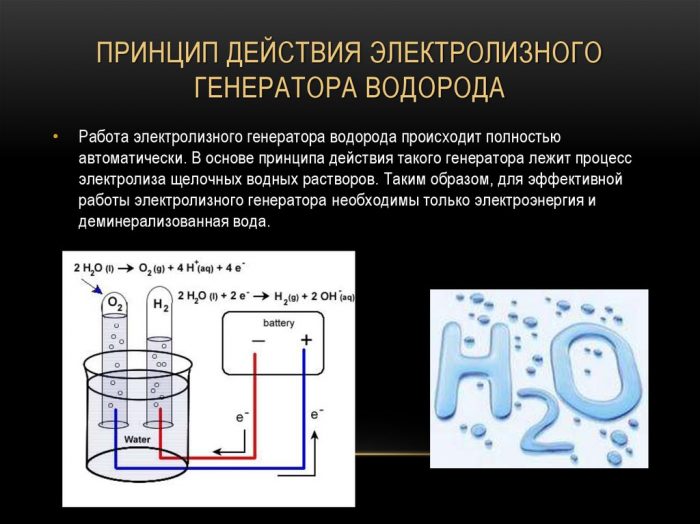

Elektroliz hidrojen jeneratörünün çalışma prensibi
- hammadde mevcudiyeti;
- basınç altında bir elementi almak;
- hareketli parçaların olmaması nedeniyle süreci otomatikleştirme yeteneği.
Bir sıvıyı elektrolizle bölme prosedürü, hidrojenin yanmasının tersidir. Özü, doğru akımın etkisi altında, sulu bir elektrolit çözeltisine daldırılan elektrotlarda oksijen ve hidrojenin salınmasıdır.
Ek bir avantaj, endüstriyel değeri olan yan ürünlerin üretimi olarak kabul edilir.Bu nedenle, enerji sektöründeki teknolojik süreçleri katalize etmek, toprak ve su kütlelerini temizlemek ve evsel atıkları atmak için büyük miktarda oksijene ihtiyaç vardır. Elektroliz sırasında elde edilen ağır su, nükleer reaktörlerde enerji mühendisliğinde kullanılmaktadır.
Konsantrasyona göre hidrojen üretimi
Bu yöntem, bir elementin onu içeren gaz karışımlarından ayrılmasına dayanır. Bu nedenle, endüstriyel hacimlerde üretilen maddenin en büyük kısmı, metanın buharla reformasyonu kullanılarak ekstrakte edilir. Bu süreçte çıkarılan hidrojen enerji, petrol arıtma, roket yapımı endüstrilerinin yanı sıra azotlu gübrelerin üretiminde kullanılır. H2 elde etme süreci farklı şekillerde gerçekleştirilir:
- kısa döngü;
- kriyojenik;
- zar.
İkinci yöntem, en etkili ve daha az maliyetli olarak kabul edilir.
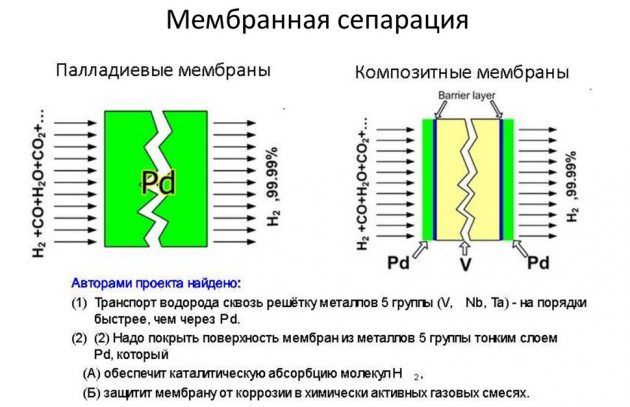

Düşük sıcaklıkta yoğuşma
Bu H2 elde etme yöntemi, gaz halindeki bileşiklerin basınç altında güçlü bir şekilde soğutulmasını içerir. Sonuç olarak, daha sonra bir ayırıcı ile sıvı bir bileşene ve bir gaza ayrılan iki fazlı bir sisteme dönüştürülürler. Sıvı ortam soğutma için kullanılır:
- Su;
- sıvılaştırılmış etan veya propan;
- sıvı amonyak.


Bu prosedür göründüğü kadar kolay değil. Hidrokarbon gazlarının tek seferde temiz bir şekilde ayrıştırılması mümkün olmayacaktır. Bazı bileşenler ekonomik olmayan ayırma bölmesinden alınan gazla çıkacaktır. Problem, ayırmadan önce hammaddenin derinlemesine soğutulmasıyla çözülebilir. Ancak bu çok fazla enerji gerektirir.
Modern düşük sıcaklıklı kondansatör sistemlerinde ek olarak demetanizasyon veya etanizasyon sütunları sağlanır. Gaz fazı son ayırma aşamasından çıkarılır ve sıvı, ısı değişiminden sonra ham gaz akışı ile rektifikasyon kolonuna gönderilir.
Adsorpsiyon yöntemi
Adsorpsiyon sırasında, hidrojeni serbest bırakmak için adsorbanlar kullanılır - gaz karışımının gerekli bileşenlerini emen katılar. Adsorban olarak aktif karbon, silikat jel, zeolitler kullanılır. Bu işlemi gerçekleştirmek için özel cihazlar kullanılır - döngüsel adsorberler veya moleküler elekler. Basınç altında uygulandığında, bu yöntem% 85 hidrojeni geri kazanabilir.
Adsorpsiyonu düşük sıcaklıkta yoğuşma ile karşılaştırırsak, işlemin ortalama olarak yüzde 30 daha düşük malzeme ve operasyonel maliyetini fark edebiliriz. Hidrojen, enerji mühendisliği için adsorpsiyonla ve çözücülerin kullanımıyla üretilir. Bu yöntem, gaz karışımından H2'nin yüzde 90'ının çıkarılmasına ve% 99,9'a kadar hidrojen konsantrasyonuna sahip nihai ürünün elde edilmesine izin verir.