Kaedah untuk menghasilkan hidrogen dalam keadaan industri
Pengekstrakan dengan penukaran metana
... Air dalam keadaan wap, dipanaskan hingga 1000 darjah Celsius, dicampurkan dengan metana di bawah tekanan dan dengan adanya pemangkin. Kaedah ini menarik dan terbukti, perlu juga diperhatikan bahawa kaedah ini terus diperbaiki: pencarian pemangkin baru, lebih murah dan lebih berkesan, sedang dilakukan.
Pertimbangkan kaedah tertua untuk menghasilkan hidrogen - gasifikasi arang batu
... Dengan syarat tidak ada akses udara dan suhu 1300 darjah Celsius, arang batu dan wap air dipanaskan. Oleh itu, hidrogen dipindahkan dari air, dan karbon dioksida diperoleh (hidrogen akan berada di puncak, karbon dioksida, juga diperoleh sebagai hasil tindak balas, berada di bahagian bawah). Ini akan menjadi pemisahan campuran gas, semuanya sangat sederhana.
Memperoleh hidrogen dengan elektrolisis air
dianggap sebagai pilihan paling mudah. Untuk pelaksanaannya, perlu menuangkan larutan soda ke dalam bekas, dan juga meletakkan dua elemen elektrik di sana. Satu akan dikenakan secara positif (anod) dan yang lain secara negatif (katod). Semasa arus digunakan, hidrogen akan menuju ke katod dan oksigen ke anod.
Memperoleh hidrogen dengan kaedah pengoksidaan separa
... Untuk ini, aloi aluminium dan galium digunakan. Ia diletakkan di dalam air, yang membawa kepada pembentukan hidrogen dan alumina semasa tindak balas. Gallium diperlukan agar tindak balas berlaku sepenuhnya (elemen ini akan mengelakkan aluminium mengoksidasi sebelum waktunya).
Perkaitan yang baru diperoleh kaedah menggunakan bioteknologi
: dalam keadaan kekurangan oksigen dan sulfur, klamidoma mula melepaskan hidrogen secara intensif. Kesan yang sangat menarik yang kini sedang dikaji secara aktif.

Jangan lupa kaedah hidrogen lama yang sudah terbukti, yang terdiri daripada penggunaan yang berbeza unsur alkali
dan air. Pada prinsipnya, teknik ini dapat dilaksanakan di persekitaran makmal dengan langkah-langkah keselamatan yang diperlukan. Oleh itu, semasa tindak balas (ia diteruskan dengan pemanasan dan dengan pemangkin), oksida logam dan hidrogen terbentuk. Tinggal hanya untuk mengumpulkannya.
Dapatkan hidrogen dengan interaksi air dan karbon monoksida
hanya mungkin dalam persekitaran industri. Karbon dioksida dan hidrogen terbentuk, prinsip pemisahannya dijelaskan di atas.

Skop penjana hidrogen
H2 adalah pembawa tenaga moden yang digunakan secara aktif di banyak kawasan industri. Berikut adalah beberapa:
- pengeluaran hidrogen klorida (HC) l;
- pengeluaran bahan api untuk pelancar roket;
- pengeluaran ammonia;
- pemprosesan logam dan memotongnya;
- pengembangan baja untuk kotej musim panas;
- sintesis asid nitrik;
- penciptaan metil alkohol;
- industri Makanan;
- pengeluaran asid hidroklorik;
- penciptaan sistem lantai yang hangat.
Di samping itu, HHO telah menjadi sangat berguna dalam kehidupan seharian, walaupun dengan tempahan. Pertama sekali, ia digunakan untuk sistem pemanasan autonomi. Sebagai tambahan, gas Brown ditambahkan ke petrol dalam usaha untuk menipu mesin dan menjimatkan bahan bakar.
Kedua-dua kes tersebut mempunyai keunikan tersendiri. Oleh itu, semasa mengatur pemanasan rumah, perlu mengambil kira bahawa suhu pembakaran HHO adalah urutan magnitud yang lebih tinggi daripada metana. Sehubungan dengan itu, anda perlu membeli dandang khas yang mahal dengan muncung tahan panas. Jika tidak, pemilik dan rumahnya akan berada dalam bahaya besar.
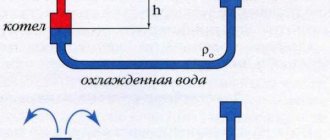
INVENSI MEMPUNYAI KELEBIHAN BERIKUT
Haba yang diperoleh dari pengoksidaan gas dapat digunakan secara langsung di lokasi, dan hidrogen dan oksigen diperoleh dari pembuangan wap sisa dan air proses.
Penggunaan air yang rendah semasa menjana elektrik dan haba.
Kesederhanaan cara.
Penjimatan tenaga yang ketara sebagai ia dibelanjakan hanya untuk memanaskan pemula kepada rejim terma yang telah ditetapkan.
Produktiviti proses yang tinggi, kerana pemisahan molekul air berlangsung sepersepuluh saat.
Kaedah letupan dan keselamatan kebakaran, kerana dalam pelaksanaannya, tidak perlu bekas untuk mengumpulkan hidrogen dan oksigen.
Semasa operasi pemasangan, air disucikan berulang kali, diubah menjadi air suling. Ini menghilangkan sedimen dan skala, yang meningkatkan jangka hayat pemasangan.
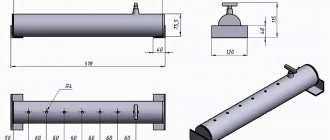
Pemasangannya diperbuat daripada keluli biasa; kecuali dandang yang diperbuat daripada keluli tahan panas dengan lapisan dan pelindung dindingnya. Maksudnya, tidak diperlukan bahan mahal khas.
Penemuan ini dapat digunakan di
industri dengan menggantikan hidrokarbon dan bahan bakar nuklear di loji janakuasa dengan air murah, meluas dan mesra alam, sambil mengekalkan kuasa loji ini.
Hidrogen di rumah: adakah faedahnya
Mari kita perhatikan sekarang: tidak menguntungkan menggunakan penjana hidrogen untuk pemanasan rumah. Anda akan menghabiskan lebih banyak tenaga elektrik menghasilkan H2 tulen daripada anda akan mendapat tenaga setelah membakarnya. Oleh itu, untuk 1 kW haba, 2 kW elektrik dibelanjakan, iaitu, tidak ada faedah. Lebih mudah memasang dandang elektrik di rumah.
Untuk menggantikan 1 liter petrol untuk sebuah kereta, anda memerlukan 4766 liter hidrogen tulen atau 7150 liter gas oksidrogen, 1/3 daripadanya adalah oksigen. Sejauh ini, bahkan akal terbaik di dunia belum mengembangkan unit yang mampu memberikan prestasi sedemikian.


TUNTUTAN
Kaedah untuk menghasilkan hidrogen dan oksigen dari wap air
, termasuk mengalirkan wap ini melalui medan elektrik, yang dicirikan kerana mereka menggunakan wap air yang terlalu panas dengan suhu
500 - 550 o C
, melalui medan elektrik arus terus voltan tinggi untuk mengasingkan wap dan memisahkannya menjadi atom hidrogen dan oksigen.
Saya sudah lama mahu melakukan perkara yang serupa. Tetapi percubaan lebih lanjut dengan bateri dan sepasang elektrod tidak tercapai. Saya ingin membuat alat lengkap untuk penghasilan hidrogen, dalam jumlah yang banyak untuk mengembang balon. Sebelum membuat alat lengkap untuk elektrolisis air di rumah, saya memutuskan untuk memeriksa semua yang ada pada model ini.
Skema umum elektrolisis kelihatan seperti ini.
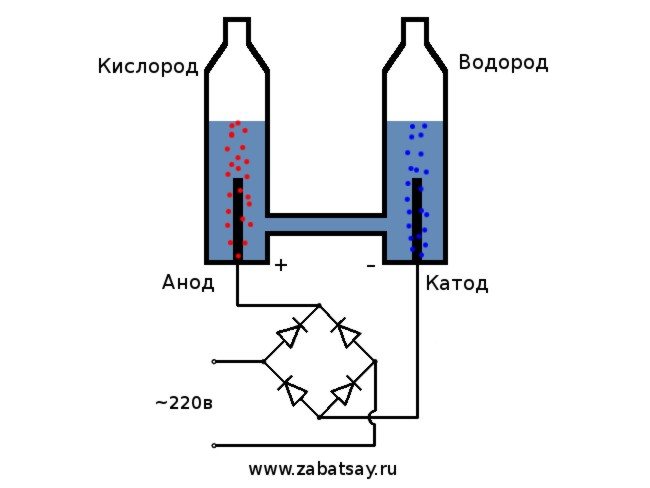

Model ini tidak sesuai untuk penggunaan seharian penuh. Tetapi kami berjaya menguji idea tersebut.
Oleh itu, saya memutuskan untuk menggunakan grafit untuk elektrod. Sumber grafit yang sangat baik untuk elektrod adalah pengumpul bas troli. Terdapat banyak dari mereka yang terbaring di penghentian akhir. Harus diingat bahawa salah satu elektrod akan runtuh.


Kami melihat dan mengubah suai dengan fail. Keamatan elektrolisis bergantung pada kekuatan arus dan luas elektrod.


Wayar dipasang pada elektrod. Wayar mesti dilindungi dengan teliti.


Botol plastik cukup sesuai untuk kes model elektrolisis. Lubang dibuat di penutup untuk paip dan wayar.


Semuanya dilapisi dengan baik dengan sealant.


Leher botol yang dipotong sesuai untuk menyambungkan dua bekas.


Mereka perlu disatukan dan jahitan mesti dicairkan.


Kacang dibuat dari penutup botol.


Lubang dibuat dalam dua botol di bahagian bawah. Segala-galanya dihubungkan dan diisi dengan teliti dengan sealant.


Kami akan menggunakan rangkaian isi rumah 220V sebagai sumber voltan. Saya ingin memberi amaran kepada anda bahawa ini adalah mainan yang agak berbahaya. Oleh itu, jika anda tidak mempunyai kemahiran yang mencukupi atau terdapat keraguan, maka lebih baik tidak mengulanginya.Di rangkaian isi rumah, kita mempunyai arus bolak-balik, untuk elektrolisis mesti diluruskan. Jambatan diod sangat sesuai untuk ini. Foto dalam gambar tidak cukup kuat dan cepat habis. Pilihan terbaik adalah jambatan diod MB156 Cina dalam kotak aluminium.


Jambatan diod menjadi sangat panas. Penyejukan aktif akan diperlukan. Penyejuk untuk pemproses komputer sangat sesuai. Kotak persimpangan dengan ukuran yang sesuai boleh digunakan untuk kandang. Dijual dalam barangan elektrik.


Beberapa lapisan kadbod mesti diletakkan di bawah jambatan dioda.


Lubang yang diperlukan dibuat di penutup kotak persimpangan.


Seperti inilah unit pemasangan. Electrolyzer dikuasakan dari sumber, kipas dikuasakan oleh sumber kuasa sejagat. Larutan baking soda digunakan sebagai elektrolit. Di sini mesti diingat bahawa semakin tinggi kepekatan larutan, semakin tinggi kadar tindak balasnya. Tetapi pada masa yang sama, pemanasan juga lebih tinggi. Lebih-lebih lagi, tindak balas penguraian natrium pada katod akan menyumbang kepada pemanasan. Tindak balas ini adalah eksotermik. Hasilnya, hidrogen dan natrium hidroksida akan terbentuk.


Peranti dalam foto di atas sangat panas. Ia mesti dimatikan secara berkala dan tunggu sehingga ia sejuk. Masalah pemanasan sebahagiannya diselesaikan dengan menyejukkan elektrolit. Untuk ini saya menggunakan pam pancut meja. Tiub panjang mengalir dari satu botol ke botol yang lain melalui pam dan baldi air sejuk.


Kesesuaian masalah ini hari ini cukup tinggi kerana hakikat bahawa penggunaan hidrogen sangat luas, dan dalam bentuk tulennya praktikalnya tidak terdapat di mana-mana alam. Itulah sebabnya mengapa beberapa teknik telah dikembangkan yang membolehkan pengekstrakan gas ini dari sebatian lain melalui tindak balas kimia dan fizikal. Perkara ini dibincangkan dalam artikel di atas.
Memperoleh hidrogen dan memeriksa kesuciannya
Hidrogen dapat diperoleh dengan bertindak balas asid zink dan hidroklorik.
Zn + 2HCl = ZnCl2 + H2 ↑
Zink mengalihkan hidrogen dari asid, seperti semua logam yang berada dalam rangkaian voltan di sebelah kiri hidrogen.
Untuk mengumpul hidrogen dalam tabung uji, anda perlu membalikkannya, kerana hidrogen lebih ringan daripada udara dan cenderung ke atas. Kaedah pengumpulan hidrogen ini disebut "kaedah perpindahan udara."
Rajah. 1. Mendapatkan hidrogen dan mengumpulkannya dengan anjakan udara
Tabung uji mengumpulkan hidrogen, tetapi juga mengandungi udara, dan oleh itu oksigen. Hidrogen dan oksigen adalah campuran yang boleh meletup. Kami menyalakan hidrogen yang terkumpul dengan serpihan. Tabung uji kecil dan letupan hidrogen dan oksigen hanyalah ledakan tajam. Semakin kurang oksigen dalam campuran, kapas lebih senyap.
Sekiranya hidrogen yang terkumpul di dalam tabung uji itu tulen, maka kita akan mendengar bunyi kusam. Hidrogen seperti itu boleh dinyalakan.
Pengeluaran hidrogen isi rumah
Pemilihan elektrolisis
Untuk mendapatkan elemen rumah, anda memerlukan alat khas - elektrolisis. Terdapat banyak pilihan untuk peralatan tersebut di pasaran, peranti ditawarkan oleh syarikat teknologi terkenal dan pengeluar kecil. Unit berjenama lebih mahal, tetapi kualiti binaannya lebih tinggi.
Perkakas rumah kecil dan senang digunakan. Perincian utamanya adalah:
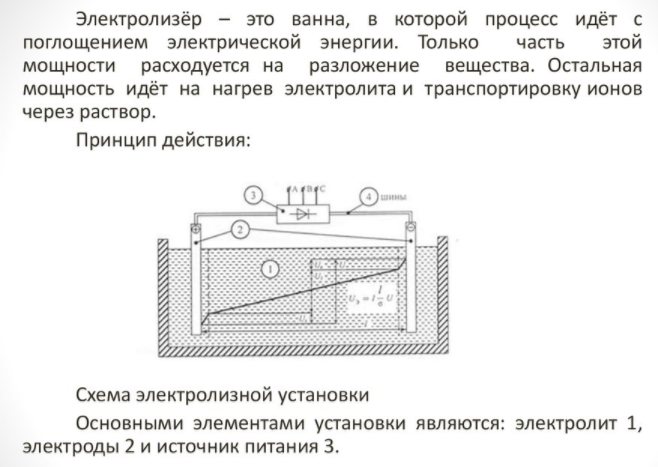

Electrolyzer - apa itu
- pembaharu;
- sistem pembersihan;
- sel bahan api;
- peralatan pemampat;
- bekas untuk menyimpan hidrogen.
Air paip sederhana diambil sebagai bahan mentah, dan elektrik datang dari saluran biasa. Unit berkuasa solar menjimatkan elektrik.
Hidrogen rumah digunakan dalam sistem pemanasan atau memasak. Dan juga memperkaya campuran bahan bakar-udara untuk meningkatkan kekuatan enjin kereta.
Membuat radas dengan tangan anda sendiri
Lebih murah untuk membuat peranti sendiri di rumah.Sel kering kelihatan seperti bekas tertutup, yang terdiri daripada dua plat elektrod dalam bekas dengan larutan elektrolit. World Wide Web menawarkan pelbagai skema pemasangan untuk peranti dengan model yang berbeza:
- dengan dua penapis;
- dengan susunan kontena atas atau bawah;
- dengan dua atau tiga injap;
- dengan papan tergalvani;
- pada elektrod.
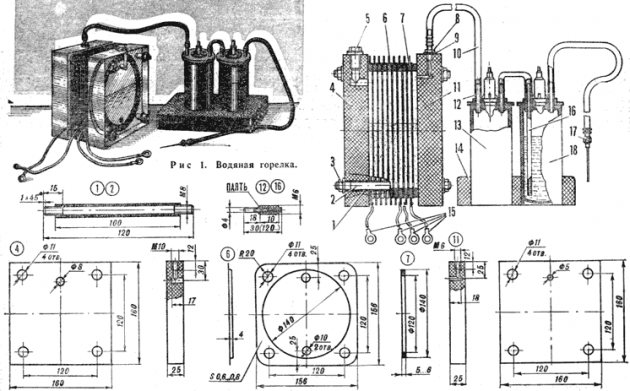

Gambarajah peranti elektrolisis
Alat mudah untuk menghasilkan hidrogen tidak sukar dibuat. Ia memerlukan:
- keluli tahan karat lembaran;
- tiub telus;
- kelengkapan;
- bekas plastik (1.5 l);
- penapis air dan injap tidak balik.
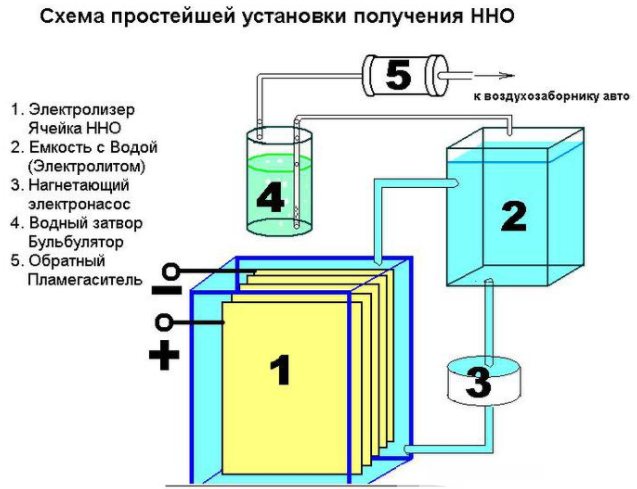

Peranti alat ringkas untuk menghasilkan hidrogen
Di samping itu, pelbagai perkakasan akan diperlukan: mur, mesin basuh, selak. Langkah pertama adalah memotong kepingan menjadi 16 petak persegi, memotong sudut dari masing-masing. Di sudut yang bertentangan daripadanya, diperlukan untuk menggerudi lubang untuk memasang plat. Untuk memastikan arus tetap, plat mesti disambungkan mengikut skema tambah - tolak - tambah - tolak. Bahagian-bahagian ini diasingkan antara satu sama lain dengan tiub, dan pada sambungan dengan selak dan pencuci (tiga keping di antara plat). 8 pinggan diletakkan di tambah dan tolak.
Apabila dipasang dengan betul, tulang rusuk plat tidak akan menyentuh elektrod. Bahagian yang dipasang diturunkan ke dalam bekas plastik. Pada titik di mana dinding menyentuh, dua lubang pemasangan dibuat dengan bolt. Pasang injap keselamatan untuk mengeluarkan lebihan gas. Kelengkapan dipasang di penutup bekas dan jahitannya ditutup dengan silikon.
Menguji radas
Untuk menguji peranti, lakukan beberapa tindakan:
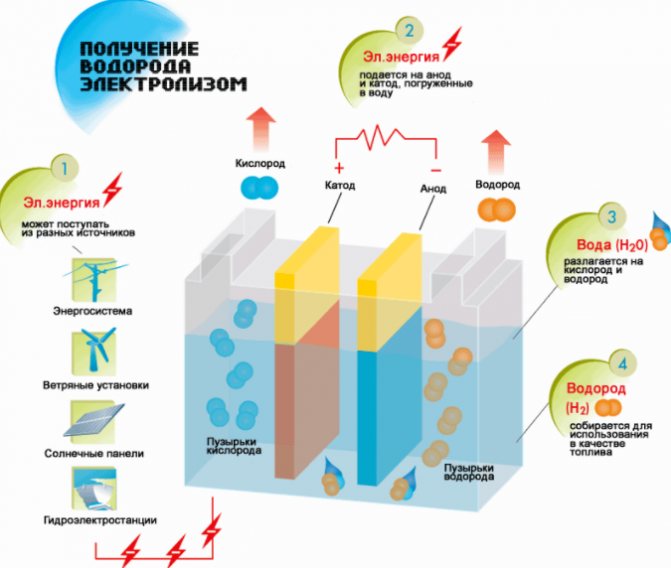

Skim pengeluaran hidrogen
- Isi dengan cecair.
- Tutup dengan penutup, sambungkan salah satu hujung tiub ke pemasangan.
- Yang kedua direndam dalam air.
- Sambungkan ke sumber kuasa.
Setelah menyambungkan peranti ke saluran keluar, setelah beberapa saat, proses dan pemendakan elektrolisis akan terasa.
Air tulen tidak mempunyai kekonduksian elektrik yang baik. Untuk meningkatkan penunjuk ini, anda perlu membuat penyelesaian elektrolitik dengan menambahkan alkali - natrium hidroksida. Ia terdapat dalam sebatian pembersih paip seperti tahi lalat.
Kaedah untuk menghasilkan hidrogen
Hidrogen adalah unsur gas tidak berwarna dan tidak berbau dengan ketumpatan 1/14 berbanding udara. Dalam keadaan bebas, jarang berlaku. Biasanya hidrogen digabungkan dengan unsur kimia lain: oksigen, karbon.
Pengeluaran hidrogen untuk keperluan industri dan kejuruteraan kuasa dilakukan dengan beberapa kaedah. Yang paling popular adalah:
- elektrolisis air;
- kaedah kepekatan;
- pemeluwapan suhu rendah;
- penjerapan.
Hidrogen dapat diasingkan bukan hanya dari sebatian gas atau air. Hidrogen dihasilkan dengan mengekspos kayu dan arang batu pada suhu tinggi, serta dengan memproses sisa buangan.
Hidrogen atom untuk kejuruteraan tenaga diperoleh menggunakan kaedah pemisahan termal bahan molekul pada wayar yang terbuat dari platinum, tungsten atau paladium. Ia dipanaskan dalam atmosfer hidrogen di bawah tekanan kurang dari 1,33 Pa. Dan juga unsur radioaktif digunakan untuk mendapatkan hidrogen.
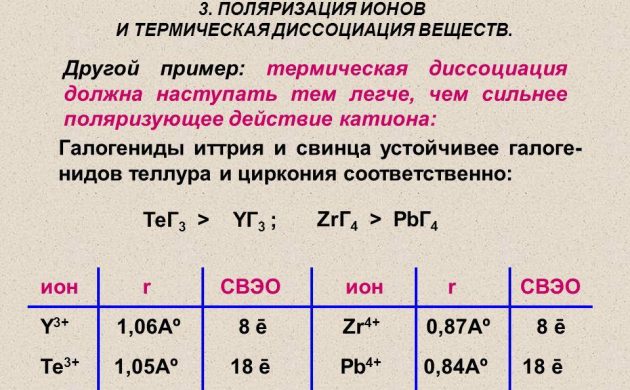

Pemisahan terma
Kaedah elektrolisis
Kaedah evolusi hidrogen yang paling mudah dan popular adalah elektrolisis air. Ia membolehkan pengeluaran hidrogen tulen. Kelebihan kaedah lain adalah:
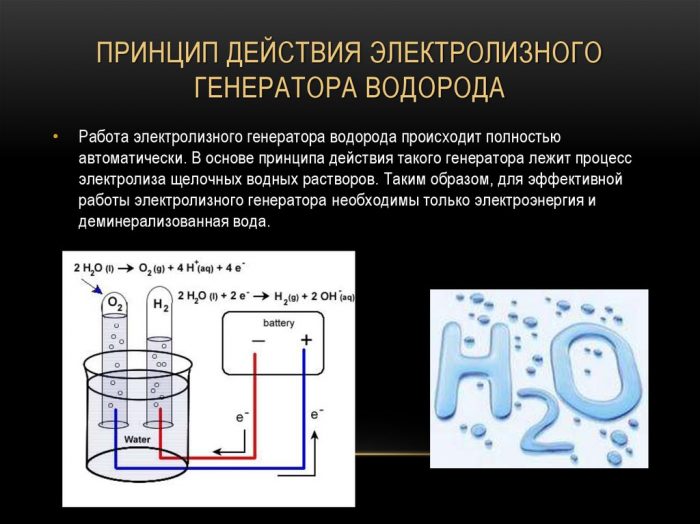

Prinsip operasi penjana hidrogen elektrolisis
- ketersediaan bahan mentah;
- menerima unsur di bawah tekanan;
- keupayaan untuk mengotomatisasi proses kerana kekurangan bahagian yang bergerak.
Prosedur untuk membelah cecair dengan elektrolisis adalah kebalikan dari pembakaran hidrogen. Intinya adalah bahawa di bawah pengaruh arus terus, oksigen dan hidrogen dilepaskan pada elektrod yang dicelupkan dalam larutan elektrolit berair.
Kelebihan tambahan dianggap sebagai pengeluaran produk sampingan dengan nilai industri.Oleh itu, sejumlah besar oksigen diperlukan untuk memangkin proses teknologi di sektor tenaga, membersihkan tanah dan badan air, dan membuang sampah isi rumah. Air berat yang diperoleh semasa elektrolisis digunakan dalam kejuruteraan tenaga di reaktor nuklear.
Pengeluaran hidrogen mengikut kepekatan
Kaedah ini didasarkan pada pemisahan unsur dari campuran gas yang mengandunginya. Jadi, bahagian terbesar bahan yang dihasilkan dalam jumlah industri diekstraksi menggunakan pembaharuan stim metana. Hidrogen yang diekstraksi dalam proses ini digunakan dalam tenaga, penyulingan minyak, industri pembuatan roket, dan juga untuk pengeluaran baja nitrogen. Proses mendapatkan H2 dilakukan dengan cara yang berbeza:
- kitaran pendek;
- kriogenik;
- membran.
Kaedah terakhir dianggap paling berkesan dan lebih murah.
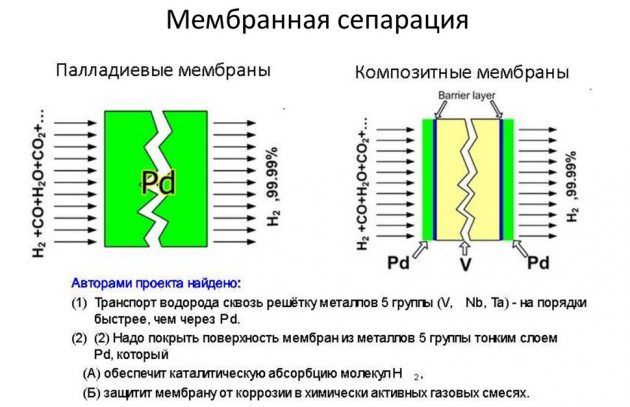

Pemeluwapan suhu rendah
Kaedah mendapatkan H2 ini terdiri daripada penyejukan kuat sebatian gas di bawah tekanan. Akibatnya, mereka diubah menjadi sistem dua fasa, yang kemudian dipisahkan oleh pemisah menjadi komponen cair dan gas. Media cecair digunakan untuk penyejukan:
- air;
- etana cair atau propana;
- ammonia cecair.


Prosedur ini tidak semudah yang didengar. Tidak mustahil untuk memisahkan gas hidrokarbon secara serentak. Sebilangan komponen akan keluar dengan gas yang diambil dari ruang pemisah, yang tidak menjimatkan. Masalahnya dapat diselesaikan dengan penyejukan bahan mentah sebelum dipisahkan. Tetapi ini memerlukan banyak tenaga.
Di dalam sistem kondensor suhu rendah moden, tiang demethanization atau deethanization juga disediakan. Fasa gas dikeluarkan dari tahap pemisahan terakhir, dan cecair dihantar ke ruang pembetulan dengan aliran gas mentah setelah pertukaran haba.
Kaedah penjerapan
Semasa penjerapan, untuk melepaskan hidrogen, penyerap digunakan - pepejal yang menyerap komponen yang diperlukan dari campuran gas. Karbon aktif, gel silikat, zeolit digunakan sebagai penjerap. Untuk menjalankan proses ini, alat khas digunakan - penyerap siklik atau penyaring molekul. Apabila dilaksanakan di bawah tekanan, kaedah ini dapat memulihkan 85% hidrogen.
Sekiranya kita membandingkan penjerapan dengan pemeluwapan suhu rendah, kita dapat melihat kos bahan dan operasi proses yang lebih rendah - rata-rata, sebanyak 30 peratus. Hidrogen dihasilkan oleh penjerapan untuk kejuruteraan tenaga dan dengan penggunaan pelarut. Kaedah ini membolehkan pengekstrakan 90 peratus H2 dari campuran gas dan mendapatkan produk akhir dengan kepekatan hidrogen hingga 99.9%.