Metoder för att producera väte under industriella förhållanden
Extraktion genom metanomvandling
... Vatten i ångform, förvärmt till 1000 grader Celsius, blandas med metan under tryck och i närvaro av en katalysator. Denna metod är intressant och beprövad. Det bör också noteras att den ständigt förbättras: sökandet efter nya katalysatorer, billigare och effektivare, pågår.
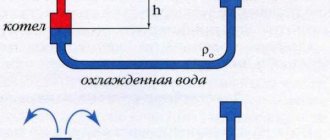
Tänk på den äldsta metoden för att producera väte - kolförgasning
... I avsaknad av luftåtkomst och en temperatur på 1300 grader Celsius värms kol och vattenånga. Således förflyttas väte från vatten och koldioxid erhålls (väte kommer uppe, koldioxid, också erhållet som ett resultat av reaktionen, är längst ner). Detta kommer att vara separationen av gasblandningen, allt är väldigt enkelt.
Skaffa väte med elektrolys av vatten
anses vara det enklaste alternativet. För dess genomförande är det nödvändigt att hälla en sodalösning i behållaren och också placera två elektriska element där. En kommer att laddas positivt (anod) och den andra negativt (katod). När ström appliceras kommer väte att gå till katoden och syre till anoden.
Att erhålla väte enligt metoden partiell oxidation
... För detta används en legering av aluminium och gallium. Det placeras i vatten, vilket leder till bildandet av väte och aluminiumoxid under reaktionen. Gallium är nödvändigt för att reaktionen ska kunna ske fullständigt (detta element förhindrar att aluminium oxiderar i förtid).
Nyligen förvärvad relevans metod för användning av bioteknik
: under förutsättning av syre- och svavelbrist, börjar klamydomonas att släppa väte intensivt. En mycket intressant effekt som nu studeras aktivt.

Glöm inte en annan gammal, beprövad metod för väteproduktion, som består i att använda olika alkaliska element
och vatten. I princip är denna teknik möjlig i laboratorium med nödvändiga säkerhetsåtgärder på plats. Således bildas en metalloxid och väte under reaktionens gång (det fortsätter med upphettning och med katalysatorer). Det återstår bara att samla in det.
Få väte förbi växelverkan mellan vatten och kolmonoxid
endast möjligt i en industriell miljö. Koldioxid och väte bildas, principen om deras separation beskrivs ovan.

Omfattningen av vätgeneratorn
H2 är en modern energibärare som används aktivt i många industriområden. Här är några:
- produktion av klorväte (HC) l;
- produktion av bränsle för raketkastare;
- produktion av ammoniak;
- bearbetning och skärning av metall;
- utveckling av gödselmedel för sommarstugor;
- syntes av salpetersyra;
- skapandet av metylalkohol;
- livsmedelsindustrin;
- saltsyraproduktion;
- skapande av varma golvsystem.
Dessutom har HHO blivit mycket användbart i vardagen, om än med reservationer. Först och främst används den för autonoma värmesystem. Dessutom tillsätts Browns gas till bensin i ett försök att lura motorn och spara på bränsle.
Båda fallen har sina egna särdrag. Så när du organiserar uppvärmning av hemmet måste du ta hänsyn till att förbränningstemperaturen för HHO är en storleksordning högre än för metan. I detta avseende är det nödvändigt att köpa en speciell, dyr panna med ett värmebeständigt munstycke. Annars kommer ägaren och hans hem att vara i betydande fara.
UPPFINNINGEN HAR FÖLJANDE FÖRDELAR
Värmen som erhålls från oxidationen av gaser kan användas direkt på plats och väte och syre erhålls genom bortskaffande av ånga och processvatten.
Låg vattenförbrukning vid generering av el och värme.
Enkelheten i vägen.
Betydande energibesparingar som den spenderas bara på att värma upp startmotorn till det etablerade termiska systemet.
Hög produktivitet i processen, eftersom dissociation av vattenmolekyler varar tiondelar av en sekund.
Explosion och brandsäkerhet av metoden, eftersom i dess genomförande finns det inget behov av behållare för uppsamling av väte och syre.
Under installationens drift renas vatten upprepade gånger och omvandlas till destillerat vatten. Detta eliminerar sediment och kalk, vilket ökar installationens livslängd.
Installationen är gjord av vanligt stål; förutom pannor av värmebeständigt stål med foder och avskärmning av väggarna. Det vill säga inga speciella dyra material krävs.
Uppfinningen kan användas i
industri genom att ersätta kolväte och kärnbränsle i kraftverk med billigt, utbrett och miljövänligt vatten, samtidigt som kraften i dessa anläggningar bibehålls.
Väte hemma: finns det en fördel
Vi noterar direkt: det är olönsamt att använda en vätgenerator för att värma ett hus. Du kommer att spendera mer el på att producera ren H2 än att du får energi efter att ha bränt den. Så för 1 kW värme spenderas 2 kW el, det vill säga det finns ingen fördel. Det är lättare att installera någon av de elektriska pannorna hemma.
För att ersätta 1 liter bensin till en bil behöver du 4766 liter rent väte eller 7150 liter oxivätegas, varav 1/3 är syre. Hittills har även de bästa hjärnorna i världen inte utvecklat en enhet som kan leverera sådan prestanda.


KRAV
Metod för att producera väte och syre från vattenånga
, inklusive att leda denna ånga genom ett elektriskt fält, kännetecknat av att de använder överhettad vattenånga med en temperatur
500 - 550 ° C
, passerat genom ett högspänningsriktigt elektriskt fält för att dissociera ånga och separera den i väte- och syreatomer.
Jag har länge velat göra en liknande sak. Men ytterligare experiment med ett batteri och ett par elektroder nådde inte. Jag ville skapa en fullfjädrad apparat för produktion av väte, i mängder för att blåsa upp en ballong. Innan jag gjorde en fullfjädrad apparat för elektrolys av vatten hemma bestämde jag mig för att kontrollera allt på modellen.
Elektrolysatorns allmänna system ser ut så här.
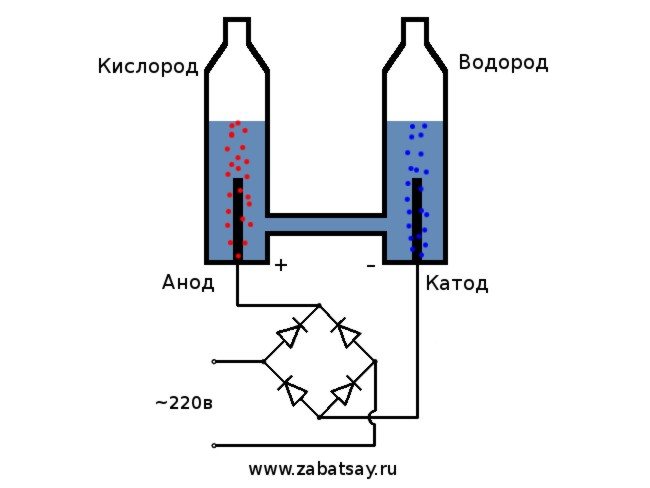

Denna modell är inte lämplig för full daglig användning. Men vi lyckades testa idén.
Så jag bestämde mig för att använda grafit för elektroderna. En utmärkt grafitkälla för elektroder är vagnbussuppsamlaren. Det finns gott om dem som ligger vid slutstationerna. Man måste komma ihåg att en av elektroderna kommer att kollapsa.


Vi såg och slutförde med en fil. Intensiteten hos elektrolysen beror på strömstyrkan och elektrodernas yta.


Ledningar är fästa vid elektroderna. Ledningarna måste vara noggrant isolerade.


För den elektrolytiska cellmodellen är plastflaskor ganska lämpliga. Hål är gjorda i locket för rör och ledningar.


Allt är grundligt belagt med tätningsmedel.


Avskurna flaskhalsar är lämpliga för anslutning av två behållare.


De måste sammanfogas och sömmen måste smältas.


Nötterna är gjorda av flasklock.


Hålen är gjorda i två flaskor längst ner. Allt är anslutet och fylls noggrant med tätningsmedel.


Vi kommer att använda ett 220V hushållsnätverk som spänningskälla. Jag vill varna dig för att det här är en ganska farlig leksak. Så om du inte har tillräckliga färdigheter eller det finns tvivel är det bättre att inte upprepa.I hushållsnätverket har vi en växelström, för elektrolys måste den rätas ut. En diodbro är perfekt för detta. Den på bilden var inte tillräckligt kraftfull och brann snabbt ut. Det bästa alternativet var den kinesiska MB156-diodbryggan i ett aluminiumfodral.


Diodbryggan blir väldigt varm. Aktiv kylning krävs. En kylare för en datorprocessor är perfekt. En kopplingsdosa av lämplig storlek kan användas för inneslutningen. Säljs i elektriska varor.


Flera lager kartong måste placeras under diodbryggan.


De nödvändiga hålen görs i locket på kopplingsboxen.


Så här ser den monterade enheten ut. Elektrolysatorn drivs från elnätet, fläkten drivs av en universell strömkälla. En bakpulverlösning används som elektrolyt. Här måste man komma ihåg att ju högre koncentrationen av lösningen, desto högre reaktionshastighet. Men samtidigt är uppvärmningen också högre. Dessutom kommer reaktionen av natriumnedbrytning vid katoden att bidra till uppvärmningen. Denna reaktion är exoterm. Som ett resultat bildas väte och natriumhydroxid.


Enheten på bilden ovan var väldigt het. Det måste stängas av regelbundet och vänta tills det svalnar. Uppvärmningsproblemet löstes delvis genom kylning av elektrolyten. För detta använde jag en bordsbrunnspump. Ett långt rör går från en flaska till en annan genom en pump och en hink med kallt vatten.


Relevansen av denna fråga idag är ganska hög på grund av att vätesfären är extremt omfattande och i sin rena form finns den praktiskt taget inte någonstans i naturen. Därför har flera tekniker utvecklats som möjliggör extraktion av denna gas från andra föreningar genom kemiska och fysiska reaktioner. Detta diskuteras i artikeln ovan.
Skaffa väte och kontrollera det för renhet
Väte kan erhållas genom att reagera zink och saltsyra.
Zn + 2HCl = ZnCl2 + H2
Zink förskjuter väte från syror, som alla metaller som står i spänningsserien till vänster om väte.
För att samla väte i ett provrör, vänd det upp och ner, eftersom väte är lättare än luft och tenderar uppåt. Denna metod för att samla väte kallas "luftförskjutningsmetoden".
Fikon. 1. Skaffa väte och samla upp det genom luftförskjutning
Provröret ackumulerar väte, men det innehåller också luft och därmed syre. Väte och syre är explosiva blandningar. Vi tänder det uppsamlade vätet med en splinter. Provröret är litet och explosionen av väte och syre är bara en skarp smäll. Ju mindre syre i blandningen, desto tystare är bomullen.
Om vätet som samlas upp i provröret är rent, hör vi en tråkig pop. Sådant väte kan antändas.
Hushållens vätgasproduktion
Val av elektrolysator
För att få ett huselement behöver du en speciell apparat - en elektrolysator. Det finns många alternativ för sådan utrustning på marknaden; enheterna erbjuds av både välkända teknikföretag och små tillverkare. Märkesenheter är dyrare, men byggkvaliteten är högre.
Hushållsapparaten är liten och enkel att använda. Dess viktigaste detaljer är:

Elektrolysator - vad är det?
- reformator;
- rengöringssystem;
- bränsleceller;
- kompressorutrustning;
- en behållare för lagring av väte.
Enkelt kranvatten tas som råvara och el kommer från ett vanligt utlopp. Solenergidrivna enheter sparar på el.
Hemväte används i värme- eller matlagningssystem. Och även de berikar bränsle-luftblandningen för att öka kraften i bilens motorer.
Skapa en apparat med egna händer
Det är ännu billigare att göra enheten själv hemma.En torr cell ser ut som en förseglad behållare, som består av två elektrodplattor i en behållare med en elektrolytisk lösning. World Wide Web erbjuder en mängd olika monteringsscheman för enheter av olika modeller:
- med två filter;
- med topp- eller bottenarrangemang av behållaren;
- med två eller tre ventiler;
- med galvaniserad bräda;
- på elektroderna.
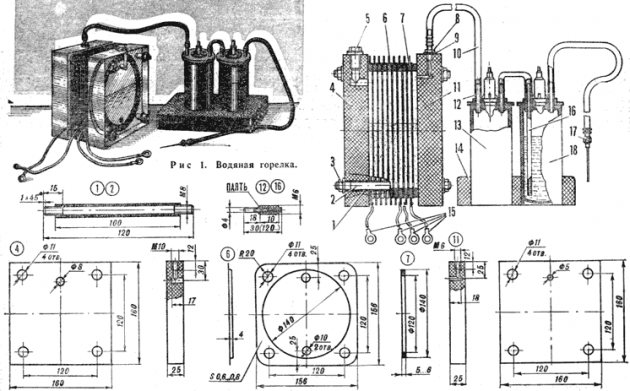

Elektrolysenhetsdiagram
Det är inte svårt att skapa en enkel anordning för att producera väte. Det kommer att kräva:
- plåt rostfritt stål;
- transparent rör;
- beslag;
- plastbehållare (1,5 l);
- vattenfilter och backventil.
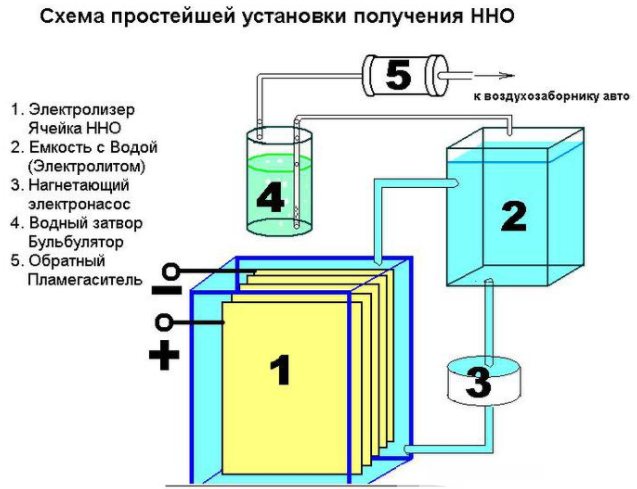

Anordningen för en enkel anordning för att producera väte
Dessutom kommer olika hårdvaror att behövas: muttrar, brickor, bultar. Det första steget är att skära arket i 16 kvadratiska fack, klippa ett hörn från var och en av dem. I det motsatta hörnet från det måste du borra ett hål för att bulta plattorna. För att säkerställa konstant ström måste plattorna anslutas enligt schema plus - minus - plus - minus. Dessa delar är isolerade från varandra med ett rör och vid anslutningen med en bult och brickor (tre delar mellan plattorna). 8 plattor placeras på plus och minus.
När de är korrekt monterade kommer plattorna inte att röra elektroderna. De monterade delarna sänks ner i en plastbehållare. Vid den punkt där väggarna berörs är två monteringshål gjorda med bultar. Installera en säkerhetsventil för att avlägsna överflödig gas. Beslag monteras i behållarlocket och sömmarna tätas med silikon.
Testa apparaten
För att testa enheten, utför flera åtgärder:
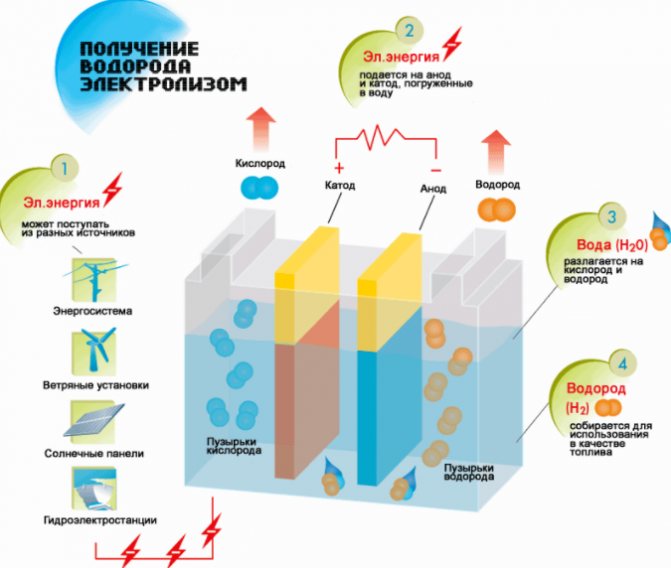

Väteproduktionssystem
- Fyll på med vätska.
- Täck med lock, anslut ena änden av röret till kopplingen.
- Den andra är nedsänkt i vatten.
- Anslut till en strömkälla.
Efter att ha anslutit enheten till ett uttag märks elektrolysprocessen och utfällningen efter några sekunder.
Rent vatten har inte god elektrisk ledningsförmåga. För att förbättra denna indikator måste du skapa en elektrolytisk lösning genom att tillsätta en alkalinatriumhydroxid. Det finns i rörrengöringsföreningar som Mole.
Metoder för att producera väte
Väte är ett färglöst och luktfritt gasformigt element med en densitet på 1/14 i förhållande till luft. I ett fritt tillstånd är det sällsynt. Vanligtvis kombineras väte med andra kemiska element: syre, kol.
Väteproduktion för industriella behov och kraftteknik utförs med flera metoder. De mest populära är:
- elektrolys av vatten;
- koncentrationsmetod;
- låg temperatur kondens;
- adsorption.
Väte kan isoleras inte bara från gasformiga eller vattenföreningar. Väte produceras genom att trä och kol utsätts för höga temperaturer samt genom bearbetning av bioavfall.
Atomiskt väte för kraftteknik erhålls med metoden för termisk dissociation av en molekylär substans på en tråd gjord av platina, volfram eller palladium. Den värms upp i en väteatmosfär under ett tryck mindre än 1,33 Pa. Och även radioaktiva element används för att erhålla väte.
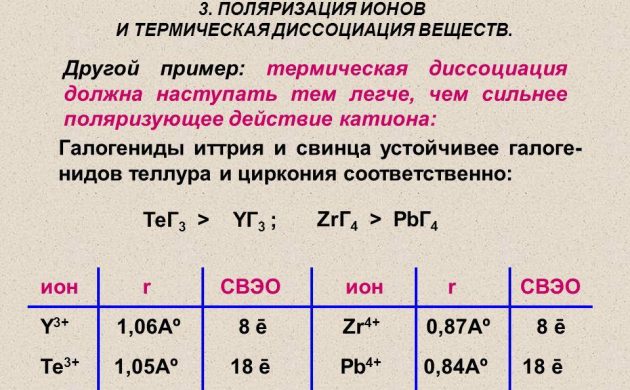

Termisk dissociation
Elektrolysmetod
Den enklaste och mest populära metoden för väteutveckling är vattenelektrolys. Det möjliggör produktion av praktiskt taget rent väte. Andra fördelar med denna metod beaktas:
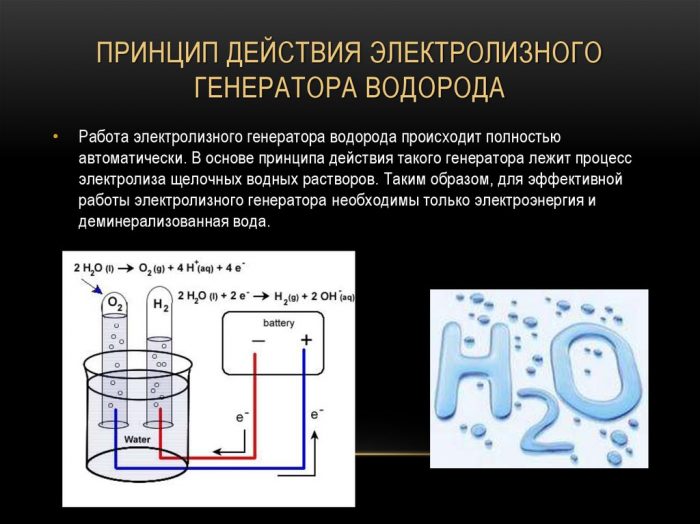

Principen för drift av elektrolysvätegeneratorn
- tillgången på råvaror;
- mottagande av ett element under tryck;
- förmågan att automatisera processen på grund av bristen på rörliga delar.
Proceduren för klyvning av en vätska genom elektrolys är omvänd förbränning av väte. Dess väsen är att under påverkan av likström frigörs syre och väte på elektroderna doppade i en vattenhaltig elektrolytlösning.
En ytterligare fördel anses vara produktion av biprodukter med industriellt värde.Således behövs en stor mängd syre för att katalysera tekniska processer inom energisektorn, rensa mark och vatten och avyttra hushållsavfall. Tungvatten som erhållits under elektrolys används i kraftteknik i kärnreaktorer.
Väteproduktion efter koncentration
Denna metod baseras på separationen av ett element från gasblandningar som innehåller det. Således extraheras den största delen av det industriellt producerade ämnet med ångreformering av metan. Väte som utvinns i denna process används inom energi, oljeraffinering, raketbyggande industrier samt för produktion av kvävegödselmedel. Processen för att erhålla H2 utförs på olika sätt:
- kort cykel;
- kryogen;
- membran.
Den senare metoden anses vara den mest effektiva och billigare.
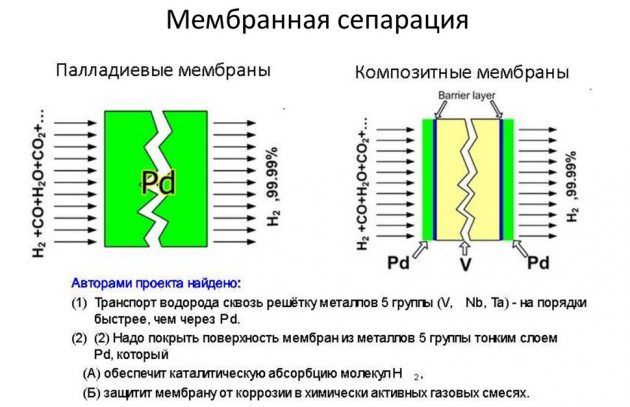

Kondens vid låg temperatur
Denna metod för att erhålla H2 består i stark kylning av gasformiga föreningar under tryck. Som ett resultat omvandlas de till ett tvåfassystem som sedan separeras av en separator till en flytande komponent och en gas. Flytande media används för kylning:
- vatten;
- flytande etan eller propan;
- flytande ammoniak.


Denna procedur är inte så lätt som det låter. Det kommer inte att vara möjligt att rent separera kolvätegaser på en gång. Några av komponenterna kommer att lämnas med gas som tas från separationsfacket, vilket inte är ekonomiskt. Problemet kan lösas genom djupkylning av råvaran före separering. Men detta kräver mycket energi.
I moderna lågtemperaturkondensorsystem finns dessutom avmetaniserings- eller avetaniseringskolonner. Gasfasen avlägsnas från det sista separationssteget och vätskan skickas till destillationskolonnen med en ström av rågas efter värmeväxling.
Adsorptionsmetod
Under adsorption, för att frigöra väte, används adsorbenter - fasta ämnen som absorberar de nödvändiga komponenterna i gasblandningen. Aktivt kol, silikatgel, zeoliter används som adsorbenter. För att utföra denna process används speciella anordningar - cykliska adsorberare eller molekylsiktar. När den implementeras under tryck kan denna metod återvinna 85 procent väte.
Om vi jämför adsorption med kondensation vid låg temperatur kan vi notera en lägre material- och driftskostnad för processen - i genomsnitt 30 procent. Väte produceras genom adsorption för kraftteknik och med användning av lösningsmedel. Denna metod gör det möjligt att extrahera 90 procent H2 från gasblandningen och erhålla slutprodukten med en vätekoncentration på upp till 99,9%.