Ổn định hóa học
Xem xét các tính chất hóa học của xăng, cần phải tập trung vào việc thành phần của hydrocacbon sẽ không thay đổi trong bao lâu, vì khi bảo quản lâu, các thành phần nhẹ hơn biến mất và hiệu suất giảm đáng kể.
Đặc biệt, vấn đề là nghiêm trọng nếu nhiên liệu cấp cao hơn (AI 95) được lấy từ xăng có trị số octan tối thiểu bằng cách thêm propan hoặc metan vào thành phần của nó. Đặc tính chống kích nổ của chúng cao hơn isooctan, nhưng chúng cũng tiêu tan ngay lập tức.
Theo GOST, thành phần hóa học của nhiên liệu của bất kỳ nhãn hiệu nào phải không thay đổi trong 5 năm, tuân theo các quy tắc bảo quản. Nhưng trên thực tế, thường ngay cả nhiên liệu mới mua cũng đã có trị số octan thấp hơn mức quy định.
Những người bán hàng vô đạo đức sẽ bị đổ lỗi cho điều này, những người đã thêm khí đốt hóa lỏng vào các thùng chứa nhiên liệu, thời gian lưu trữ đã hết và hàm lượng không đáp ứng các yêu cầu của GOST. Thông thường, các lượng khí khác nhau được thêm vào cùng một loại nhiên liệu để có trị số octan là 92 hoặc 95. Xác nhận của các thủ thuật đó là mùi hăng của khí tại trạm nạp.
Phương pháp xác định điểm chớp cháy
Có phương pháp đóng mở nồi nấu (thùng chứa các sản phẩm dầu). Nhiệt độ thu được khác nhau do lượng hơi tích lũy.
Phương pháp nấu chảy mở bao gồm:
- Làm sạch xăng khỏi độ ẩm bằng cách sử dụng natri clorua.
- Đổ đầy chén nung đến một mức nhất định.
- Làm nóng thùng chứa đến nhiệt độ thấp hơn 10 độ so với kết quả mong đợi.
- Đánh lửa của một đầu đốt gas trên bề mặt.
- Tại thời điểm đánh lửa, điểm chớp cháy được ghi lại.
Phương pháp nấu chảy kín khác ở chỗ xăng trong bình chứa được trộn liên tục. Khi mở nắp, ngọn lửa tự động bốc lên.
Thiết bị điểm chớp cháy bao gồm các thành phần sau:
- lò sưởi điện (công suất từ 600 watt);
- dung tích 70 ml;
- máy khuấy đồng;
- bộ đánh lửa điện hoặc gas;
- nhiệt kế.
Tùy thuộc vào kết quả, các chất dễ cháy được phân loại:
- đặc biệt nguy hiểm (ở điểm chớp cháy dưới -200C);
- nguy hiểm (từ -200C đến + 230C);
- nguy hiểm ở nhiệt độ cao (từ 230C đến 610C).
Tốc độ - Đốt cháy - Nhiên liệu
Chi phí thực của 1 lít xăng là bao nhiêu
Tốc độ đốt cháy nhiên liệu tăng lên rất nhiều nếu hỗn hợp cháy chuyển động xoáy mạnh (hỗn loạn). Theo đó, cường độ truyền nhiệt hỗn loạn có thể cao hơn nhiều so với cường độ khuếch tán phân tử.
Tốc độ đốt cháy của nhiên liệu phụ thuộc vào một số lý do được thảo luận ở phần sau của chương này và đặc biệt, vào chất lượng của sự hòa trộn nhiên liệu với không khí. Tốc độ đốt cháy nhiên liệu được xác định bằng lượng nhiên liệu đốt trong một đơn vị thời gian.
Tốc độ đốt cháy nhiên liệu và do đó, tốc độ tỏa nhiệt được xác định bởi kích thước của bề mặt đốt. Bụi than có kích thước hạt tối đa 300 - 500 micron có bề mặt đốt lớn hơn hàng chục nghìn lần so với nhiên liệu ghi xích đã phân loại thô.
Tốc độ đốt cháy nhiên liệu phụ thuộc vào nhiệt độ và áp suất trong buồng đốt, tăng dần khi chúng tăng lên. Do đó, sau khi đánh lửa, tốc độ cháy tăng lên và trở nên rất cao ở cuối buồng đốt.
Tốc độ đốt cháy nhiên liệu cũng chịu ảnh hưởng của tốc độ động cơ. Với sự gia tăng số vòng quay, thời gian của giai đoạn được giảm xuống.
Sự hỗn loạn của dòng khí làm tăng mạnh tốc độ đốt cháy nhiên liệu do tăng diện tích bề mặt đốt và tốc độ lan truyền của mặt trước ngọn lửa với tốc độ truyền nhiệt tăng.
Khi vận hành trên hỗn hợp nạc, tốc độ đốt cháy nhiên liệu bị chậm lại. Do đó, nhiệt lượng do khí tỏa ra đến các bộ phận tăng lên và động cơ quá nóng. Dấu hiệu của hỗn hợp quá nạc là nhấp nháy ở bộ chế hòa khí và ống nạp.
Sự hỗn loạn của dòng khí làm tăng mạnh tốc độ đốt cháy nhiên liệu do tăng diện tích bề mặt đốt và tốc độ lan truyền mặt trước ngọn lửa do tăng tốc độ truyền nhiệt.
Các ankan bình thường có số cetan lớn nhất, đặc trưng cho tốc độ đốt cháy nhiên liệu trong động cơ.
Thành phần của hỗn hợp làm việc ảnh hưởng rất lớn đến tốc độ đốt cháy nhiên liệu trong động cơ. Các điều kiện này diễn ra ở hệ số.
Ảnh hưởng của chất lượng đến sự phát triển của quá trình cháy được xác định bởi tốc độ đốt cháy nhiên liệu trong pha chính. Khi đốt cháy một lượng lớn nhiên liệu trong giai đoạn này, giá trị pz và Tz tăng lên, tỷ trọng của nhiên liệu sau đốt giảm trong quá trình giãn nở, và chỉ số polytrope nz càng lớn. Sự phát triển của quá trình này là thuận lợi nhất, vì đạt được việc sử dụng nhiệt tốt nhất.
Trong quá trình làm việc của động cơ, trị số của tốc độ đốt cháy nhiên liệu rất quan trọng. Tốc độ cháy được hiểu là lượng (khối lượng) nhiên liệu phản ứng (đốt cháy) trên một đơn vị thời gian.
Một số hiện tượng chung cho thấy tốc độ đốt cháy nhiên liệu trong động cơ là khá tự nhiên, không phải ngẫu nhiên. Điều này được chỉ ra bởi khả năng tái tạo của các chu kỳ rõ ràng hơn hoặc ít hơn trong xi lanh động cơ, trên thực tế, quyết định hoạt động ổn định của động cơ. Trong các động cơ tương tự, bản chất kéo dài của quá trình đốt cháy luôn được quan sát với các hỗn hợp nhỏ. Theo quy luật, sự làm việc nặng nhọc của động cơ, xảy ra với tốc độ phản ứng cháy cao, được quan sát thấy, như một quy luật, ở động cơ diesel không máy nén và làm việc mềm - ở động cơ đánh lửa từ tia lửa điện. Điều này cho thấy rằng sự hình thành hỗn hợp và đánh lửa khác nhau về cơ bản gây ra sự thay đổi thường xuyên trong tốc độ cháy. Khi tốc độ động cơ tăng lên, thời gian cháy giảm theo thời gian, và góc quay của trục khuỷu tăng lên. Đường cong động học của quá trình đốt cháy trong động cơ có bản chất tương tự như đường cong động học của một số phản ứng hóa học không liên quan trực tiếp đến động cơ và xảy ra trong các điều kiện khác nhau.
Thí nghiệm cho biết sự phụ thuộc của cường độ truyền nhiệt bức xạ vào tốc độ đốt cháy nhiên liệu. Với quá trình đốt cháy nhanh chóng ở gốc ngọn đuốc, nhiệt độ cao hơn phát triển và truyền nhiệt tăng cường. Sự không đồng nhất của trường nhiệt độ, cùng với các nồng độ khác nhau của các hạt phát xạ, dẫn đến sự không đồng nhất về mức độ đen của ngọn lửa. Tất cả những điều trên gây khó khăn lớn cho việc phân tích xác định nhiệt độ của bộ tản nhiệt và mức độ phát xạ của lò.
Với ngọn lửa tầng (xem Phần 3 để biết thêm chi tiết), tốc độ đốt cháy nhiên liệu là không đổi và Q 0; quá trình cháy là im lặng. Tuy nhiên, nếu vùng cháy hỗn loạn và đây là trường hợp đang được xem xét, thì ngay cả khi mức tiêu thụ nhiên liệu trung bình không đổi, tốc độ đốt cháy cục bộ thay đổi theo thời gian và đối với phần tử có khối lượng nhỏ Q.Q. Sự hỗn loạn liên tục làm xáo trộn ngọn lửa; tại bất kỳ thời điểm nào, sự cháy bị giới hạn bởi ngọn lửa này hoặc một loạt các ngọn lửa chiếm một vị trí ngẫu nhiên trong vùng cháy.
Nhiên liệu khí
Nhiên liệu khí là hỗn hợp của nhiều loại khí khác nhau: mêtan, ethylene và các hydrocacbon khác, carbon monoxide, carbon dioxide hoặc carbon dioxide, nitơ, hydro, hydro sunfua, oxy và các khí khác, cũng như hơi nước.
Mêtan (CH4) là thành phần chính của nhiều loại khí tự nhiên. Hàm lượng của nó trong khí tự nhiên đạt 93 ... 98%. Đốt cháy 1 m3 khí metan giải phóng ~ 35 800 kJ nhiệt.
Nhiên liệu khí cũng có thể chứa một lượng nhỏ ethylene (C2H4). Đốt cháy 1 m3 etylen sinh ra nhiệt lượng ~ 59.000 kJ.
Ngoài metan và etylen, nhiên liệu khí còn chứa các hợp chất hydrocacbon, chẳng hạn như propan (C3H8), butan (C4H10), v.v ... Quá trình đốt cháy các hydrocacbon này tạo ra nhiều nhiệt hơn quá trình đốt cháy etylen, nhưng lượng của chúng không đáng kể trong các khí dễ cháy. .
Hiđro (H2) nhẹ hơn không khí 14,5 lần. Quá trình đốt cháy 1 m3 hydro giải phóng nhiệt lượng ~ 10 800 kJ. Nhiều loại khí dễ cháy, trừ khí lò cốc, chứa một lượng tương đối nhỏ hydro. Trong khí lò cốc, hàm lượng của nó có thể đạt 50 ... 60%.
Carbon monoxide (CO) là thành phần dễ cháy chính của khí lò cao. Quá trình đốt cháy 1 m3 khí này tạo ra nhiệt lượng ~ 12.770 kJ. Khí này không màu, không mùi và có độc tính cao.
Hydrogen sulfide (H2S) là một chất khí nặng, có mùi khó chịu và rất độc. Khi có hydro sunfua trong khí, sự ăn mòn các bộ phận kim loại của lò và đường ống dẫn khí sẽ tăng lên. Tác hại của hydrogen sulfide được tăng cường bởi sự hiện diện của oxy và độ ẩm trong khí. Đốt cháy 1 m3 hydro sunfua giải phóng nhiệt lượng ~ 23 400 kJ.
Phần còn lại của các khí: CO2, N2, O2 và hơi nước là các thành phần dằn, vì khi tăng hàm lượng các khí này trong nhiên liệu, hàm lượng các thành phần dễ cháy của nó sẽ giảm. Sự hiện diện của chúng dẫn đến giảm nhiệt độ cháy của nhiên liệu. Hàm lượng oxy tự do> 0,5% trong nhiên liệu khí được coi là nguy hiểm vì lý do an toàn.
Sôi - xăng
Số Octan Thành phần xăng
Xăng bắt đầu sôi ở nhiệt độ tương đối thấp và diễn ra rất mạnh.
Điểm cuối của xăng không được quy định.
Xăng bắt đầu sôi dưới 40 C, cuối 180 C, nhiệt độ bắt đầu kết tinh không quá 60 C. Độ axit của xăng không quá 1 mg / 100 ml.
Điểm sôi cuối của xăng theo GOST là 185 C và nhiệt độ thực tế là 180 C.
Điểm sôi cuối của xăng là nhiệt độ tại đó một phần tiêu chuẩn (100 ml) của xăng thử được chưng cất hoàn toàn (đun sôi) từ bình thủy tinh trong đó nó được đặt trong bình thu nhận trong tủ lạnh.
| Sơ đồ cài đặt ổn định. |
Điểm sôi cuối cùng của xăng không được vượt quá 200 - 225 C. Đối với xăng hàng không, nhiệt độ sôi cuối thấp hơn nhiều, có trường hợp lên tới 120 C.
MPa, nhiệt độ sôi của xăng là 338 K, khối lượng mol trung bình của nó là 120 kg / kmol, và nhiệt hóa hơi là 252 kJ / kg.
Điểm sôi ban đầu của xăng, ví dụ 40 đối với xăng hàng không, cho biết sự có mặt của các phần nhỏ, sôi nhẹ, nhưng không cho biết hàm lượng của chúng. Điểm sôi của phần 10% đầu tiên, hay nhiệt độ bắt đầu, đặc trưng cho các đặc tính ban đầu của xăng, tính bay hơi của nó, cũng như xu hướng hình thành khóa khí trong hệ thống cung cấp xăng. Điểm sôi của phân đoạn 10% càng thấp thì động cơ càng dễ khởi động, nhưng cũng có khả năng hình thành khóa khí lớn hơn, có thể gây gián đoạn cung cấp nhiên liệu và thậm chí dừng động cơ. Nhiệt độ sôi của phân đoạn khởi động quá cao gây khó khăn cho việc khởi động động cơ ở nhiệt độ môi trường thấp, dẫn đến hao xăng.
| Ảnh hưởng của điểm cuối nhiệt độ sôi của xăng đến mức tiêu thụ trong quá trình vận hành xe. Ảnh hưởng của nhiệt độ chưng cất 90% xăng đến trị số octan của gasoline có nguồn gốc khác nhau. |
Sự giảm điểm cuối nhiệt độ sôi của các gasoline cải cách dẫn đến sự suy giảm khả năng chống kích nổ của chúng. Cần có những nghiên cứu và tính toán kinh tế để giải quyết vấn đề này.Cần lưu ý rằng theo thông lệ nước ngoài của một số quốc gia, các loại gasoline động cơ có nhiệt độ sôi từ 215 - 220 C hiện đang được sản xuất và sử dụng.
| Ảnh hưởng của điểm cuối nhiệt độ sôi của xăng đến mức tiêu thụ trong quá trình vận hành xe. Ảnh hưởng của nhiệt độ chưng cất 90% xăng đến trị số octan của gasoline có nguồn gốc khác nhau. |
Sự giảm điểm cuối nhiệt độ sôi của các gasoline cải cách dẫn đến sự suy giảm khả năng chống kích nổ của chúng. Cần có những nghiên cứu và tính toán kinh tế để giải quyết vấn đề này. Cần lưu ý rằng theo thông lệ nước ngoài của một số quốc gia, các loại gasoline động cơ có nhiệt độ sôi từ 215 - 220 C hiện đang được sản xuất và sử dụng.
Nếu điểm sôi cuối của xăng cao, thì các phân đoạn nặng chứa trong nó có thể không bay hơi, và do đó, không cháy hết trong động cơ, dẫn đến tăng mức tiêu thụ nhiên liệu.
Việc hạ thấp điểm sôi cuối của các gasoline chạy thẳng dẫn đến tăng khả năng chống kích nổ của chúng. Các gasoline chạy thẳng có trị số octan thấp có số octan tương ứng là 75 và 68 và được sử dụng như các thành phần của gasoline động cơ.
Đốt - xăng
Thiết kế và nguyên lý hoạt động Hệ thống phun xăng trực tiếp Bosch Motronic MED 7
Quá trình đốt cháy xăng, dầu hỏa và các hydrocacbon lỏng khác xảy ra trong pha khí. Sự cháy chỉ có thể xảy ra khi nồng độ hơi nhiên liệu trong không khí nằm trong giới hạn nhất định, riêng cho từng chất. Nếu một lượng nhỏ hơi nhiên liệu được chứa trong không khí IB, quá trình đốt cháy sẽ không xảy ra, cũng như trong trường hợp có quá nhiều hơi nhiên liệu và không đủ oxy.
| Sự thay đổi nhiệt độ trên bề mặt dầu hỏa trong quá trình chữa cháy bằng bọt. | Sự phân bố nhiệt độ trong dầu hỏa trước khi bắt đầu dập tắt (a và khi kết thúc. |
Khi xăng cháy, người ta biết rằng một lớp ho mẹt được hình thành, độ dày của lớp này tăng dần theo thời gian.
Khi xăng cháy, nước và khí cacbonic được hình thành. Điều này có đủ xác nhận rằng xăng không phải là một nguyên tố?
Khi xăng, dầu hỏa và các chất lỏng khác được đốt cháy trong các bồn chứa, sự nghiền nhỏ của dòng khí thành các thể tích riêng biệt và sự cháy của từng thể tích riêng biệt đặc biệt rõ ràng.
Khi xăng và dầu được đốt cháy trong các bồn chứa có đường kính lớn, đặc tính của hệ thống sưởi sẽ khác đáng kể so với mô tả ở trên. Khi chúng cháy, một lớp được nung nóng xuất hiện, độ dày của lớp này tăng lên một cách tự nhiên theo thời gian và nhiệt độ giống như nhiệt độ trên bề mặt chất lỏng. Dưới đó, nhiệt độ của chất lỏng giảm xuống nhanh chóng và gần bằng nhiệt độ ban đầu. Bản chất của các đường cong cho thấy rằng trong quá trình đốt cháy, xăng bị phân hủy thành hai lớp - một lớp trên và một lớp dưới.
Ví dụ, đốt cháy xăng trong không khí được gọi là một quá trình hóa học. Trong trường hợp này, năng lượng được giải phóng, tương đương khoảng 1300 kcal trên 1 mol xăng.
Việc phân tích các sản phẩm cháy của xăng và dầu đang trở nên vô cùng quan trọng, vì kiến thức về thành phần riêng lẻ của các sản phẩm đó là cần thiết để nghiên cứu các quá trình cháy trong động cơ và nghiên cứu ô nhiễm không khí.
Như vậy, khi xăng được đốt cháy trong các thùng rộng, có tới 40% nhiệt lượng thoát ra do quá trình đốt cháy được tiêu thụ cho bức xạ.
Bàn 76 cho thấy tốc độ cháy của xăng với phụ gia tetranitro-metan.
Các thí nghiệm đã chỉ ra rằng tốc độ đốt cháy xăng từ bề mặt của bồn chứa bị ảnh hưởng đáng kể bởi đường kính của nó.
| Căn chỉnh lực lượng, phương tiện khi dập lửa trên đoạn. |
Với sự hỗ trợ của GPS-600, lính cứu hỏa đã ứng phó thành công, loại bỏ được tình trạng cháy xăng tràn dọc đường ray, đảm bảo sự di chuyển của người điều khiển thùng xe đến nơi ghép xe tăng.Sau khi ngắt điện, bằng một đoạn dây tiếp xúc, họ gắn 2 bồn chứa xăng vào xe chữa cháy rồi kéo ra khỏi vùng cháy.
| Tốc độ đốt nóng của dầu trong các thùng có đường kính khác nhau. |
Một sự gia tăng đặc biệt lớn về tốc độ ấm lên do gió đã được nhận thấy khi đốt xăng. Khi xăng đang cháy trong thùng dài 2 64 m với tốc độ gió 1 3 m / s thì tốc độ đốt nóng là 9 63 mm / phút và ở tốc độ gió 10 m / s thì tốc độ đốt nóng tăng lên 17 1. mm / phút.
Nhiệt độ bốc cháy và các thông số khác
Quá trình đốt cháy than là một phản ứng hóa học của quá trình oxy hóa cacbon xảy ra ở nhiệt độ ban đầu cao và tỏa nhiệt mạnh. Giờ thì đơn giản hơn: nhiên liệu than không thể bốc cháy như giấy; cần phải làm nóng sơ bộ đến 370-700 ° C để đánh lửa, tùy thuộc vào nhãn hiệu nhiên liệu.
Thời điểm quan trọng. Hiệu suất của quá trình đốt than trong lò nung hoặc lò hơi đốt nhiên liệu rắn gia dụng được đặc trưng không phải ở nhiệt độ tối đa, mà là mức độ hoàn toàn của quá trình cháy. Mỗi phân tử carbon kết hợp với hai hạt oxy trong không khí để tạo thành carbon dioxide CO2. Quá trình này được phản ánh trong công thức hóa học.
Nếu hạn chế lượng ôxy đi vào (đậy quạt gió, chuyển lò hơi TT sang chế độ đốt cháy âm ỉ), thay vào đó CO2, carbon monoxide CO được hình thành và thải vào ống khói, hiệu suất đốt sẽ giảm đáng kể. Để đạt được hiệu quả cao, cần tạo điều kiện thuận lợi:
- Than nâu bốc cháy ở nhiệt độ +370 ° C, đá - 470 ° C, than antraxit - 700 độ. Cần làm nóng trước bộ gia nhiệt bằng củi (than củi mùn cưa).
- Không khí được cung cấp cho hộp cứu hỏa quá mức, hệ số an toàn là 1,3-1,5.
- Quá trình đốt cháy được hỗ trợ bởi nhiệt độ cao của than nóng nằm trên lò. Điều quan trọng là phải đảm bảo sự truyền oxy qua toàn bộ độ dày của nhiên liệu, vì không khí di chuyển qua chảo tro do sự hút gió tự nhiên của ống khói.
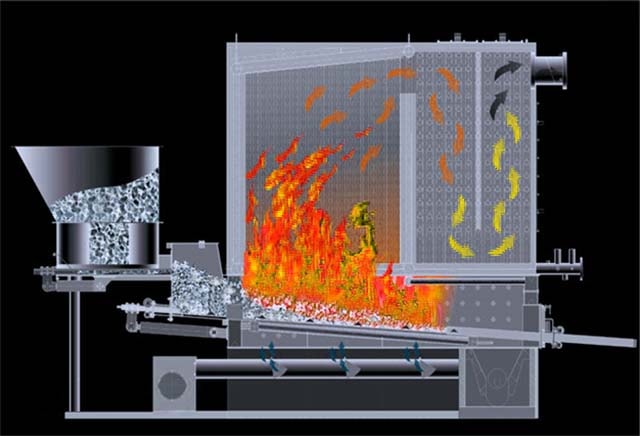
Bình luận. Các trường hợp ngoại lệ duy nhất là bếp kiểu Bubafonya sản xuất tại nhà và nồi hơi hình trụ cho đốt trên, nơi không khí được đưa vào lò từ trên xuống dưới.
Nhiệt độ cháy lý thuyết và truyền nhiệt riêng của các loại nhiên liệu khác nhau được thể hiện trong bảng so sánh. Điều đáng chú ý là, trong điều kiện lý tưởng, bất kỳ loại nhiên liệu nào cũng sẽ tỏa nhiệt tối đa khi tương tác với lượng không khí cần thiết.
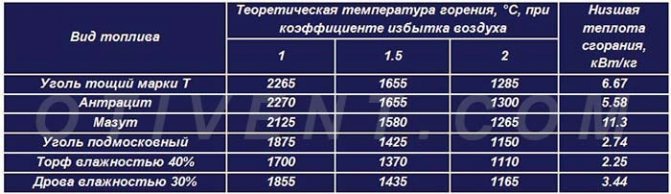

Trong thực tế, việc tạo ra các điều kiện như vậy là không thực tế, do đó không khí được cung cấp dư thừa. Nhiệt độ cháy thực của than nâu trong lò hơi TT thông thường nằm trong khoảng 700 ... 800 ° C, đá và than antraxit - 800 ... 1100 độ.
Nếu bạn lạm dụng nó với lượng oxy, năng lượng sẽ bắt đầu được sử dụng để làm nóng không khí và chỉ đơn giản là bay vào đường ống, hiệu suất của lò sẽ giảm xuống rõ rệt. Hơn nữa, nhiệt độ của đám cháy có thể lên tới 1500 ° C. Quá trình này giống như một đám cháy thông thường - ngọn lửa lớn, nhiệt lượng nhỏ. Một ví dụ về quá trình đốt cháy than hiệu quả bằng vòi đốt trên lò hơi tự động được trình bày trong video:
Nhiệt độ - quá trình đốt cháy - nhiên liệu
| Sự phụ thuộc của tiêu chí B vào tỷ số giữa diện tích các nguồn nhiệt với diện tích phân xưởng. |
Cường độ chiếu xạ của công nhân phụ thuộc vào nhiệt độ đốt cháy của nhiên liệu trong lò, kích thước của lỗ nạp, độ dày của thành lò tại lỗ nạp và cuối cùng là khoảng cách mà công nhân từ nơi nạp. hố.
| Tỷ lệ CO / CO và H2 / HO trong sản phẩm của quá trình đốt cháy không hoàn toàn khí thiên nhiên, phụ thuộc vào hệ số tiêu hao không khí a. |
Nhiệt độ thực tế có thể đạt được 1L là nhiệt độ cháy của nhiên liệu trong điều kiện thực tế. Khi xác định giá trị của nó, phải tính đến tổn thất nhiệt ra môi trường, thời gian của quá trình cháy, phương pháp đốt và các yếu tố khác.
Không khí dư thừa ảnh hưởng đáng kể đến nhiệt độ cháy của nhiên liệu.Vì vậy, ví dụ, nhiệt độ đốt cháy thực tế của khí thiên nhiên với lượng dư 10% không khí là 1868C, với lượng dư 20% là 1749C và với lượng không khí dư 100%, nó giảm xuống còn 1167 C. , việc đốt nóng không khí, đi đến quá trình đốt cháy nhiên liệu, làm tăng nhiệt độ của quá trình đốt cháy của nó. Vậy, khi đốt khí thiên nhiên (1Max 2003 C) với không khí được nung nóng đến 200 C thì nhiệt độ cháy tăng lên 2128 C, và khi đốt nóng không khí lên 400 C - lên đến 2257 C.
| Sơ đồ chung của thiết bị lò. |
Khi đốt nóng không khí và nhiên liệu dạng khí, nhiệt độ cháy của nhiên liệu tăng lên, do đó, nhiệt độ của không gian làm việc của lò cũng tăng lên. Trong nhiều trường hợp, không thể đạt được nhiệt độ cần thiết cho một quy trình công nghệ nhất định nếu không có nhiệt độ cao của không khí và nhiên liệu khí. Ví dụ, luyện thép trong lò nung lộ thiên, trong đó nhiệt độ của ngọn đuốc (dòng khí cháy) trong không gian nóng chảy phải là 1800 - 2000 C, sẽ không thể nếu không làm nóng không khí và khí đốt lên 1000 - 1200 C. Khi đốt nóng các lò công nghiệp sử dụng nhiên liệu địa phương có hàm lượng calo thấp (củi ẩm, than bùn, than nâu), công việc của họ mà không làm nóng không khí thường thậm chí là không thể.
Từ công thức này có thể thấy rằng nhiệt độ cháy của nhiên liệu có thể tăng lên bằng cách tăng tử số và giảm mẫu số. Sự phụ thuộc của nhiệt độ cháy của các khí khác nhau vào tỷ lệ không khí dư được thể hiện trong Hình.
Không khí dư thừa cũng ảnh hưởng mạnh đến nhiệt độ cháy của nhiên liệu. Vậy nhiệt lượng của khí thiên nhiên với không khí dư 10% - 1868 C, với không khí dư 20% - 1749 C và với lượng dư 100% bằng 1167 C.
Nếu nhiệt độ mối nối nóng chỉ bị giới hạn bởi nhiệt độ đốt cháy của nhiên liệu, thì việc sử dụng bộ hồi lưu có thể làm tăng nhiệt độ bằng cách tăng nhiệt độ của các sản phẩm cháy và do đó tăng hiệu suất tổng thể của TEG.
Sự làm giàu của vụ nổ với oxy dẫn đến sự gia tăng đáng kể nhiệt độ cháy của nhiên liệu. Như dữ liệu đồ thị trong Hình. 17, nhiệt độ lý thuyết của quá trình đốt cháy nhiên liệu có liên quan đến việc làm giàu oxy của vụ nổ bằng một sự phụ thuộc, thực tế là tuyến tính với hàm lượng oxy trong vụ nổ là 40%. Ở các mức độ làm giàu cao hơn, sự phân ly của các sản phẩm cháy bắt đầu có ảnh hưởng đáng kể, do đó các đường cong của sự phụ thuộc nhiệt độ vào mức độ làm giàu của vụ nổ lệch khỏi đường thẳng và tiệm cận với nhiệt độ giới hạn cho một nhiên liệu. Do đó, sự phụ thuộc được coi là của nhiệt độ đốt cháy nhiên liệu vào mức độ làm giàu oxy của vụ nổ có hai vùng - vùng có độ giàu tương đối thấp, nơi có sự phụ thuộc tuyến tính và vùng có độ giàu cao (trên 40%), nơi sự gia tăng nhiệt độ có một đặc tính phân rã.
Một chỉ tiêu kỹ thuật nhiệt quan trọng của hoạt động của lò là nhiệt độ lò, nhiệt độ này phụ thuộc vào nhiệt độ cháy của nhiên liệu và bản chất của nhiệt tiêu thụ.
Tro của nhiên liệu, tùy thuộc vào thành phần của các tạp chất khoáng, ở nhiệt độ của quá trình cháy của nhiên liệu có thể được nung chảy thành các mảnh xỉ. Đặc tính của tro nhiên liệu phụ thuộc vào nhiệt độ được cho trong bảng. NHƯNG.
Giá trị của tmaK trong bảng. IV - З - nhiệt lượng đốt cháy nhiên liệu (lý thuyết).
Tổn thất nhiệt qua thành lò ra bên ngoài (ra môi trường) làm giảm nhiệt độ cháy của nhiên liệu.
Đốt cháy nhiên liệu
Quá trình đốt cháy nhiên liệu là quá trình oxy hóa các thành phần dễ cháy xảy ra ở nhiệt độ cao và kèm theo đó là sự tỏa nhiệt. Bản chất của quá trình cháy được xác định bởi nhiều yếu tố, bao gồm phương pháp đốt, thiết kế của lò, nồng độ oxy, ... Nhưng các điều kiện của quá trình, thời gian và kết quả cuối cùng của quá trình cháy phần lớn phụ thuộc vào thành phần , các đặc tính vật lý và hóa học của nhiên liệu.
Thành phần nhiên liệu
Nhiên liệu rắn bao gồm than đá và than nâu, than bùn, đá phiến dầu, gỗ. Các loại nhiên liệu này là các hợp chất hữu cơ phức tạp được hình thành chủ yếu bởi năm nguyên tố - cacbon C, hydro H, oxy O, lưu huỳnh S và nitơ N. Nhiên liệu cũng chứa hơi ẩm và các khoáng chất khó cháy, tạo thành tro sau khi đốt cháy. Độ ẩm và tro là chất dằn bên ngoài của nhiên liệu, trong khi oxy và nitơ là bên trong.
Thành phần chính của bộ phận dễ cháy là cacbon, nó quyết định sự tỏa ra nhiệt lượng lớn nhất. Tuy nhiên, tỷ lệ cacbon trong nhiên liệu rắn càng lớn thì càng khó bắt lửa. Trong quá trình đốt cháy, hydro giải phóng nhiệt nhiều hơn 4,4 lần so với carbon, nhưng tỷ trọng của nó trong thành phần của nhiên liệu rắn là rất nhỏ. Oxy, không phải là một yếu tố tạo nhiệt và liên kết hydro và carbon, làm giảm nhiệt của quá trình đốt cháy, do đó nó là một yếu tố không mong muốn. Hàm lượng của nó đặc biệt cao trong than bùn và gỗ. Lượng nitơ trong nhiên liệu rắn tuy ít nhưng có khả năng tạo thành các ôxít có hại cho môi trường và con người. Lưu huỳnh cũng là một tạp chất có hại, nó tỏa nhiệt ít, nhưng tạo thành các ôxít dẫn đến ăn mòn kim loại của lò hơi và ô nhiễm bầu khí quyển.
Thông số kỹ thuật nhiên liệu và ảnh hưởng của chúng đến quá trình đốt cháy
Các đặc tính kỹ thuật quan trọng nhất của nhiên liệu là: nhiệt lượng đốt cháy, năng suất chất bay hơi, tính chất cặn không bay hơi (than cốc), hàm lượng tro và độ ẩm.
Nhiệt đốt cháy nhiên liệu
Nhiệt trị là nhiệt lượng tỏa ra trong quá trình đốt cháy hoàn toàn một đơn vị khối lượng (kJ / kg) hoặc thể tích nhiên liệu (kJ / m3). Phân biệt nhiệt cao hơn và nhiệt thấp hơn của quá trình cháy. Cao nhất bao gồm nhiệt thoát ra trong quá trình ngưng tụ hơi chứa trong các sản phẩm cháy. Khi đốt cháy nhiên liệu trong lò hơi, khí thải của khói thải có nhiệt độ mà hơi ẩm ở trạng thái hơi. Do đó, trong trường hợp này, nhiệt lượng đốt cháy thấp hơn được sử dụng, không tính đến nhiệt ngưng tụ hơi nước.
Thành phần và giá trị nhiệt thực của tất cả các mỏ than đã biết đã được xác định và đưa ra trong các đặc tính tính toán.
Giải phóng vật chất bay hơi
Khi nhiên liệu rắn được đốt nóng mà không tiếp xúc với không khí dưới ảnh hưởng của nhiệt độ cao, hơi nước đầu tiên được giải phóng, và sau đó sự phân hủy nhiệt của các phân tử xảy ra với sự giải phóng các chất khí, được gọi là các chất dễ bay hơi.
Việc giải phóng các chất dễ bay hơi có thể xảy ra trong khoảng nhiệt độ từ 160 đến 1100 ° C, nhưng trung bình - trong khoảng nhiệt độ 400-800 ° C. Nhiệt độ của thời điểm bắt đầu giải phóng các chất bay hơi, số lượng và thành phần của các sản phẩm ở thể khí phụ thuộc vào thành phần hóa học của nhiên liệu. Nhiên liệu càng cũ về mặt hóa học, sự giải phóng các chất bay hơi càng thấp và nhiệt độ bắt đầu giải phóng chúng càng cao.
Các chất bay hơi cung cấp sự bắt lửa sớm hơn của các hạt vật chất và có ảnh hưởng đáng kể đến quá trình đốt cháy nhiên liệu. Nhiên liệu non - than bùn, than nâu - dễ bắt cháy, cháy nhanh và gần như hoàn toàn. Ngược lại, nhiên liệu có chất bay hơi thấp, chẳng hạn như antraxit, khó bắt lửa hơn, cháy chậm hơn nhiều và không cháy hoàn toàn (tăng tổn thất nhiệt).
Đặc tính cặn không bay hơi (than cốc)
Phần rắn của nhiên liệu còn lại sau khi giải phóng các chất bay hơi, bao gồm chủ yếu là cacbon và một phần khoáng, được gọi là than cốc. Cặn than cốc có thể, tùy thuộc vào tính chất của các hợp chất hữu cơ có trong khối dễ cháy: đóng cục, đóng cục yếu (bị phá hủy khi tiếp xúc), dạng bột. Than antraxit, than bùn, than nâu tạo ra cặn bột không bay hơi. Hầu hết các loại than bitum đều được thiêu kết, nhưng không phải lúc nào cũng được nung mạnh. Cặn dính hoặc bột không bay hơi tạo ra than bitum với hiệu suất chất bay hơi rất cao (42-45%) và với năng suất rất thấp (dưới 17%).
Cấu trúc của cặn than cốc rất quan trọng khi đốt than trong lò ghi.Khi đốt lò hơi công suất, hiệu suất than cốc không quan trọng lắm.
Hàm lượng tro
Nhiên liệu rắn chứa lượng tạp chất khoáng khó cháy lớn nhất. Chúng chủ yếu là đất sét, silicat, pyrit sắt, nhưng oxit sắt, sunfat, cacbonat và silicat của sắt, oxit của các kim loại khác nhau, clorua, kiềm, v.v. cũng có thể được bao gồm. Hầu hết chúng rơi xuống trong quá trình khai thác dưới dạng đá, giữa các vỉa than nằm giữa, nhưng cũng có các chất khoáng đã đi vào nhiên liệu từ lò luyện than hoặc trong quá trình chuyển đổi khối lượng ban đầu của nó.
Khi đốt cháy nhiên liệu, các tạp chất khoáng trải qua một loạt các phản ứng, kết quả là tạo thành cặn rắn không cháy được gọi là tro. Khối lượng và thành phần của tro không đồng nhất với khối lượng và thành phần tạp chất khoáng của nhiên liệu.
Tính chất tro đóng vai trò quan trọng trong tổ chức vận hành lò hơi và lò. Các hạt của nó, do các sản phẩm cháy mang đi, mài mòn các bề mặt gia nhiệt ở tốc độ cao, và ở tốc độ thấp, chúng bị lắng lại trên chúng, dẫn đến sự suy giảm khả năng truyền nhiệt. Tro mang đi vào ống khói có thể gây hại cho môi trường, để tránh điều này cần phải lắp đặt các thiết bị thu gom tro.
Một đặc tính quan trọng của tro là tính dễ chảy; chúng phân biệt giữa tro chịu lửa (trên 1425 ° C), nóng chảy trung bình (1200-1425 ° C) và tro nóng chảy thấp (dưới 1200 ° C). Tro đã qua giai đoạn nấu chảy và chuyển thành một khối nung kết hoặc nung chảy được gọi là xỉ. Đặc tính nhiệt độ của khả năng nấu chảy tro có tầm quan trọng lớn đối với việc đảm bảo hoạt động đáng tin cậy của các bề mặt lò và nồi hơi; việc lựa chọn chính xác nhiệt độ của các khí gần các bề mặt này sẽ loại bỏ xỉ.
Độ ẩm
Độ ẩm là một thành phần không mong muốn của nhiên liệu, nó cùng với các tạp chất khoáng là chất dằn và làm giảm hàm lượng của phần dễ cháy. Ngoài ra, nó làm giảm giá trị nhiệt, vì năng lượng bổ sung là cần thiết cho sự bay hơi của nó.
Độ ẩm trong nhiên liệu có thể là bên trong hoặc bên ngoài. Độ ẩm bên ngoài được chứa trong các mao quản hoặc bị giữ lại trên bề mặt. Với tuổi hóa học, lượng ẩm mao mạch giảm dần. Các mảnh nhiên liệu càng nhỏ thì độ ẩm bề mặt càng lớn. Độ ẩm bên trong xâm nhập vào chất hữu cơ.
Độ ẩm trong nhiên liệu làm giảm nhiệt của quá trình cháy và dẫn đến tăng mức tiêu hao nhiên liệu. Đồng thời, thể tích sản phẩm cháy tăng, tổn thất nhiệt với khí thải tăng và hiệu suất của tổ máy lò hơi giảm. Độ ẩm cao vào mùa đông dẫn đến đóng băng than, khó nghiền và giảm độ chảy.
Phương pháp đốt nhiên liệu tùy thuộc vào loại lò
Các loại thiết bị đốt chính:
- nhiều lớp,
- buồng.
Lò nung lớp nhằm đốt cháy nhiên liệu rắn dạng cục. Chúng có thể đặc và lỏng. Khi đốt cháy trong một lớp dày đặc, không khí cháy đi qua lớp đó mà không ảnh hưởng đến tính ổn định của nó, nghĩa là, trọng lực của các hạt cháy vượt quá áp suất động của không khí. Khi đốt cháy trong tầng sôi, do vận tốc không khí tăng lên, các hạt chuyển sang trạng thái "sôi". Trong trường hợp này, sự hòa trộn tích cực giữa chất oxy hóa và nhiên liệu xảy ra, do đó quá trình đốt cháy nhiên liệu được tăng cường.
TẠI lò nung đốt cháy nhiên liệu dạng bột rắn, cũng như chất lỏng và khí. Lò buồng được chia thành các lò xyclon và lò nung. Trong quá trình đốt cháy, các hạt than không được quá 100 micron, chúng cháy theo thể tích của buồng đốt. Quá trình đốt cháy theo chu kỳ cho phép kích thước hạt lớn hơn; dưới tác động của lực ly tâm, chúng bị văng lên thành lò và cháy hoàn toàn theo dòng xoáy trong vùng nhiệt độ cao.
Sự đốt cháy nhiên liệu. Các giai đoạn chính của quy trình
Trong quá trình đốt cháy nhiên liệu rắn, có thể phân biệt một số giai đoạn: đốt nóng và bay hơi ẩm, thăng hoa các chất bay hơi và hình thành cặn than cốc, đốt các chất bay hơi và than cốc, và hình thành xỉ. Sự phân chia quá trình đốt cháy này tương đối tùy tiện, vì mặc dù các giai đoạn này diễn ra tuần tự, nhưng chúng có một phần chồng chéo lên nhau. Vì vậy, sự thăng hoa của các chất dễ bay hơi bắt đầu trước khi sự bay hơi cuối cùng của tất cả độ ẩm, sự hình thành các chất bay hơi xảy ra đồng thời với quá trình đốt cháy chúng, giống như sự bắt đầu của quá trình oxy hóa cặn than cốc trước khi kết thúc quá trình đốt cháy các chất bay hơi, và Quá trình đốt than cốc cũng có thể tiến hành sau khi tạo xỉ.
Thời gian chảy của mỗi giai đoạn của quá trình cháy phần lớn được xác định bởi các đặc tính của nhiên liệu. Giai đoạn đốt than cốc kéo dài lâu nhất, ngay cả đối với nhiên liệu có năng suất bay hơi cao. Các yếu tố vận hành khác nhau và các tính năng thiết kế của lò có tác động đáng kể đến thời gian của các giai đoạn của quá trình đốt.
1. Chuẩn bị nhiên liệu trước khi đánh lửa
Nhiên liệu đi vào lò được đốt nóng, do đó, khi có hơi ẩm, nó sẽ bay hơi và nhiên liệu bị khô. Thời gian cần thiết để làm nóng và sấy khô phụ thuộc vào lượng ẩm và nhiệt độ mà nhiên liệu được cung cấp cho thiết bị đốt. Đối với nhiên liệu có độ ẩm cao (than bùn, than nâu ướt), giai đoạn gia nhiệt và sấy khô tương đối lâu.
Nhiên liệu được cung cấp cho các lò xếp chồng lên nhau ở nhiệt độ gần với nhiệt độ môi trường. Chỉ vào mùa đông, khi than đóng băng, nhiệt độ của nó mới thấp hơn trong phòng lò hơi. Đối với quá trình đốt trong lò đốt và lò xoáy, nhiên liệu phải được nghiền và nghiền, kèm theo làm khô bằng không khí nóng hoặc khí lò. Nhiệt độ của nhiên liệu vào càng cao thì cần ít thời gian và nhiệt để đốt nóng nó đến nhiệt độ bốc cháy.
Quá trình làm khô nhiên liệu trong lò xảy ra do hai nguồn nhiệt: nhiệt đối lưu của sản phẩm cháy và nhiệt bức xạ của mỏ hàn, lớp lót, xỉ.
Trong các lò buồng, quá trình gia nhiệt được thực hiện chủ yếu do nguồn thứ nhất, tức là, phụ gia các sản phẩm cháy vào nhiên liệu tại thời điểm đưa vào lò. Vì vậy, một trong những yêu cầu quan trọng đối với việc thiết kế các thiết bị đưa nhiên liệu vào lò là phải đảm bảo hút mạnh các sản phẩm cháy. Nhiệt độ cao hơn trong hộp cứu hỏa cũng góp phần làm cho thời gian làm nóng và sấy khô ngắn hơn. Để đạt được mục đích này, khi đốt cháy nhiên liệu khi bắt đầu giải phóng các chất bay hơi ở nhiệt độ cao (hơn 400 ° C), các đai cháy được chế tạo trong các lò buồng, nghĩa là chúng đóng các ống chắn bằng vật liệu cách nhiệt chịu lửa trong để giảm cảm nhận nhiệt của chúng.
Khi đốt nhiên liệu theo kiểu giường, vai trò của từng loại nguồn nhiệt do thiết kế của lò quyết định. Trong các lò có lưới thép, quá trình gia nhiệt và sấy khô được thực hiện chủ yếu bằng nhiệt bức xạ của ngọn đuốc. Trong các lò có ghi cố định và cấp nhiên liệu từ phía trên, quá trình đốt nóng và sấy xảy ra do các sản phẩm cháy chuyển động qua lớp từ dưới lên.
Trong quá trình đun nóng ở nhiệt độ trên 110 ° C, sự phân hủy nhiệt của các chất hữu cơ tạo nên nhiên liệu bắt đầu. Các hợp chất kém mạnh nhất là những hợp chất chứa một lượng oxy đáng kể. Các hợp chất này bị phân hủy ở nhiệt độ tương đối thấp với sự hình thành các chất bay hơi và cặn rắn, bao gồm chủ yếu là cacbon.
Nhiên liệu non về thành phần hoá học, chứa nhiều ôxi, có nhiệt độ thấp thời kỳ đầu giải phóng các chất ở thể khí và cho tỉ lệ phần trăm của chúng cao hơn. Nhiên liệu có hàm lượng hợp chất oxy thấp có năng suất bay hơi thấp và điểm chớp cháy cao hơn.
Hàm lượng các phân tử trong nhiên liệu rắn dễ bị phân hủy khi đun nóng cũng ảnh hưởng đến khả năng phản ứng của cặn không bay hơi.Đầu tiên, sự phân hủy của khối chất cháy xảy ra chủ yếu ở bề mặt ngoài của nhiên liệu. Với việc gia nhiệt thêm, các phản ứng sinh nhiệt bắt đầu xảy ra bên trong các hạt nhiên liệu, áp suất tăng lên trong chúng và lớp vỏ bên ngoài bị vỡ. Khi đốt cháy nhiên liệu có năng suất bay hơi cao, cặn than cốc trở nên xốp và có bề mặt lớn hơn so với cặn rắn đặc.
2. Quá trình đốt cháy các hợp chất khí và than cốc
Quá trình đốt cháy nhiên liệu thực tế bắt đầu bằng sự đốt cháy các chất dễ bay hơi. Trong giai đoạn chuẩn bị nhiên liệu, các phản ứng dây chuyền phân nhánh của quá trình oxy hóa các chất ở thể khí xảy ra, lúc đầu các phản ứng này diễn ra với tốc độ thấp. Nhiệt giải phóng được cảm nhận bởi các bề mặt của lò và một phần được tích lũy dưới dạng năng lượng của các phân tử chuyển động. Điều này dẫn đến sự gia tăng tốc độ của các phản ứng dây chuyền. Ở một nhiệt độ nhất định, các phản ứng oxy hóa xảy ra với tốc độ sao cho nhiệt lượng tỏa ra bao phủ hoàn toàn sự hấp thụ nhiệt. Nhiệt độ này là điểm chớp cháy.
Nhiệt độ bắt lửa không phải là hằng số, nó phụ thuộc cả vào đặc tính của nhiên liệu và các điều kiện trong vùng bắt lửa, trung bình là 400-600 ° C. Sau khi đốt cháy hỗn hợp khí, các phản ứng oxi hóa tự tăng tốc tiếp tục làm tăng nhiệt độ. Để duy trì sự cháy, cần phải cung cấp liên tục các chất oxy hóa và chất cháy.
Sự bốc cháy của các chất ở thể khí dẫn đến sự bao bọc của hạt than cốc trong vỏ lửa. Quá trình đốt than cốc bắt đầu khi quá trình đốt cháy các chất bay hơi kết thúc. Hạt rắn nóng lên đến nhiệt độ cao, và khi lượng chất bay hơi giảm, độ dày của lớp đốt ranh giới giảm, oxy đến bề mặt cacbon nóng.
Quá trình đốt than cốc bắt đầu ở nhiệt độ 1000 ° C và là quá trình lâu nhất. Nguyên nhân là do nồng độ oxy giảm thứ nhất, thứ hai là phản ứng dị thể tiến hành chậm hơn phản ứng đồng thể. Kết quả là thời gian cháy của một hạt nhiên liệu rắn được xác định chủ yếu bằng thời gian cháy của cặn than cốc (khoảng 2/3 tổng thời gian). Đối với nhiên liệu có năng suất chất bay hơi cao, cặn rắn nhỏ hơn ½ khối lượng hạt ban đầu, do đó, quá trình cháy của chúng diễn ra nhanh chóng và khả năng cháy dưới thấp. Nhiên liệu cũ về mặt hóa học có dạng hạt dày đặc, quá trình đốt cháy chúng mất gần như toàn bộ thời gian trong lò.
Cặn than cốc của hầu hết các nhiên liệu rắn là chủ yếu, và đối với một số loài, hoàn toàn bao gồm cacbon. Quá trình đốt cháy carbon rắn xảy ra với sự tạo thành carbon monoxide và carbon dioxide.
Điều kiện tối ưu để tản nhiệt
Việc tạo ra các điều kiện tối ưu cho quá trình đốt cháy cacbon là cơ sở để xây dựng đúng phương pháp công nghệ đốt nhiên liệu rắn trong các tổ máy lò hơi. Các yếu tố sau đây có thể ảnh hưởng đến việc đạt được sự tỏa nhiệt cao nhất trong lò: nhiệt độ, không khí thừa, sự hình thành hỗn hợp sơ cấp và thứ cấp.
Nhiệt độ... Sự tỏa nhiệt trong quá trình đốt cháy nhiên liệu phụ thuộc đáng kể vào chế độ nhiệt độ của lò. Ở nhiệt độ tương đối thấp, quá trình đốt cháy hoàn toàn các chất dễ cháy xảy ra trong lõi đèn pin; cacbon monoxit, hydro và hydrocacbon vẫn còn trong các sản phẩm cháy. Ở nhiệt độ từ 1000 đến 1800-2000 ° C, có thể đốt cháy hoàn toàn nhiên liệu.
Không khí dư thừa... Nhiệt lượng riêng đạt giá trị lớn nhất khi đốt cháy hoàn toàn và tỷ lệ không khí dư là hợp nhất. Với việc giảm tỷ lệ không khí thừa, sự tỏa nhiệt giảm, vì thiếu oxy dẫn đến quá trình oxy hóa của nhiên liệu ít hơn. Mức nhiệt độ giảm, tốc độ phản ứng giảm, dẫn đến sự tỏa nhiệt giảm mạnh.
Sự gia tăng tỷ lệ không khí thừa lớn hơn sự đồng nhất làm giảm sự sinh nhiệt thậm chí nhiều hơn sự thiếu không khí.Trong điều kiện thực tế của quá trình đốt cháy nhiên liệu trong lò hơi, các giá trị giới hạn của sự tỏa nhiệt không đạt được, do có sự cháy không hoàn toàn. Nó phụ thuộc phần lớn vào cách tổ chức các quá trình hình thành hỗn hợp.
Quy trình trộn... Trong các lò buồng, quá trình trộn sơ cấp được thực hiện bằng cách làm khô và trộn nhiên liệu với không khí, cung cấp một phần không khí (sơ cấp) cho vùng chuẩn bị, tạo ra một ngọn đuốc mở rộng với bề mặt rộng và độ hỗn loạn cao, sử dụng không khí được làm nóng.
Trong các lò nung nhiều lớp, nhiệm vụ trộn chính là cung cấp lượng không khí cần thiết cho các vùng cháy khác nhau trên ghi.
Để đảm bảo sau khi đốt cháy các sản phẩm khí của quá trình cháy không hoàn toàn và than cốc, các quá trình hình thành hỗn hợp thứ cấp được tổ chức. Các quá trình này được tạo điều kiện thuận lợi bởi: cung cấp không khí thứ cấp ở tốc độ cao, tạo ra khí động học như vậy, trong đó đạt được sự lấp đầy đồng đều toàn bộ lò bằng một ngọn đuốc và do đó, thời gian lưu trú của khí và các hạt than cốc trong lò tăng.
3. Sự hình thành xỉ
Trong quá trình ôxy hoá khối lượng cháy của nhiên liệu rắn, các tạp chất khoáng cũng xảy ra những thay đổi đáng kể. Các chất và hợp kim có nhiệt độ nóng chảy thấp hòa tan các hợp chất chịu lửa.
Điều kiện tiên quyết để lò hơi hoạt động bình thường là việc loại bỏ các sản phẩm cháy và xỉ tạo thành không bị gián đoạn.
Trong quá trình đốt cháy lớp, sự hình thành xỉ có thể dẫn đến cháy dưới cơ học - các tạp chất khoáng bao bọc các hạt than cốc chưa cháy, hoặc xỉ nhớt có thể chặn đường không khí, ngăn cản sự tiếp cận oxy đến than cốc đang cháy. Để giảm quá trình đốt cháy, các biện pháp khác nhau được sử dụng - trong các lò có lưới thép, thời gian dành cho ghi xỉ được tăng lên, và thường xuyên thực hiện việc tráng xỉ.
Trong các lò nung nhiều lớp, xỉ được loại bỏ ở dạng khô. Trong các lò buồng, quá trình loại bỏ xỉ có thể ở dạng khô hoặc dạng lỏng.
Như vậy, quá trình đốt cháy nhiên liệu là một quá trình hóa lý phức tạp, chịu ảnh hưởng của một số lượng lớn các yếu tố khác nhau, nhưng tất cả chúng đều phải được tính đến khi thiết kế nồi hơi và lò nung.
Đốt - xăng
Việc đốt cháy xăng khi phát nổ kèm theo sự xuất hiện của tiếng gõ kim loại sắc nhọn, khói đen bám trên ống xả, tăng mức tiêu thụ xăng, giảm công suất động cơ và các hiện tượng tiêu cực khác.
Quá trình đốt cháy xăng trong động cơ còn phụ thuộc vào tỷ lệ không khí dư. Tại các giá trị a 0 9 - j - 1 1, tốc độ của quá trình oxy hóa trước ngọn lửa trong hỗn hợp làm việc là cao nhất. Do đó, tại các giá trị này của a, các điều kiện thuận lợi nhất được tạo ra để bắt đầu kích nổ.
Sau quá trình đốt cháy xăng, tổng khối lượng của các chất ô nhiễm đó tăng lên đáng kể cùng với sự phân bố lại tổng thể về số lượng của chúng. Tỷ lệ benzen trong hơi nước ngưng tụ của khí thải ô tô cao hơn trong xăng khoảng 1 đến 7 lần; hàm lượng toluen cao hơn 3 lần, và hàm lượng xylen cao hơn 30 lần. Người ta biết rằng các hợp chất oxy được tạo thành trong trường hợp này, và số lượng các ion, đặc trưng của các hợp chất không bão hòa nặng hơn của dãy olefin hoặc xicloparafin và dãy axetylen hoặc diene, đặc biệt là dãy sau, tăng mạnh. Nói chung, những thay đổi đối với buồng Haagen-Smit giống với những thay đổi cần thiết để làm cho thành phần của các mẫu khí thải điển hình của xe tương tự như trong mẫu khói ở Los Angeles.
Nhiệt trị của xăng phụ thuộc vào thành phần hóa học của nó. Do đó, các hydrocacbon giàu hydro (ví dụ, parafinic) có nhiệt lượng đốt cháy lớn.
Các sản phẩm cháy của xăng nở ra trong động cơ đốt trong dọc theo polytrope n1 27 từ 30 đến 3 at. Nhiệt độ ban đầu của các chất khí là 2100 C; Thành phần khối lượng của sản phẩm cháy của 1 kg xăng như sau: CO23 135 kg, H2 1 305 kg, O20 34 kg, N2 12 61 kg.Xác định công nở ra của các khí này nếu cho 2 g xăng vào xilanh cùng một lúc.
| Ảnh hưởng của TPP đến sự hình thành cacbon trong động cơ. |
Khi xăng được đốt cháy từ nhà máy nhiệt điện, cặn cacbon được hình thành có chứa chì oxit.
Khi xăng được đốt cháy trong động cơ đốt trong pittông, hầu như tất cả các sản phẩm được tạo thành đều mang theo khí thải. Chỉ một phần tương đối nhỏ các sản phẩm của quá trình đốt cháy không hoàn toàn nhiên liệu và dầu, một lượng nhỏ các hợp chất vô cơ được hình thành từ các nguyên tố đưa vào nhiên liệu, không khí và dầu, được lắng đọng dưới dạng cặn cacbon.
Khi xăng cháy với chì tetraetyl, oxit chì được hình thành, chỉ nóng chảy ở nhiệt độ 900 C và có thể bay hơi ở nhiệt độ rất cao, vượt quá nhiệt độ trung bình trong xi-lanh động cơ. Để ngăn chặn sự lắng đọng của oxit chì trong động cơ, các chất đặc biệt được đưa vào chất lỏng etylic - chất tẩy rửa. Các hydrocacbon halogen hóa được sử dụng làm chất nhặt rác. Thông thường đây là những hợp chất có chứa brom và clo, chúng cũng đốt cháy và liên kết chì trong các hợp chất bromua và clorua mới.
| Ảnh hưởng của TPP đến sự hình thành cacbon trong động cơ. |
Khi xăng được đốt cháy từ nhà máy nhiệt điện, cặn cacbon được hình thành có chứa chì oxit.
Trong quá trình đốt cháy xăng có chứa TPP nguyên chất, một mảng hợp chất chì được lắng đọng trong động cơ. Thành phần của chất lỏng etyl cấp R-9 (theo trọng lượng): chì tetraetyl 54 0%, bromoetan 33 0%, monoloronaphtalen 6 8 0 5%, chất độn - hàng không - xăng - đến 100%; nhuộm màu đỏ sẫm 1 g trên 1 kg hỗn hợp.
Khi đốt cháy xăng chứa TPP, trong động cơ sẽ hình thành ôxít lỗ rò có độ bay hơi thấp; vì điểm nóng chảy của oxit chì khá cao (888), một phần của nó (khoảng 10%, tính cả chì được đưa vào xăng) được lắng đọng dưới dạng cặn rắn trên thành buồng đốt, nến và van, dẫn đến một sự cố động cơ nhanh chóng.
Khi xăng được đốt cháy trong động cơ ô tô, các phân tử nhỏ hơn cũng được hình thành và năng lượng được giải phóng được phân phối trong một thể tích lớn hơn.
Khí nóng sáng từ quá trình đốt cháy xăng chảy xung quanh bộ trao đổi nhiệt 8 (bên trong từ thành bên của buồng đốt và xa hơn, qua các cửa sổ 5 bên ngoài, đi qua buồng khí thải 6) và đốt nóng không khí trong kênh trao đổi nhiệt. Tiếp theo, khí thải nóng được đưa qua ống xả số 7 dưới bể chứa và làm nóng động cơ từ bên ngoài, đồng thời khí nóng từ bộ trao đổi nhiệt được đưa qua ống xả vào cacte và làm nóng động cơ từ bên trong. Trong 1 5 - 2 phút sau khi bắt đầu làm nóng, phích cắm phát sáng sẽ tắt và quá trình đốt cháy trong lò sưởi tiếp tục mà không có sự tham gia của nó. Sau 7 - 13 phút kể từ thời điểm nhận được xung để khởi động động cơ, dầu trong cacte nóng lên đến nhiệt độ 30 C (ở nhiệt độ môi trường lên đến -25 C) và bộ phận bắt đầu phát xung, sau đó máy sưởi đã tắt.
Nhiệt độ đốt cháy
Trong kỹ thuật nhiệt, người ta phân biệt nhiệt độ cháy của các chất khí sau đây: tỏa nhiệt, nhiệt lượng, lý thuyết và thực tế (tính toán). Công suất cấp nóng tx là nhiệt độ lớn nhất của sản phẩm cháy hoàn toàn khí ở điều kiện đoạn nhiệt có hệ số không khí dư a = 1,0 và ở nhiệt độ khí và không khí bằng 0 ° C:
tx = Qh / (IVcv) (8,11)
trong đó QH là nhiệt trị thấp nhất của khí, kJ / m3; IVcp - tổng tích các thể tích của khí cacbonic, hơi nước và nitơ được tạo thành trong quá trình đốt cháy 1 m3 khí (m3 / m3) và nhiệt dung thể tích trung bình của chúng ở áp suất không đổi trong phạm vi nhiệt độ từ 0 ° đến tx (kJ / (m3 * ° С).
Do nhiệt dung của các chất khí không giống nhau nên công suất tỏa nhiệt được xác định bằng phương pháp gần đúng liên tiếp. Là thông số ban đầu, giá trị của nó được lấy đối với khí tự nhiên (= 2000 ° C), với a = 1,0, thể tích của các thành phần của sản phẩm cháy được xác định, theo bảng.8.3, nhiệt dung trung bình của chúng được tìm thấy và sau đó, theo công thức (8.11), nhiệt dung của chất khí được tính. Nếu kết quả của phép tính thấp hơn hoặc cao hơn nhiệt độ được chấp nhận, thì một nhiệt độ khác được đặt và phép tính được lặp lại. Công suất tỏa nhiệt của các chất khí đơn giản và phức tạp thông thường khi chúng cháy trong không khí khô được cho trong bảng. 8,5. Khi đốt cháy khí trong không khí chứa khoảng 1 wt. % độ ẩm, nhiệt sản xuất giảm 25-30 ° С.
Nhiệt lượng đốt cháy tK là nhiệt độ được xác định không tính đến sự phân ly của hơi nước và khí cacbonic, nhưng có tính đến nhiệt độ ban đầu thực tế của khí và không khí. Nó khác với sản lượng nhiệt tx ở chỗ nhiệt độ khí và không khí, cũng như hệ số không khí dư a, được lấy từ các giá trị thực của chúng. Bạn có thể xác định tK theo công thức:
tк = (Qн + qphys) / (ΣVcp) (8.12)
trong đó qphys là hàm lượng nhiệt (nhiệt vật lý) của khí và không khí, được đo từ 0 ° C, kJ / m3.
Khí tự nhiên và dầu mỏ hóa lỏng thường không được đốt nóng trước khi đốt, và thể tích của chúng so với thể tích của không khí cháy là nhỏ.
Bảng 8.3.
Nhiệt dung thể tích trung bình của khí, kJ / (m3 • ° С)
| Tnhiệt độ, ° С | CO2 | N2 | O2 | CO | CH4 | H2 | H2O (hơi nước) | không khí | |
| khô | ướt trên m3 khí khô nhưng | ||||||||
| 0 | 1,5981 | 1,2970 | 1,3087 | 1,3062 | 1,5708 | 1,2852 | 1,4990 | 1,2991 | 1,3230 |
| 100 | 1,7186 | 1,2991 | 1,3209 | 1,3062 | 1,6590 | 1,2978 | 1,5103 | 1,3045 | 1,3285 |
| 200 | 1,8018 | 1,3045 | 1,3398 | 1,3146 | 1,7724 | 1,3020 | 1,5267 | 1,3142 | 1,3360 |
| 300 | 1,8770 | 1,3112 | 1,3608 | 1,3230 | 1,8984 | 1,3062 | 1,5473 | 1,3217 | 1,3465 |
| 400 | 1,9858 | 1,3213 | 1,3822 | 1,3356 | 2,0286 | 1,3104 | 1,5704 | 1,3335 | 1,3587 |
| 500 | 2,0030 | 1,3327 | 1,4024 | 1,3482 | 2,1504 | 1,3104 | 1,5943 | 1,3469 | 1,3787 |
| 600 | 2,0559 | 1,3453 | 1,4217 | 1,3650 | 2,2764 | 1,3146 | 1,6195 | 1,3612 | 1,3873 |
| 700 | 2,1034 | 1,3587 | 1,3549 | 1,3776 | 2,3898 | 1,3188 | 1,6464 | 1,3755 | 1,4020 |
| 800 | 2,1462 | 1,3717 | 1,4549 | 1,3944 | 2,5032 | 1,3230 | 1,6737 | 1,3889 | 1,4158 |
| 900 | 2,1857 | 1,3857 | 1,4692 | 1,4070 | 2,6040 | 1,3314 | 1,7010 | 1,4020 | 1,4293 |
| 1000 | 2,2210 | 1,3965 | 1,4822 | 1,4196 | 2,7048 | 1,3356 | 1,7283 | 1,4141 | 1,4419 |
| 1100 | 2,2525 | 1,4087 | 1,4902 | 1,4322 | 2,7930 | 1,3398 | 1,7556 | 1,4263 | 1,4545 |
| 1200 | 2,2819 | 1,4196 | 1,5063 | 1,4448 | 2,8812 | 1,3482 | 1,7825 | 1,4372 | 1,4658 |
| 1300 | 2,3079 | 1,4305 | 1,5154 | 1,4532 | — | 1,3566 | 1,8085 | 1,4482 | 1,4771 |
| 1400 | 2,3323 | 1,4406 | 1,5250 | 1,4658 | — | 1,3650 | 1,8341 | 1,4582 | 1,4876 |
| 1500 | 2,3545 | 1,4503 | 1,5343 | 1,4742 | — | 1,3818 | 1,8585 | 1,4675 | 1,4973 |
| 1600 | 2,3751 | 1,4587 | 1,5427 | — | — | — | 1,8824 | 1,4763 | 1,5065 |
| 1700 | 2,3944 | 1,4671 | 1,5511 | — | — | — | 1,9055 | 1,4843 | 1,5149 |
| 1800 | 2,4125 | 1,4746 | 1,5590 | — | — | — | 1,9278 | 1,4918 | 1,5225 |
| 1900 | 2,4289 | 1,4822 | 1,5666 | — | — | — | 1,9698 | 1,4994 | 1,5305 |
| 2000 | 2,4494 | 1,4889 | 1,5737 | 1,5078 | — | — | 1,9694 | 1,5376 | 1,5376 |
| 2100 | 2,4591 | 1,4952 | 1,5809 | — | — | — | 1,9891 | — | — |
| 2200 | 2,4725 | 1,5011 | 1,5943 | — | — | — | 2,0252 | — | — |
| 2300 | 2,4860 | 1,5070 | 1,5943 | — | — | — | 2,0252 | — | — |
| 2400 | 2,4977 | 1,5166 | 1,6002 | — | — | — | 2,0389 | — | — |
| 2500 | 2,5091 | 1,5175 | 1,6045 | — | — | — | 2,0593 | — | — |
Vì vậy, khi xác định nhiệt lượng có thể bỏ qua nhiệt lượng của các chất khí. Khi đốt các chất khí có nhiệt trị thấp (máy phát điện, lò cao, ...), nhiệt lượng của chúng (đặc biệt là đốt nóng trước khi đốt) có ảnh hưởng rất đáng kể đến nhiệt lượng.
Sự phụ thuộc của nhiệt lượng của khí thiên nhiên của thành phần trung bình trong không khí có nhiệt độ 0 ° C và độ ẩm 1% vào hệ số không khí dư a được cho trong Bảng. 8.5, đối với LPG khi nó được đốt cháy trong không khí khô - trong bảng. 8.7. Bảng dữ liệu. 8.5-8.7 có thể được hướng dẫn với độ chính xác đầy đủ khi thiết lập nhiệt lượng đo của quá trình đốt cháy các khí tự nhiên khác, có thành phần tương đối giống nhau và các khí hydrocacbon có thành phần gần như bất kỳ. Nếu cần nhiệt độ cao khi đốt các khí có hệ số không khí thừa thấp, cũng như để tăng hiệu suất của lò, trong thực tế, không khí bị đốt nóng dẫn đến nhiệt lượng tăng (xem bảng 8.6) .
Bảng 8.4.
Khả năng gia nhiệt của khí trong không khí khô
| Khí đơn giản | Công suất làm nóng, ° С | Khí phức hợp có thành phần trung bình | Công suất sưởi gần đúng, ° С |
| Hydrogen | 2235 | Mỏ khí đốt tự nhiên | 2040 |
| Cacbon monoxit | 2370 | Mỏ dầu tự nhiên | 2080 |
| Mêtan | 2043 | than cốc | 2120 |
| Etane | 2097 | Chưng cất đá phiến ở nhiệt độ cao | 1980 |
| Propan | 2110 | Vụ nổ hơi oxy dưới áp suất | 2050 |
| Butan | 2118 | Máy phát điện than béo | 1750 |
| Pentane | 2119 | Máy phát điện thổi hơi nước từ nhiên liệu nạc | 1670 |
| Etylen | 2284 | Hóa lỏng (50% C3H4 + 50% C4H10) | 2115 |
| Axetylen | 2620 | Nước | 2210 |
Bảng 8.5.
Nhiệt lượng và nhiệt độ lý thuyết của quá trình đốt cháy khí tự nhiên trong không khí với t = 0 ° С và độ ẩm 1% * phụ thuộc vào hệ số không khí dư a
| Tỷ lệ không khí dư a | Nhiệt lượng nhiệt độ đốt cháy tк, ° С | Lý thuyết nhiệt độ đốt cháy | Tỷ lệ không khí dư a | Nhiệt lượng nhiệt độ đốt cháy tк, ° С |
| 1,0 | 2010 | 1920 | 1,33 | 1620 |
| 1,02 | 1990 | 1900 | 1,36 | 1600 |
| 1,03 | 1970 | 1880 | 1,40 | 1570 |
| 1,05 | 1940 | 1870 | 1,43 | 1540 |
| 1,06 | 1920 | 1860 | 1,46 | 1510 |
| 1,08 | 1900 | 1850 | 1,50 | 1470 |
| 1,10 | 1880 | 1840 | 1,53 | 1440 |
| 1,12 | 1850 | 1820 | 1,57 | 1410 |
| 1,14 | 1820 | 1790 | 1,61 | 1380 |
| 1,16 | 1800 | 1770 | 1,66 | 1350 |
| 1,18 | 1780 | 1760 | 1,71 | 1320 |
| 1,20 | 1760 | 1750 | 1,76 | 1290 |
| 1,22 | 1730 | — | 1,82 | 1260 |
| 1,25 | 1700 | — | 1,87 | 1230 |
| 1,28 | 1670 | — | 1,94 | 1200 |
| 1,30 | 1650 | — | 2,00 | 1170 |
>
Nhiệt độ đốt cháy lý thuyết tT là nhiệt độ tối đa được xác định tương tự như nhiệt độ đo nhiệt lượng tK, nhưng có sự hiệu chỉnh đối với các phản ứng thu nhiệt (cần nhiệt) phân ly khí cacbonic và hơi nước, dẫn đến sự tăng thể tích:
СО2 ‹–› СО + 0,5О2 - 283 mJ / mol (8.13)
Н2О ‹–› Н2 + 0,5О2 - 242 mJ / mol (8.14)
Ở nhiệt độ cao, sự phân ly có thể dẫn đến sự hình thành các nhóm hydroxyl nguyên tử hydro, oxy và OH. Ngoài ra, quá trình đốt cháy khí luôn tạo ra một lượng nitơ oxit. Tất cả các phản ứng này đều thu nhiệt và dẫn đến giảm nhiệt độ đốt cháy.
Bảng 8.6.
Nhiệt lượng của quá trình đốt cháy khí tự nhiên tу, ° С, tùy thuộc vào tỷ lệ giữa không khí khô dư thừa và nhiệt độ của nó (các giá trị làm tròn)
| Tỷ lệ không khí dư a | Nhiệt độ không khí khô, ° С | ||||||||
| 20 | 100 | 200 | 300 | 400 | 500 | 600 | 700 | 800 | |
| 0,5 | 1380 | 1430 | 1500 | 1545 | 1680 | 1680 | 1740 | 1810 | 1860 |
| 0,6 | 1610 | 1650 | 1715 | 1780 | 1840 | 1900 | 1960 | 2015 | 2150 |
| 0,7 | 1730 | 1780 | 1840 | 1915 | 1970 | 2040 | 2100 | 2200 | 2250 |
| 0,8 | 1880 | 1940 | 2010 | 2060 | 2130 | 2200 | 2260 | 2330 | 2390 |
| 0,9 | 1980 | 2030 | 2090 | 2150 | 2220 | 2290 | 2360 | 2420 | 2500 |
| 1,0 | 2050 | 2120 | 2200 | 2250 | 2320 | 2385 | 2450 | 2510 | 2560 |
| 1,2 | 1810 | 1860 | 1930 | 2000 | 2070 | 2140 | 2200 | 2280 | 2350 |
| 1,4 | 1610 | 1660 | 1740 | 1800 | 2870 | 1950 | 2030 | 2100 | 2160 |
| 1,6 | 1450 | 1510 | 1560 | 1640 | 1730 | 1800 | 1860 | 1950 | 2030 |
| 1,8 | 1320 | 1370 | 1460 | 1520 | 1590 | 1670 | 1740 | 1830 | 1920 |
| 2,0 | 1220 | 1270 | 1360 | 1420 | 1490 | 1570 | 1640 | 1720 | 1820 |
Bảng 8.7.
Nhiệt lượng đốt cháy tK của propan thương phẩm trong không khí khô với t = 0 ° С phụ thuộc vào hệ số không khí dư a
| Tỷ lệ không khí dư a | Nhiệt lượng đốt cháy tH, ° С | Tỷ lệ không khí dư a | Nhiệt lượng đốt cháy tK, ° С |
| 1,0 | 2110 | 1,45 | 1580 |
| 1,02 | 2080 | 1,48 | 1560 |
| 1,04 | 2050 | 1,50 | 1540 |
| 1,05 | 2030 | 1,55 | 1500 |
| 1,07 | 2010 | 1,60 | 1470 |
| 1,10 | 1970 | 1,65 | 1430 |
| 1,12 | 1950 | 1,70 | 1390 |
| 1,15 | 1910 | 1,75 | 1360 |
| 1,20 | 1840 | 1,80 | 1340 |
| 1,25 | 1780 | 1,85 | 1300 |
| 1,27 | 1750 | 1,90 | 1270 |
| 1,30 | 1730 | 1,95 | 1240 |
| 1,35 | 1670 | 2,00 | 1210 |
| 1,40 | 1630 | 2,10 | 1170 |
Nhiệt độ cháy lý thuyết có thể được xác định theo công thức sau:
tT = (Qн + qphys - qdis) / (ΣVcp) (8.15)
Trong đó qduc là tổng nhiệt lượng tiêu thụ cho sự phân ly СО2 và Н2О trong sản phẩm cháy, kJ / m3; IVcp - tổng tích của thể tích và nhiệt dung trung bình của các sản phẩm cháy, có tính đến độ phân ly trên 1 m3 khí.
Như bạn có thể thấy từ bảng. 8.8, ở nhiệt độ lên đến 1600 ° C, mức độ phân ly có thể được bỏ qua, và nhiệt độ cháy lý thuyết có thể được lấy bằng nhiệt lượng. Ở nhiệt độ cao hơn, mức độ phân ly có thể làm giảm đáng kể nhiệt độ trong không gian làm việc. Trong thực tế, không có nhu cầu đặc biệt này, nhiệt độ đốt cháy lý thuyết phải được xác định chỉ đối với các lò nhiệt độ cao hoạt động trên không khí đã được làm nóng trước (ví dụ, lò nung hở). Không cần thiết cho điều này đối với các nhà máy lò hơi.
Nhiệt độ thực tế (tính toán) của sản phẩm cháy td là nhiệt độ đạt được trong điều kiện thực tại điểm nóng nhất của ngọn lửa. Nó thấp hơn lý thuyết và phụ thuộc vào nhiệt lượng thất thoát ra môi trường, mức độ truyền nhiệt từ vùng cháy bằng bức xạ, độ dài của quá trình cháy trong thời gian v.v ... Nhiệt độ trung bình thực tế trong lò nung và lò hơi là được xác định bằng cân bằng nhiệt hoặc xấp xỉ bằng nhiệt độ cháy lý thuyết hoặc nhiệt lượng đối với nhiệt độ trong lò với việc đưa các hệ số hiệu chỉnh đã được thiết lập bằng thực nghiệm vào chúng:
td = t (8.16)
trong đó n - t. n. hệ số pyrometric trong:
- đối với lò sưởi và lò sưởi chất lượng cao có cách nhiệt - 0,75-0,85;
- đối với lò kín không có lớp cách nhiệt - 0,70-0,75;
- đối với lò hơi được che chắn - 0,60-0,75.
Trong thực tế, không chỉ cần biết nhiệt độ đốt cháy đoạn nhiệt đã cho ở trên mà còn cả nhiệt độ cực đại xảy ra trong ngọn lửa. Các giá trị gần đúng của chúng thường được thiết lập bằng thực nghiệm bằng các phương pháp quang phổ. Nhiệt độ tối đa phát sinh trong ngọn lửa tự do ở khoảng cách 5-10 mm tính từ đỉnh phía trước của đốt hình nón được cho trong bảng. 8,9. Phân tích dữ liệu được trình bày cho thấy nhiệt độ tối đa trong ngọn lửa nhỏ hơn nhiệt lượng tỏa ra (do tiêu thụ nhiệt cho sự phân ly của H2O và CO2 và loại bỏ nhiệt ra khỏi vùng ngọn lửa).
- Trang Chủ
- Danh mục
- Đặc điểm cháy của khí
- Nhiệt độ đốt cháy
Quá trình đốt cháy - sản phẩm dầu
Việc đốt cháy các sản phẩm dầu trong bờ bao của bể chứa được loại bỏ bằng cách cung cấp ngay bọt.
Việc đốt cháy các sản phẩm dầu trong bờ bao của bể chứa được loại bỏ bằng cách cung cấp bọt ngay lập tức.
Trong quá trình đốt cháy các sản phẩm dầu mỏ, nhiệt độ sôi của chúng (xem Bảng 69) tăng dần do quá trình chưng cất phân đoạn đang diễn ra, liên quan đến việc nhiệt độ của lớp trên cũng tăng lên.
| K Sơ đồ hệ thống cấp nước chữa cháy làm mát bể đốt qua vòng tưới .. |
Khi đốt dầu trong két, phần trên của dây đai phía trên của két tiếp xúc với ngọn lửa. Khi đốt dầu ở mức thấp hơn, chiều cao của mặt tự do của thùng tiếp xúc với ngọn lửa có thể đáng kể. Trong chế độ đốt cháy này, bể chứa có thể bị sụp đổ. Nước từ vòi phun lửa hoặc từ các vòng tưới tĩnh, rơi vào phần bên ngoài của thành trên của bể, làm nguội chúng (Hình.15.1), do đó ngăn ngừa tai nạn và lan truyền dầu vào nền đắp, tạo điều kiện thuận lợi hơn cho việc sử dụng bọt cơ khí.
Kết quả của việc nghiên cứu quá trình đốt cháy các sản phẩm dầu mỏ và hỗn hợp của chúng là rất thú vị.
Nhiệt độ của nó trong quá trình đốt cháy các sản phẩm dầu mỏ là: xăng 1200 C, dầu máy kéo 1100 C, nhiên liệu điêzen 1100 C, dầu thô 1100 C, dầu mazut 1000 C. Khi đốt củi thành đống, nhiệt độ của ngọn lửa hỗn loạn lên tới 1200 - 1300 C.
Các nghiên cứu đặc biệt lớn trong lĩnh vực vật lý về quá trình đốt cháy các sản phẩm dầu mỏ và sự dập tắt của chúng đã được thực hiện trong 15 năm qua tại Viện Nghiên cứu Phòng cháy Trung ương (TsNIIPO), Viện Năng lượng thuộc Viện Hàn lâm Khoa học Liên Xô (ENIN) và một số viện nghiên cứu và giáo dục khác.
Một ví dụ về xúc tác âm là ngăn chặn quá trình đốt cháy các sản phẩm dầu mỏ với việc bổ sung các hydrocacbon halogen hóa.
Nước thúc đẩy sự tạo bọt và hình thành nhũ tương trong quá trình đốt cháy các sản phẩm dầu mỏ có điểm chớp cháy từ 120 C trở lên. Nhũ tương, bao phủ bề mặt của chất lỏng, cô lập nó với oxy trong không khí, và cũng ngăn cản sự thoát hơi từ nó.
| Tốc độ cháy của các khí hiđrocacbon hóa lỏng trong bình đẳng nhiệt. |
Quá trình đốt cháy các khí hydrocacbon hóa lỏng trong bình đẳng nhiệt không khác với quá trình đốt các sản phẩm dầu mỏ. Tốc độ cháy trong trường hợp này có thể được tính theo công thức (13) hoặc xác định bằng thực nghiệm. Đặc thù của quá trình đốt cháy chất khí hoá lỏng trong điều kiện đẳng nhiệt là nhiệt độ của toàn bộ khối chất lỏng trong bình bằng nhiệt độ sôi ở áp suất khí quyển. Đối với hydro, metan, etan, propan và butan, các nhiệt độ này lần lượt là - 252, - 161, - 88, - 42 và 0 5 C.
| Sơ đồ lắp đặt máy phát điện GVPS-2000 trên bồn chứa. |
Nghiên cứu và thực hành chữa cháy đã chỉ ra rằng để ngăn chặn sự cháy của sản phẩm dầu, bọt phải bao phủ hoàn toàn toàn bộ bề mặt của nó một lớp có độ dày nhất định. Tất cả các loại bọt có tỷ lệ giãn nở thấp đều không hiệu quả trong việc dập tắt đám cháy các sản phẩm dầu trong các bể chứa ở mức ngập lụt thấp hơn. Bọt, rơi từ độ cao lớn (6 - 8 m) xuống bề mặt nhiên liệu, được nhúng và bao bọc trong màng nhiên liệu, cháy hết hoặc nhanh chóng xẹp xuống. Chỉ có thể ném bọt với đa số 70 - 150 vào bể đang cháy bằng các tia phun có bản lề.
| Tàn lửa. |